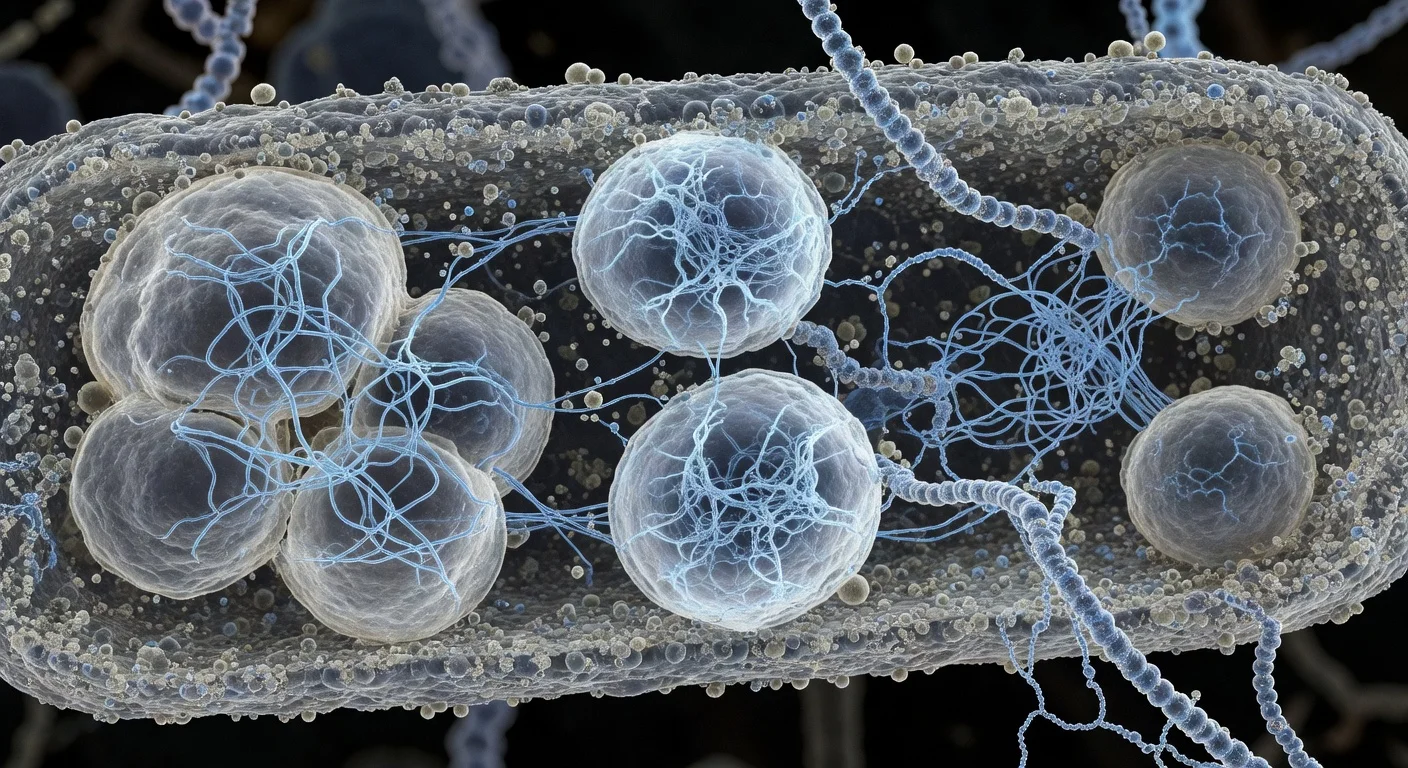
Des scientifiques de Scripps Research rapportent que certains condensats biomoléculaires —compartiments cellulaires sans membrane, semblables à des gouttelettes— contiennent des réseaux de filaments protéiques fins agissant comme une charpente interne. L'équipe indique que perturber cette architecture filamentaire modifie les propriétés physiques des condensats et altère la croissance bactérienne et la ségrégation de l'ADN, ouvrant la possibilité que la structure des condensats puisse un jour être ciblée thérapeutiquement dans des maladies comme le cancer et la SLA. L'étude est parue dans Nature Structural & Molecular Biology le 2 février 2026.
Les condensats biomoléculaires sont des agrégats en forme de gouttelettes qui aident les cellules à organiser des activités clés sans membranes. Les chercheurs les décrivent comme impliqués dans des processus incluant la régulation de la conversion des instructions génétiques de l'ADN en protéines, l'élimination de déchets cellulaires potentiellement toxiques et la contribution à des mécanismes supprimant la croissance tumorale. Dans un travail axé sur une protéine bactérienne appelée PopZ, une équipe dirigée par Scripps Research a examiné comment ces compartiments sans membrane peuvent avoir une organisation fonctionnelle. Chez certaines bactéries en forme de bâtonnet, PopZ s'accumule aux pôles cellulaires et forme des condensats recrutant d'autres protéines nécessaires aux processus liés à la division cellulaire. En utilisant la tomographie cryo-électronique —une approche que les chercheurs comparent à un scanner CT à l'échelle moléculaire—, l'équipe rapporte que les molécules de PopZ s'assemblent en filaments fins via un processus ordonné étape par étape. Ces filaments forment une charpente interne aidant à déterminer les caractéristiques physiques du condensat. L'étude a également utilisé le transfert d'énergie de résonance Förster à molécule unique (FRET) pour sonder le comportement de PopZ au niveau des molécules individuelles. Les chercheurs rapportent que PopZ adopte différentes conformations selon qu'il est à l'intérieur ou à l'extérieur du condensat. « Comprendre que la conformation protéique dépend de l'emplacement nous donne plusieurs façons d'ingénier la fonction cellulaire », a déclaré Daniel Scholl, premier auteur de l'article et ancien chercheur post-doctorant dans les laboratoires Lasker et Deniz. Pour tester si le réseau de filaments est requis pour la fonction normale, l'équipe a conçu une variante de PopZ incapable de former des filaments. Selon les chercheurs, les condensats modifiés étaient plus fluides et avaient une tension de surface réduite. Introduits dans des bactéries, ces changements étaient associés à un arrêt de croissance et des échecs dans la ségrégation de l'ADN. Bien que les expériences portent sur un système bactérien, Scripps Research indique que les résultats pourraient éclairer la réflexion des scientifiques sur les condensats dans les cellules humaines. L'organisation de recherche pointe des condensats à base de filaments impliqués dans le contrôle qualité des protéines et la régulation de la croissance —processus liés aux maladies neurodégénératives et à la biologie du cancer— et suggère qu'une architecture de condensat définissable pourrait offrir de nouveaux points d'entrée thérapeutiques. L'article, intitulé « The filamentous ultrastructure of the PopZ condensate is required for its cellular function », liste Keren Lasker comme auteure principale, avec Ashok A. Deniz et Raphael Park comme auteurs correspondants conjoints. Les auteurs supplémentaires cités dans le communiqué de l'organisation incluent Tumara Boyd, Andrew P. Latham, Alexandra Salazar, Asma M. A. M. Khan, Steven Boeynaems, Alex S. Holehouse, Gabriel C. Lander et Andrej Sali. Scripps Research a indiqué que le travail a été soutenu par des financeurs incluant les National Institutes of Health et la National Science Foundation, entre autres.