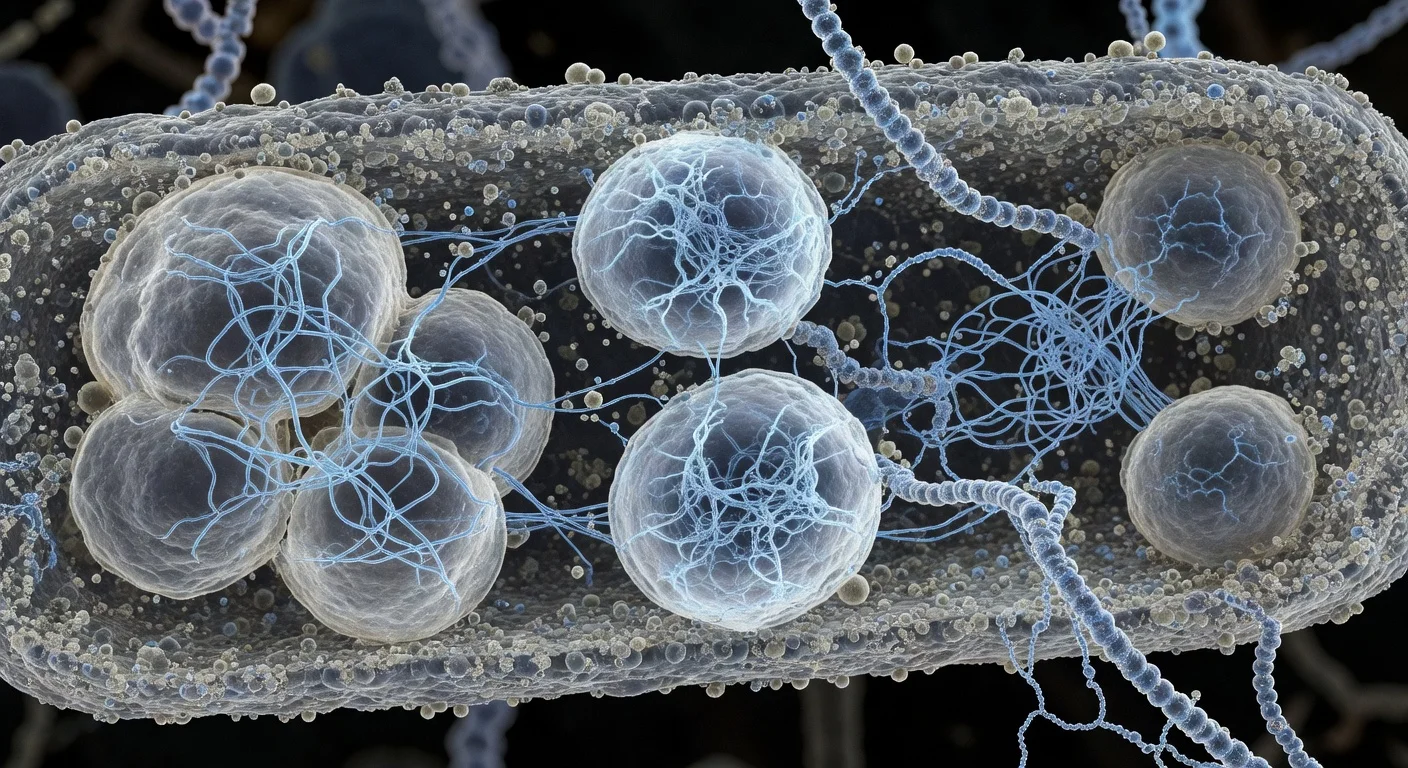
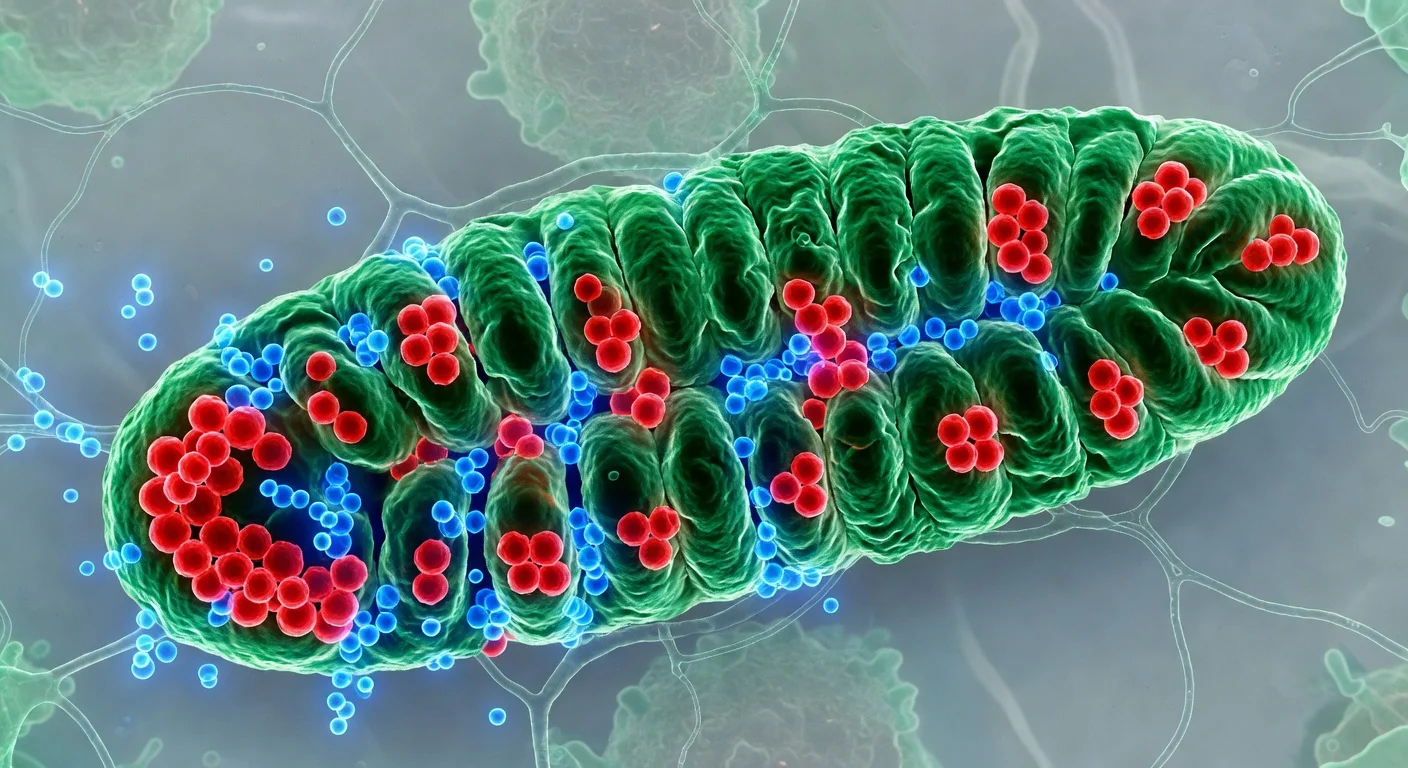
Forskare vid Scripps Research rapporterar att vissa biomolekylära kondensat —membranlösa, droppliknande cellkompartment— innehåller nätverk av tunna proteinfilament som fungerar som ett internt ställverk. Teamet säger att störning av denna filamentarkitektur förändrar kondensatets fysikaliska egenskaper och försämrar bakteriell tillväxt och DNA-segregation, vilket väcker möjligheten att kondensatstrukturen en dag kan vara terapeutiskt målbart i sjukdomar som cancer och ALS. Studien publicerades i Nature Structural & Molecular Biology den 2 februari 2026.
Biomolekylära kondensat är droppliknande kluster som hjälper celler att organisera nyckelaktiviteter utan membran. Forskare beskriver dem som inblandade i processer som inkluderar att reglera hur genetiska instruktioner i DNA omvandlas till proteiner, hjälpa till att rensa potentiellt toxiskt cellavfall och bidra till mekanismer som kan hämma tumörtillväxt. I ett arbete fokuserat på ett bakteriellt protein kallat PopZ undersökte ett Scripps Research-ledt team hur dessa membranlösa kompartment kan ha funktionell organisation. I vissa stavformade bakterier ackumuleras PopZ vid cellpolerna och bildar kondensat som rekryterar andra proteiner som behövs för cell-delningrelaterade processer. Med hjälp av kryo-elektron-tomografi —en metod som forskarna liknar vid en CT-skanning i molekylär skala — rapporterar teamet att PopZ-molekyler samlas till tunna filament genom en ordnad, steg-för-steg-process. Dessa filament bildar ett internt ställverk som hjälper till att bestämma kondensatets fysikaliska egenskaper. Studien använde också single-molecule Förster-resonansenergiöverföring (FRET) för att undersöka PopZ-beteende på individmoleculellnivå. Forskarna rapporterar att PopZ antar olika konformationer beroende på om det är inne i eller utanför kondensatet. «Att inse att proteinets konformation beror på platsen ger oss flera sätt att ingeniörera cellfunktion», sa Daniel Scholl, artikelns förstaförfattare och tidigare postdoc i Lasker- och Deniz-labb. För att testa om filamentnätverket krävs för normal funktion konstruerade teamet en PopZ-variant som inte kunde bilda filament. Enligt forskarna var de förändrade kondensaten mer flytande och hade minskad ytspänning. När de introducerades i bakterier associerades förändringarna med stoppad tillväxt och misslyckanden i DNA-segregation. Även om experimenten centrerades på ett bakteriellt system säger Scripps Research att resultaten kan informera hur forskare tänker om kondensat i humana celler också. Forskningsorganisationen pekade på filamentbaserade kondensat som är implicerade i proteinkvalitetskontroll och tillväxtreglering —processer kopplade till neurodegenerativa sjukdomar och cancerbiologi — och föreslog att definierbar kondensatarkitektur slutligen kan ge nya terapeutiska ingångar. Artikeln, med titeln «The filamentous ultrastructure of the PopZ condensate is required for its cellular function», listar Keren Lasker som seniorförfattare, med Ashok A. Deniz och Raphael Park som medsvarande författare. Ytterligare författare nämnda i forskningsorganisationens pressmeddelande inkluderar Tumara Boyd, Andrew P. Latham, Alexandra Salazar, Asma M. A. M. Khan, Steven Boeynaems, Alex S. Holehouse, Gabriel C. Lander och Andrej Sali. Scripps Research säger att arbetet stöddes av finansiärer inklusive National Institutes of Health och National Science Foundation, bland andra.