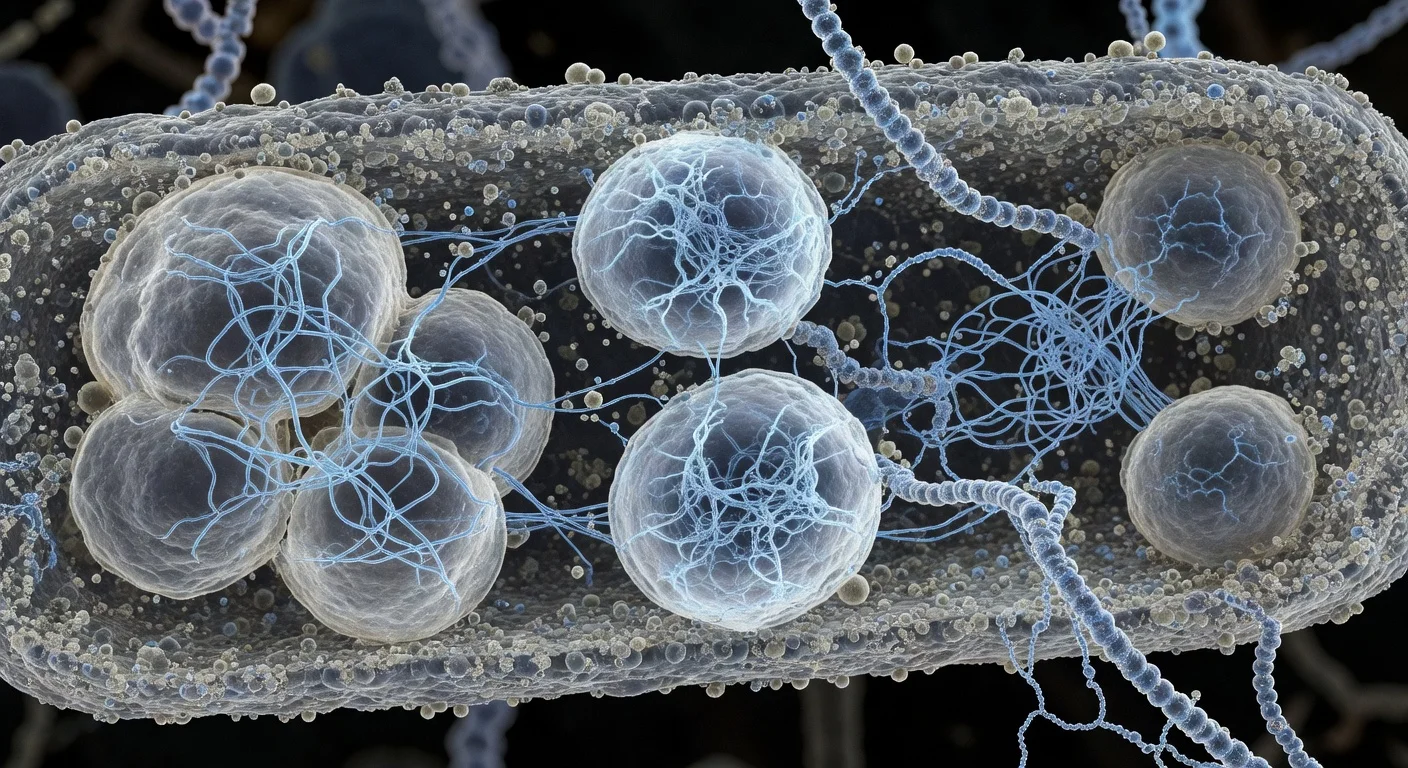
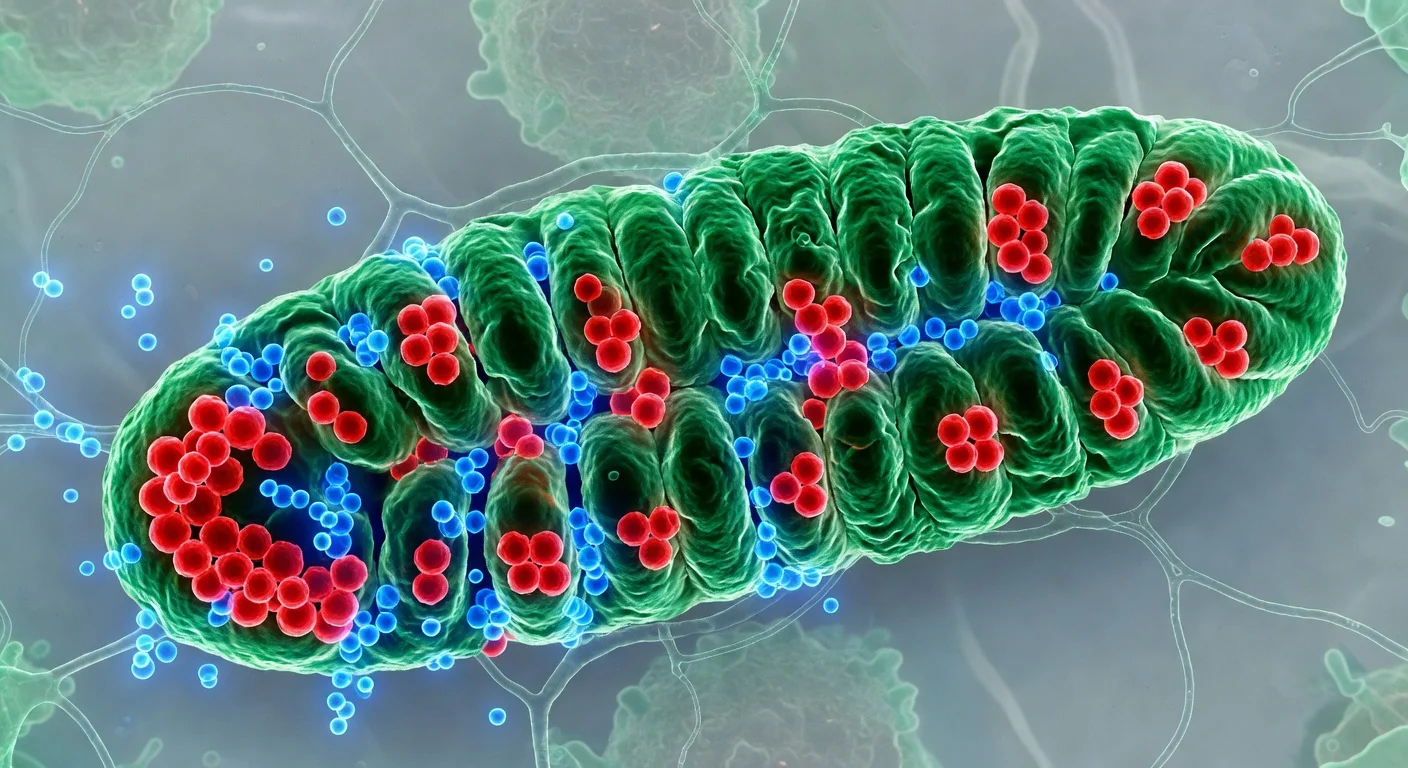
Científicos de Scripps Research informan que algunos condensados biomoleculares —compartimentos celulares sin membrana, similares a gotas— contienen redes de filamentos proteicos delgados que actúan como un andamio interno. El equipo dice que alterar esta arquitectura de filamentos modifica las propiedades físicas de los condensados e perjudica el crecimiento bacteriano y la segregación del ADN, lo que plantea la posibilidad de que la estructura de los condensados pueda ser un objetivo terapéutico en enfermedades como el cáncer y la ELA. El estudio apareció en Nature Structural & Molecular Biology el 2 de febrero de 2026.
Los condensados biomoleculares son racimos similares a gotas que ayudan a las células a organizar actividades clave sin membranas. Los investigadores los describen como implicados en procesos que incluyen regular cómo las instrucciones genéticas del ADN se convierten en proteínas, ayudar a eliminar residuos celulares potencialmente tóxicos y contribuir a mecanismos que pueden suprimir el crecimiento tumoral. En un trabajo centrado en una proteína bacteriana llamada PopZ, un equipo liderado por Scripps Research examinó cómo estos compartimentos sin membrana pueden tener una organización funcional. En ciertas bacterias en forma de bastón, PopZ se acumula en los polos celulares y forma condensados que reclutan otras proteínas necesarias para procesos relacionados con la división celular. Utilizando tomografía de electrones criogénicos —un enfoque que los investigadores comparan con una tomografía computarizada a escala molecular—, el equipo informa que las moléculas de PopZ se ensamblan en filamentos delgados mediante un proceso ordenado paso a paso. Esos filamentos forman un andamio interno que ayuda a determinar las características físicas del condensado. El estudio también utilizó transferencia de energía de resonancia de Förster a nivel de molécula única (FRET) para sondar el comportamiento de PopZ a nivel de moléculas individuales. Los investigadores informan que PopZ adopta diferentes conformaciones dependiendo de si está dentro o fuera del condensado. «Darnos cuenta de que la conformación de la proteína depende de la ubicación nos da múltiples formas de ingeniar la función celular», dijo Daniel Scholl, primer autor del artículo y exinvestigador postdoctoral en los laboratorios de Lasker y Deniz. Para probar si la red de filamentos es necesaria para la función normal, el equipo diseñó una variante de PopZ que no podía formar filamentos. Según los investigadores, los condensados alterados eran más fluidos y tenían una tensión superficial reducida. Cuando se introdujeron en bacterias, los cambios se asociaron con el crecimiento detenido y fallos en la segregación del ADN. Aunque los experimentos se centraron en un sistema bacteriano, Scripps Research dijo que los hallazgos pueden informar sobre cómo los científicos piensan en los condensados en células humanas también. La organización de investigación señaló a condensados basados en filamentos implicados en el control de calidad de proteínas y la regulación del crecimiento —procesos relacionados con enfermedades neurodegenerativas y la biología del cáncer— y sugirió que una arquitectura de condensados definible podría eventualmente proporcionar nuevos puntos de entrada terapéuticos. El artículo, titulado «The filamentous ultrastructure of the PopZ condensate is required for its cellular function», lista a Keren Lasker como autora principal, con Ashok A. Deniz y Raphael Park como autores correspondientes conjuntos. Autores adicionales nombrados en el comunicado de la organización de investigación incluyen a Tumara Boyd, Andrew P. Latham, Alexandra Salazar, Asma M. A. M. Khan, Steven Boeynaems, Alex S. Holehouse, Gabriel C. Lander y Andrej Sali. Scripps Research dijo que el trabajo fue apoyado por financiadores que incluyen los National Institutes of Health y la National Science Foundation, entre otros.