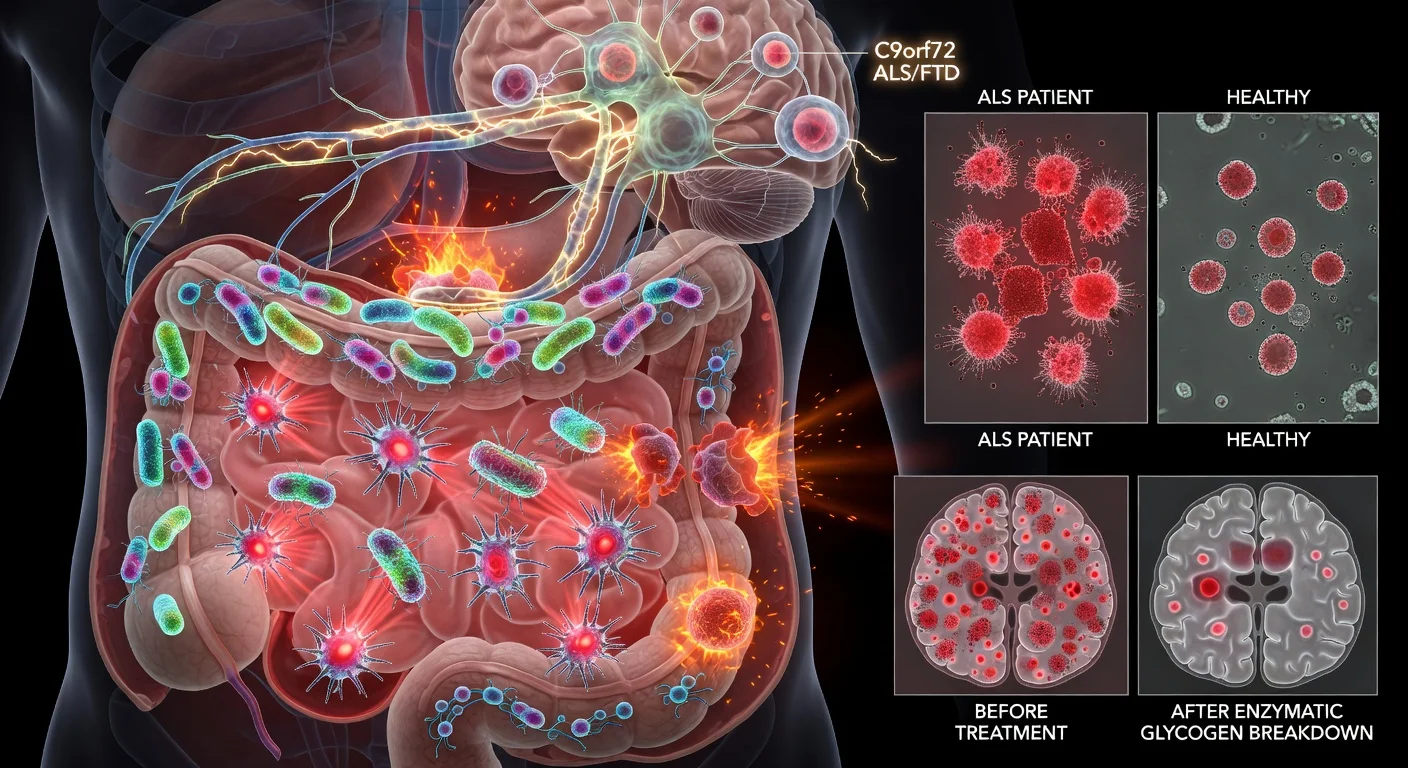
Investigadores de la Case Western Reserve University informan que algunas bacterias intestinales pueden producir formas de glucógeno inusualmente inflamatorias y que este glucógeno microbiano puede activar una respuesta inmunitaria relacionada con la inflamación cerebral en modelos de enfermedades vinculadas a la mutación del gen C9orf72. En muestras de heces de pacientes, el equipo detectó estas formas de glucógeno con mayor frecuencia en casos de ELA y demencia frontotemporal asociada al gen C9orf72 en comparación con controles sanos, y la degradación enzimática del glucógeno en el intestino mejoró los resultados en ratones.
Investigadores de la Case Western Reserve University han reportado evidencia de que ciertas bacterias intestinales pueden producir formas inflamatorias de glucógeno —un carbohidrato que a veces se describe como un “azúcar”— que puede provocar respuestas inmunitarias relevantes para la esclerosis lateral amiotrófica (ELA) y la demencia frontotemporal (DFT), particularmente en entornos que involucran al gen C9orf72.
El estudio, publicado en Cell Reports, se centró en cómo los productos microbianos en el intestino interactúan con el sistema inmunitario en el contexto del C9orf72, un gen en el que una expansión de repeticiones es la causa genética conocida más común de ELA y DFT. En un análisis de muestras fecales humanas descrito en el artículo, se detectaron formas inflamatorias de glucógeno en 15 de 22 muestras de ELA y en 1 de 1 muestra de un paciente con DFT asociada al C9orf72, en comparación con 4 de 12 controles sanos.
Aaron Burberry, profesor asistente en el Departamento de Patología de la Facultad de Medicina de la Case Western Reserve y autor correspondiente del trabajo, señaló que el equipo descubrió que “las bacterias intestinales dañinas producen formas inflamatorias de glucógeno (un tipo de azúcar), y que estos azúcares bacterianos desencadenan respuestas inmunitarias que dañan el cerebro”.
En experimentos realizados con ratones libres de gérmenes, los investigadores informaron que colonizar animales con deficiencia de C9orf72 con una cepa bacteriana productora de glucógeno (incluida Parabacteroides merdae en su modelo) aumentó los cambios inmunitarios sistémicos y los signos de afectación del sistema nervioso central, incluida la alteración de la barrera hematoencefálica y la infiltración de células inmunitarias. También reportaron que digerir enzimáticamente el glucógeno en el intestino disminuyó la reactividad microglial en el cerebro y mejoró la supervivencia en los ratones con deficiencia de C9orf72.
Alex Rodriguez-Palacios, profesor asistente en el Instituto de Investigación de Salud Digestiva de la Facultad de Medicina y coautor del estudio, indicó que el equipo logró reducir el glucógeno dañino en experimentos de formas que “mejoraron la salud cerebral y extendieron la esperanza de vida”, según el resumen de los hallazgos publicado por la universidad.
Los investigadores sostienen que el trabajo ofrece una explicación potencial de por qué solo algunas personas con riesgo genético desarrollan ELA o DFT: la actividad microbiana en el intestino puede actuar como un factor ambiental que influye en las vías inflamatorias vinculadas a la enfermedad. Afirmaron que los resultados apuntan a posibles estrategias terapéuticas, incluidos enfoques destinados a descomponer el glucógeno inflamatorio en el tracto digestivo o atacar los mecanismos que conectan los microbios intestinales con la actividad inmunitaria que afecta al sistema nervioso.
Burberry dijo que el grupo planea estudios más amplios de los microbiomas de los pacientes y señaló que los ensayos clínicos para probar si la degradación del glucógeno podría ralentizar la progresión de la ELA/DFT “podrían comenzar en un año”, según el comunicado de la universidad.