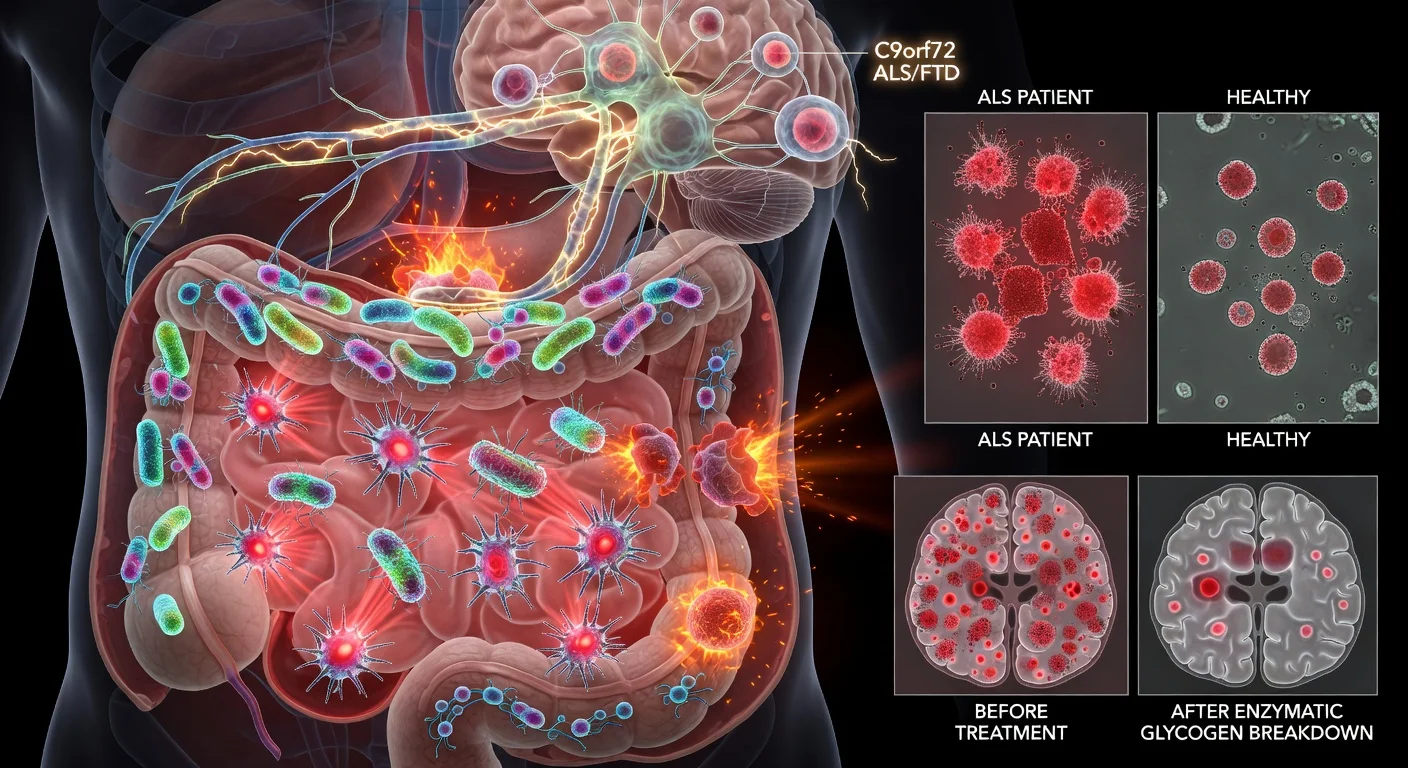
ケース・ウェスタン・リザーブ大学の研究チームは、一部の腸内細菌が炎症を誘発しやすい特殊な形態のグリコーゲンを産生し、それがC9orf72変異に関連する疾患モデルにおいて脳の炎症につながる免疫活性を引き起こす可能性があることを報告した。患者の便サンプルを調査した結果、これらのグリコーゲン形態は、健常な対照群と比較して、ALS患者およびC9orf72関連前頭側頭型認知症患者においてより高い頻度で検出された。また、マウスの実験では、腸内でグリコーゲンを酵素的に分解することで予後の改善が見られた。
ケース・ウェスタン・リザーブ大学の研究チームは、特定の腸内細菌が炎症性のグリコーゲン(「糖」とも呼ばれる炭水化物)を産生し、それが筋萎縮性側索硬化症(ALS)や前頭側頭型認知症(FTD)、特にC9orf72遺伝子が関与する病態において免疫応答を誘発する可能性があることを報告した。
『セル・レポート』誌に掲載された本研究は、ALSおよびFTDの最も一般的な遺伝的原因である反復配列の伸長がみられるC9orf72遺伝子の文脈において、腸内の微生物産物がどのように免疫システムと相互作用するかを調査した。論文に記載されたヒトの糞便サンプルの調査では、炎症性のグリコーゲンがALS患者の22検体中15検体、C9orf72関連FTD患者の1検体中1検体から検出されたのに対し、健常な対照群では12検体中4検体であった。
ケース・ウェスタン・リザーブ大学医学部病理学科の助教であり、本研究の責任著者であるアーロン・バーベリー氏は、「有害な腸内細菌は炎症性のグリコーゲン(糖の一種)を産生し、これらの細菌由来の糖が脳に損傷を与える免疫応答を誘発する」と述べた。
無菌マウスを用いた実験において、研究チームは、C9orf72欠損マウスにグリコーゲンを産生する細菌株(モデルではParabacteroides merdaeを使用)を定着させると、全身性の免疫変化や、血液脳関門の破綻、免疫細胞の浸潤など、中枢神経系への影響の徴候が強まったことを報告した。また、腸内でグリコーゲンを酵素的に分解することで、脳内のミクログリアの反応性が抑えられ、C9orf72欠損マウスの生存率が改善したことも報告された。
医学部消化器健康研究所の助教であり共著者の一人であるアレックス・ロドリゲス・パラシオス氏は、同大学の発表によれば、実験において有害なグリコーゲンを減少させることで「脳の健康が改善し、寿命が延びた」と述べた。
研究チームは、この研究がなぜ遺伝的リスクのある一部の人々だけがALSやFTDを発症するのかという疑問に対して、腸内の微生物活動が疾患に関連する炎症経路に影響を与える環境因子として機能している可能性があるという説明を提供すると論じている。彼らは、消化管内の炎症性グリコーゲンを分解するアプローチや、神経系に影響を与える免疫活動と腸内微生物をつなぐメカニズムを標的とするアプローチなど、可能性のある治療戦略を示唆している。
バーベリー氏によると、同グループは今後、患者のマイクロバイオームに関するより大規模な研究を計画しており、グリコーゲンの分解がALS/FTDの進行を遅らせるかどうかを検証する臨床試験が「1年以内にも開始される可能性がある」と同大学のリリースで述べている。