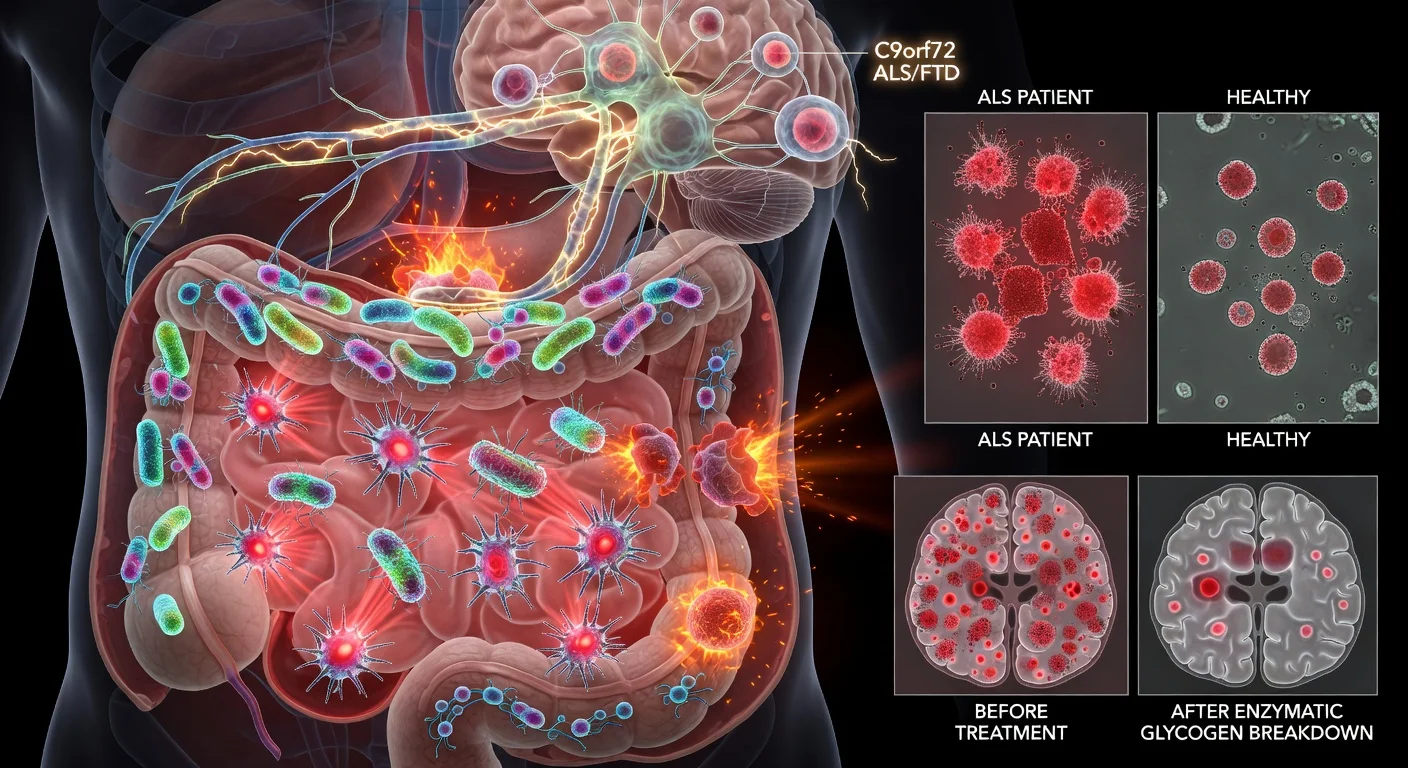
Para peneliti di Case Western Reserve University melaporkan bahwa beberapa bakteri usus dapat menghasilkan bentuk glikogen yang sangat bersifat inflamasi, dan glikogen mikroba ini dapat memicu aktivitas imun yang terkait dengan peradangan otak pada model penyakit yang berhubungan dengan mutasi C9orf72. Dalam sampel feses pasien, tim peneliti menemukan bentuk glikogen ini lebih sering terjadi pada penderita ALS dan demensia frontotemporal terkait C9orf72 dibandingkan dengan kontrol yang sehat, dan penguraian glikogen secara enzimatik di dalam usus terbukti memperbaiki hasil pada tikus.
Para peneliti di Case Western Reserve University telah melaporkan bukti bahwa bakteri usus tertentu dapat memproduksi bentuk glikogen yang bersifat inflamasi—sebuah karbohidrat yang terkadang disebut sebagai “gula”—yang dapat memicu respons imun yang relevan dengan amyotrophic lateral sclerosis (ALS) dan demensia frontotemporal (FTD), terutama dalam kondisi yang melibatkan gen C9orf72.
Studi yang diterbitkan dalam Cell Reports ini berfokus pada bagaimana produk mikroba di dalam usus berinteraksi dengan sistem kekebalan tubuh dalam konteks C9orf72, sebuah gen di mana ekspansi pengulangan merupakan penyebab genetik paling umum yang diketahui dari ALS dan FTD. Dalam survei sampel feses manusia yang dijelaskan dalam makalah tersebut, bentuk glikogen inflamasi terdeteksi pada 15 dari 22 sampel ALS dan 1 dari 1 sampel dari pasien dengan FTD terkait C9orf72, dibandingkan dengan 4 dari 12 sampel kontrol yang sehat.
Aaron Burberry, seorang asisten profesor di Departemen Patologi di Case Western Reserve School of Medicine dan penulis korespondensi dalam penelitian ini, mengatakan bahwa timnya menemukan bahwa “bakteri usus yang berbahaya memproduksi bentuk glikogen inflamasi (sejenis gula), dan gula bakteri ini memicu respons imun yang merusak otak.”
Dalam eksperimen yang menggunakan tikus bebas kuman, para peneliti melaporkan bahwa mengolonisasi hewan yang kekurangan C9orf72 dengan galur bakteri penghasil glikogen (termasuk Parabacteroides merdae dalam model mereka) meningkatkan perubahan imun sistemik dan tanda-tanda keterlibatan sistem saraf pusat, termasuk gangguan sawar darah otak dan infiltrasi sel imun. Mereka juga melaporkan bahwa pencernaan glikogen secara enzimatik di dalam usus meredam reaktivitas mikroglia di otak dan meningkatkan kelangsungan hidup pada tikus yang kekurangan C9orf72.
Alex Rodriguez-Palacios, seorang asisten profesor di Digestive Health Research Institute di School of Medicine dan salah satu penulis, mengatakan bahwa timnya mampu mengurangi glikogen berbahaya dalam eksperimen dengan cara yang “meningkatkan kesehatan otak dan memperpanjang umur,” menurut ringkasan temuan universitas tersebut.
Para peneliti berpendapat bahwa pekerjaan ini menawarkan penjelasan potensial mengapa hanya sebagian orang yang berisiko secara genetik yang menderita ALS atau FTD: aktivitas mikroba di dalam usus mungkin berfungsi sebagai faktor lingkungan yang memengaruhi jalur inflamasi yang terkait dengan penyakit tersebut. Mereka mengatakan hasil tersebut mengarah pada kemungkinan strategi terapeutik, termasuk pendekatan yang ditujukan untuk menguraikan glikogen inflamasi di saluran pencernaan atau menargetkan mekanisme yang menghubungkan mikroba usus dengan aktivitas imun yang memengaruhi sistem saraf.
Burberry mengatakan kelompoknya merencanakan studi yang lebih besar terhadap mikrobioma pasien dan mengatakan uji klinis untuk menguji apakah degradasi glikogen dapat memperlambat perkembangan ALS/FTD “dapat dimulai dalam setahun,” menurut rilis universitas.