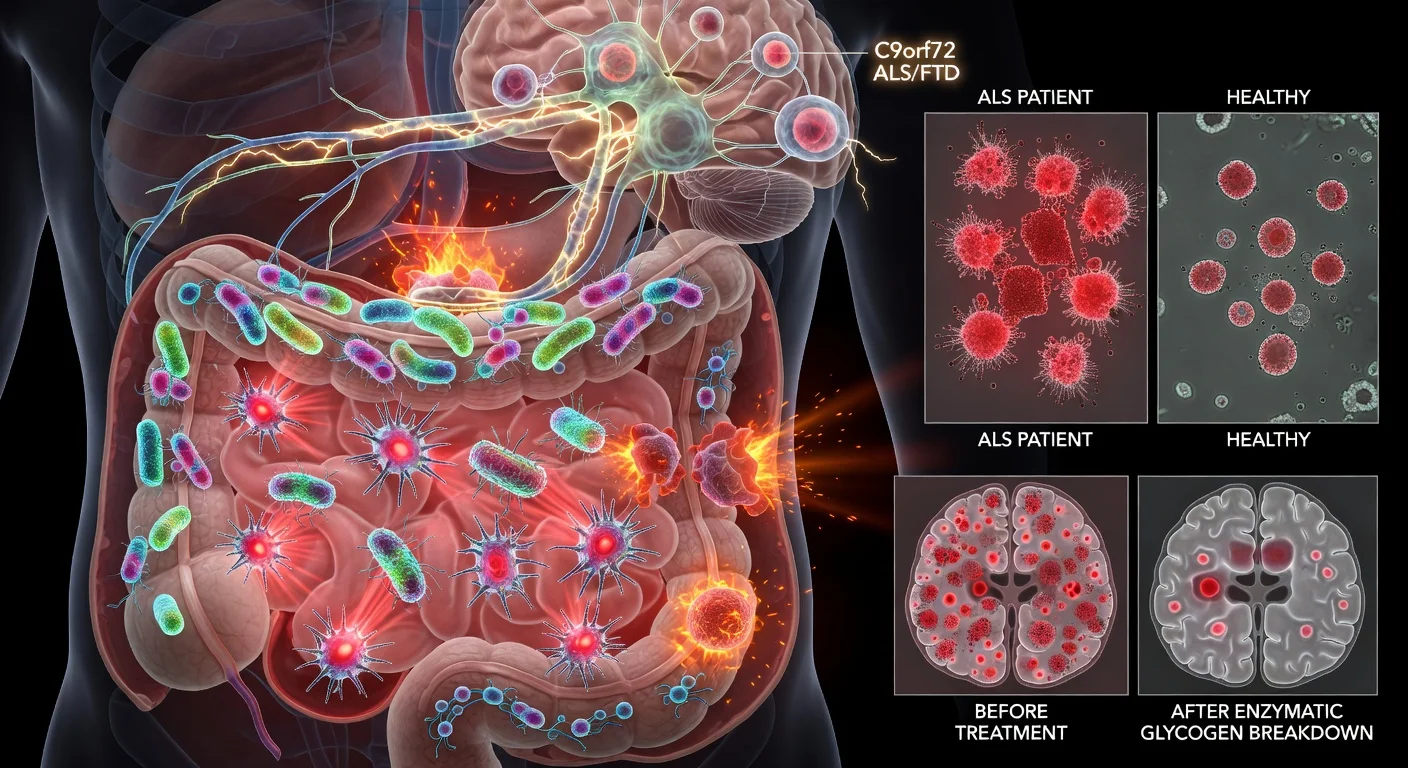
Des chercheurs de l'Université Case Western Reserve rapportent que certaines bactéries intestinales peuvent produire des formes anormalement inflammatoires de glycogène et que ce glycogène microbien peut déclencher une activité immunitaire liée à l'inflammation cérébrale dans des modèles de maladies associés à la mutation C9orf72. Dans les échantillons de selles des patients, l'équipe a trouvé ces formes de glycogène plus fréquemment dans la SLA et la démence fronto-temporale liée au gène C9orf72 que chez les témoins sains, et la dégradation enzymatique du glycogène dans l'intestin a amélioré les résultats chez les souris.
Des chercheurs de l'Université Case Western Reserve ont rapporté des preuves que certaines bactéries intestinales peuvent produire des formes inflammatoires de glycogène — un glucide parfois décrit comme un « sucre » — qui peut provoquer des réponses immunitaires pertinentes pour la sclérose latérale amyotrophique (SLA) et la démence fronto-temporale (DFT), en particulier dans les contextes impliquant le gène C9orf72.
L'étude, publiée dans Cell Reports, s'est concentrée sur la façon dont les produits microbiens dans l'intestin interagissent avec le système immunitaire dans le contexte de C9orf72, un gène dont l'expansion de répétitions est la cause génétique connue la plus fréquente de la SLA et de la DFT. Dans une étude sur des échantillons fécaux humains décrite dans l'article, des formes inflammatoires de glycogène ont été détectées chez 15 des 22 échantillons de SLA et dans 1 échantillon sur 1 provenant d'un patient atteint de DFT associée au gène C9orf72, contre 4 sur 12 témoins sains.
Aaron Burberry, professeur adjoint au département de pathologie de la Case Western Reserve School of Medicine et auteur correspondant des travaux, a déclaré que l'équipe a découvert que « les bactéries intestinales nocives produisent des formes inflammatoires de glycogène (un type de sucre), et que ces sucres bactériens déclenchent des réponses immunitaires qui endommagent le cerveau ».
Lors d'expériences utilisant des souris axéniques (sans germes), les chercheurs ont rapporté que la colonisation d'animaux déficients en C9orf72 par une souche bactérienne productrice de glycogène (incluant Parabacteroides merdae dans leur modèle) accentuait les changements immunitaires systémiques et les signes d'implication du système nerveux central, notamment la rupture de la barrière hémato-encéphalique et l'infiltration de cellules immunitaires. Ils ont également rapporté que la digestion enzymatique du glycogène dans l'intestin atténuait la réactivité microgliale dans le cerveau et améliorait la survie chez les souris déficientes en C9orf72.
Alex Rodriguez-Palacios, professeur adjoint au Digestive Health Research Institute de la School of Medicine et co-auteur, a déclaré que l'équipe a réussi à réduire le glycogène nocif lors d'expériences, ce qui a « amélioré la santé cérébrale et prolongé la durée de vie », selon le résumé des conclusions de l'université.
Les chercheurs soutiennent que ces travaux offrent une explication potentielle à la raison pour laquelle seules certaines personnes génétiquement à risque développent la SLA ou la DFT : l'activité microbienne dans l'intestin peut servir de facteur environnemental influençant les voies inflammatoires liées à la maladie. Ils ont indiqué que les résultats pointent vers des stratégies thérapeutiques possibles, notamment des approches visant à décomposer le glycogène inflammatoire dans le tube digestif ou à cibler les mécanismes qui connectent les microbes intestinaux à l'activité immunitaire affectant le système nerveux.
Burberry a déclaré que le groupe prévoit des études plus vastes sur le microbiome des patients et que des essais cliniques testant si la dégradation du glycogène pourrait ralentir la progression de la SLA/DFT « pourraient commencer dans un an », selon le communiqué de l'université.