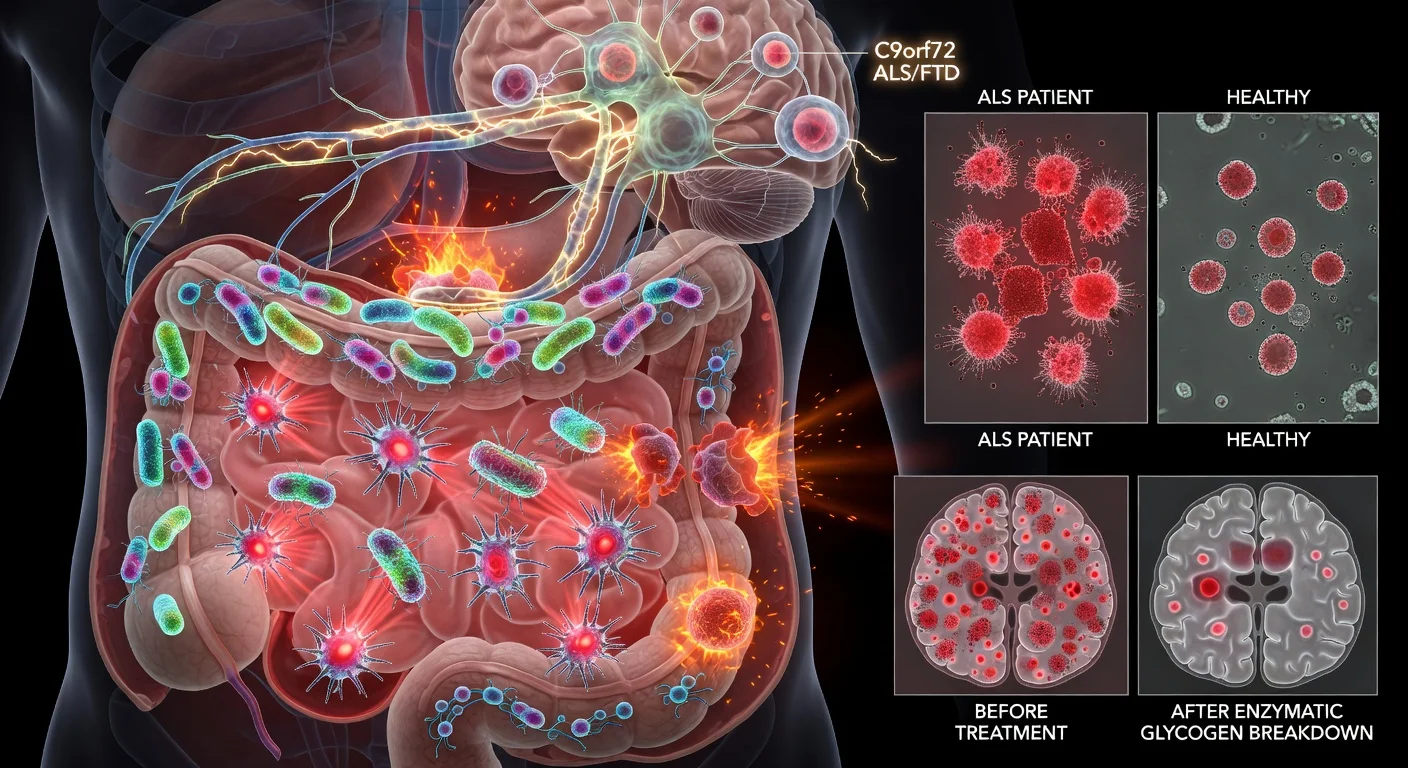
Pesquisadores da Case Western Reserve University relatam que algumas bactérias intestinais podem produzir formas de glicogênio incomumente inflamatórias e que esse glicogênio microbiano pode desencadear atividade imunológica ligada à inflamação cerebral em modelos de doenças vinculados à mutação C9orf72. Em amostras de fezes de pacientes, a equipe encontrou essas formas de glicogênio com mais frequência na ELA e na demência frontotemporal relacionada ao C9orf72 do que em controles saudáveis, e a decomposição enzimática do glicogênio no intestino melhorou os resultados em camundongos.
Pesquisadores da Case Western Reserve University relataram evidências de que certas bactérias intestinais podem produzir formas inflamatórias de glicogênio — um carboidrato por vezes descrito como um "açúcar" — que podem provocar respostas imunes relevantes para a esclerose lateral amiotrófica (ELA) e a demência frontotemporal (DFT), particularmente em contextos envolvendo o gene C9orf72.
O estudo, publicado na Cell Reports, concentrou-se em como os produtos microbianos no intestino interagem com o sistema imunológico no contexto do C9orf72, um gene no qual uma expansão de repetição é a causa genética conhecida mais comum de ELA e DFT. Em um levantamento de amostras fecais humanas descrito no artigo, formas inflamatórias de glicogênio foram detectadas em 15 de 22 amostras de ELA e em 1 de 1 amostra de um paciente com DFT associada ao C9orf72, em comparação com 4 de 12 controles saudáveis.
Aaron Burberry, professor assistente no Departamento de Patologia da Case Western Reserve School of Medicine e um dos autores correspondentes do trabalho, afirmou que a equipe descobriu que "bactérias intestinais nocivas produzem formas inflamatórias de glicogênio (um tipo de açúcar), e que esses açúcares bacterianos desencadeiam respostas imunes que danificam o cérebro".
Em experimentos usando camundongos livres de germes, os pesquisadores relataram que a colonização de animais com deficiência de C9orf72 com uma cepa bacteriana produtora de glicogênio (incluindo Parabacteroides merdae em seu modelo) intensificou as alterações imunológicas sistêmicas e sinais de envolvimento do sistema nervoso central, incluindo ruptura da barreira hematoencefálica e infiltração de células imunes. Eles também relataram que a digestão enzimática do glicogênio no intestino reduziu a reatividade da microglia no cérebro e melhorou a sobrevivência em camundongos com deficiência de C9orf72.
Alex Rodriguez-Palacios, professor assistente no Digestive Health Research Institute da School of Medicine e coautor, disse que a equipe conseguiu reduzir o glicogênio nocivo em experimentos de maneiras que "melhoraram a saúde cerebral e prolongaram a expectativa de vida", de acordo com o resumo das descobertas da universidade.
Os pesquisadores argumentam que o trabalho oferece uma explicação potencial para o motivo pelo qual apenas algumas pessoas geneticamente em risco desenvolvem ELA ou DFT: a atividade microbiana no intestino pode servir como um fator ambiental que influencia as vias inflamatórias ligadas à doença. Eles afirmaram que os resultados apontam para possíveis estratégias terapêuticas, incluindo abordagens destinadas a decompor o glicogênio inflamatório no trato digestivo ou direcionar mecanismos que conectam os micróbios intestinais à atividade imunológica que afeta o sistema nervoso.
Burberry disse que o grupo planeja estudos maiores dos microbiomas dos pacientes e afirmou que ensaios clínicos testando se a degradação do glicogênio poderia retardar a progressão da ELA/DFT "poderiam começar em um ano", de acordo com o comunicado da universidade.