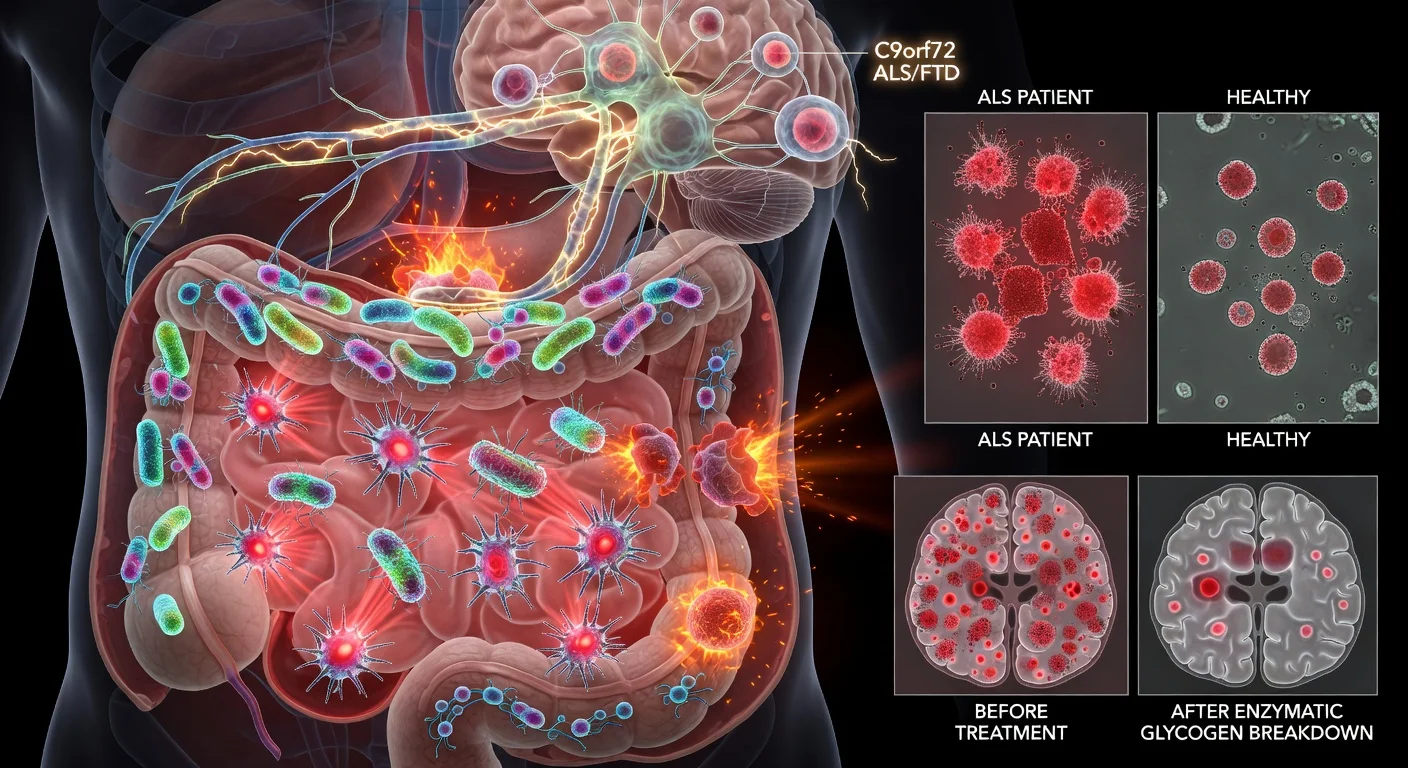
أفاد باحثون في جامعة كيس وسترن ريسرف بأن بعض بكتيريا الأمعاء يمكنها إنتاج أشكال من الجليكوجين تسبب التهابات غير عادية، وأن هذا الجليكوجين الميكروبي يمكنه تحفيز نشاط مناعي مرتبط بالتهاب الدماغ في نماذج مرضية مرتبطة بطفرة C9orf72. وفي عينات براز المرضى، وجد الفريق هذه الأشكال من الجليكوجين بنسبة أكبر في حالات التصلب الجانبي الضموري (ALS) والخرف الجبهي الصدغي المرتبط بـ C9orf72 مقارنة بالمجموعة الضابطة السليمة، كما أدى تكسير الجليكوجين إنزيمياً في الأمعاء إلى تحسين النتائج لدى الفئران.
أفاد باحثون في جامعة كيس وسترن ريسرف بوجود أدلة على أن بكتيريا معوية معينة يمكنها إنتاج أشكال التهابية من الجليكوجين - وهو كربوهيدرات توصف أحياناً بأنها "سكر" - يمكن أن تثير استجابات مناعية ذات صلة بمرض التصلب الجانبي الضموري (ALS) والخرف الجبهي الصدغي (FTD)، لا سيما في البيئات التي تتضمن جين C9orf72.
ركزت الدراسة، التي نُشرت في دورية Cell Reports، على كيفية تفاعل النواتج الميكروبية في الأمعاء مع الجهاز المناعي في سياق جين C9orf72، وهو جين يُعد تكرار توسعه السبب الجيني الأكثر شيوعاً المعروف للإصابة بمرض التصلب الجانبي الضموري والخرف الجبهي الصدغي. وفي مسح للعينات البرازية البشرية الموصوفة في الورقة البحثية، تم الكشف عن أشكال التهابية من الجليكوجين في 15 من أصل 22 عينة لمرضى التصلب الجانبي الضموري، وفي عينة واحدة من أصل عينة واحدة لمريض مصاب بالخرف الجبهي الصدغي المرتبط بـ C9orf72، مقارنة بـ 4 من أصل 12 عينة من المجموعة الضابطة السليمة.
وذكر آرون بوربيري، الأستاذ المساعد في قسم علم الأمراض بكلية الطب في جامعة كيس وسترن ريسرف والمؤلف المقابل للبحث، أن الفريق وجد أن "بكتيريا الأمعاء الضارة تنتج أشكالاً التهابية من الجليكوجين (نوع من السكر)، وأن هذه السكريات البكتيرية تحفز استجابات مناعية تضر بالدماغ".
وفي تجارب استخدمت فئراناً خالية من الجراثيم، أفاد الباحثون أن استعمار الحيوانات التي تعاني من نقص في جين C9orf72 بسلالة بكتيرية منتجة للجليكوجين (بما في ذلك بكتيريا Parabacteroides merdae في نموذجهم) أدى إلى تفاقم التغيرات المناعية الجهازية وعلامات إصابة الجهاز العصبي المركزي، بما في ذلك خلل في الحاجز الدموي الدماغي وتسلل الخلايا المناعية. كما ذكروا أن هضم الجليكوجين إنزيمياً في الأمعاء قلل من نشاط الخلايا الدبقية الصغيرة في الدماغ وحسن معدلات البقاء على قيد الحياة لدى الفئران التي تعاني من نقص في جين C9orf72.
وقال أليكس رودريغيز بالاسيوس، الأستاذ المساعد في معهد أبحاث صحة الجهاز الهضمي بكلية الطب والمؤلف المشارك، إن الفريق تمكن من تقليل الجليكوجين الضار في التجارب بطرق "حسنت صحة الدماغ وأطالت عمر" الفئران، وفقاً لملخص الجامعة للنتائج.
ويجادل الباحثون بأن هذا العمل يقدم تفسيراً محتملاً لسبب إصابة بعض الأشخاص المعرضين وراثياً فقط بمرض التصلب الجانبي الضموري أو الخرف الجبهي الصدغي: فقد يعمل النشاط الميكروبي في الأمعاء كعامل بيئي يؤثر على المسارات الالتهابية المرتبطة بالمرض. وأشاروا إلى أن النتائج تشير إلى استراتيجيات علاجية محتملة، بما في ذلك نهج تهدف إلى تكسير الجليكوجين الالتهابي في الجهاز الهضمي أو استهداف الآليات التي تربط ميكروبات الأمعاء بالنشاط المناعي الذي يؤثر على الجهاز العصبي.
وذكر بوربيري أن المجموعة تخطط لإجراء دراسات أوسع على ميكروبيوم المرضى، وأضاف أن التجارب السريرية التي تختبر ما إذا كان تحلل الجليكوجين يمكن أن يبطئ من تقدم مرض التصلب الجانبي الضموري/الخرف الجبهي الصدغي "قد تبدأ في غضون عام"، وذلك حسب البيان الصادر عن الجامعة.