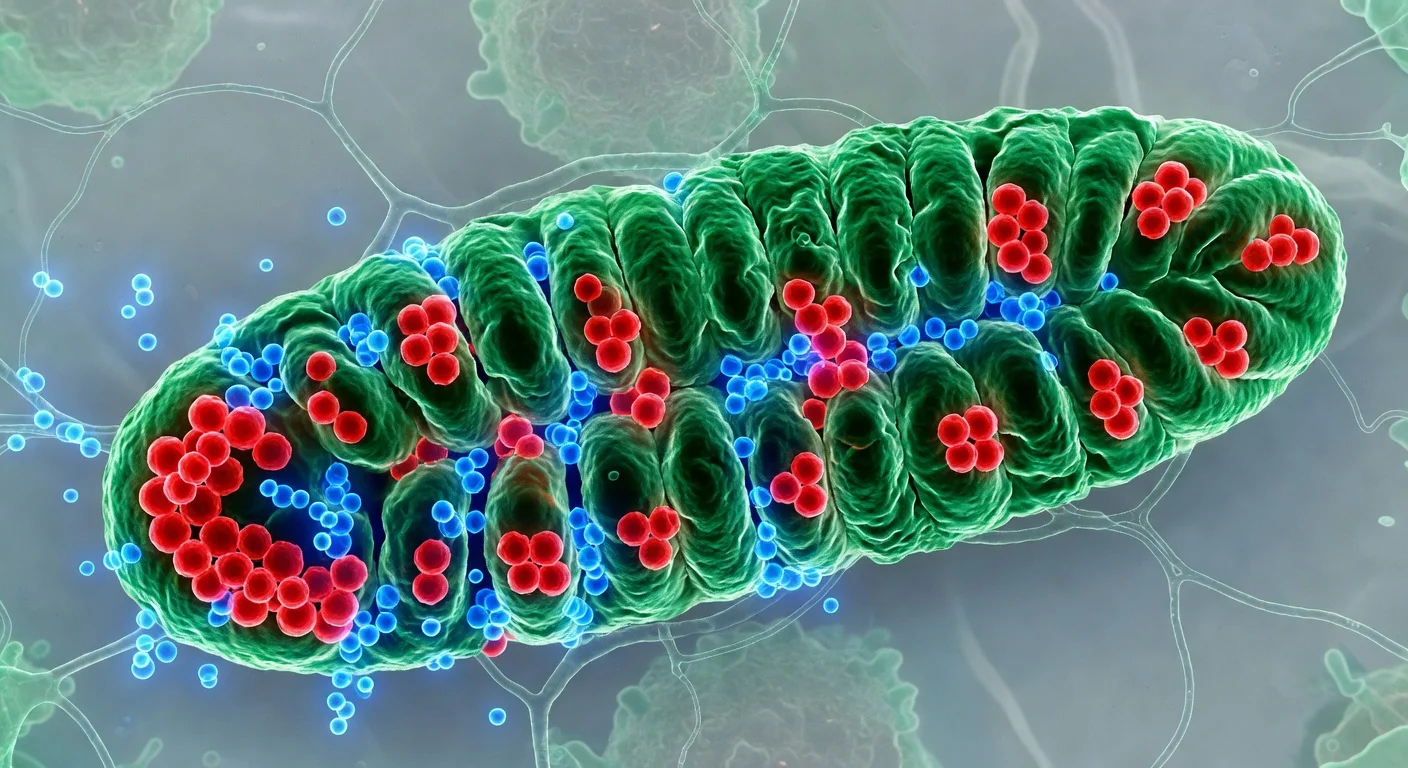
Des chercheurs de l'EPFL rapportent qu'un changement de forme transitoire des mitochondries, appelé « perlage » — où l'organite forme brièvement des constrictions semblables à des perles — peut redistribuer les amas d'ADN mitochondrial (ADNmt) en nucléoïdes plus régulièrement espacés. Ces travaux, publiés le 2 avril 2026 dans la revue Science, suggèrent que ce processus est déclenché par l'afflux de calcium dans les mitochondries et pourrait aider à expliquer comment les cellules maintiennent une organisation robuste de l'ADNmt, une caractéristique impliquée dans diverses maladies mitochondriales.
Les mitochondries, souvent décrites comme les centrales énergétiques de la cellule, possèdent leur propre matériel génétique : l'ADN mitochondrial (ADNmt). Les cellules contiennent généralement des centaines à des milliers de copies d'ADNmt, regroupées en amas appelés nucléoïdes.
Les scientifiques observent depuis longtemps que ces nucléoïdes sont régulièrement espacés au sein des mitochondries, une configuration censée favoriser une transmission fiable de l'ADNmt lors de la division cellulaire et une expression génique plus uniforme le long de l'organite.
Dans une étude dirigée par Suliana Manley, du Laboratoire de biophysique expérimentale de l'EPFL, les chercheurs soutiennent que les explications couramment avancées — telles que la fusion, la fission ou l'ancrage moléculaire mitochondrial — ne permettent pas d'expliquer pleinement la persistance de cet espacement, notamment lorsque ces mécanismes sont perturbés.
Pour étudier comment cet espacement est maintenu, l'équipe a combiné l'imagerie par super-résolution, la microscopie corrélative lumière-électrons et la microscopie à contraste de phase afin de suivre les changements de forme des mitochondries et les nucléoïdes individuels dans des cellules vivantes.
Les chercheurs rapportent que les mitochondries peuvent subir des épisodes de « perlage » quelques fois par minute, formant temporairement une série de constrictions régulièrement espacées ressemblant à un collier de perles. L'espacement entre ces constrictions correspond étroitement aux distances habituelles entre les nucléoïdes. Pendant le perlage, les chercheurs ont observé des amas de nucléoïdes plus larges se diviser en unités plus petites occupant les « perles » voisines, et après que la mitochondrie a retrouvé une forme tubulaire, les nucléoïdes redistribués ont pu rester séparés.
En utilisant des approches génétiques et pharmacologiques, l'étude lie le perlage à l'entrée de calcium dans les mitochondries et rapporte que l'organisation interne de la membrane aide à maintenir la séparation des nucléoïdes. Lorsque ces éléments régulateurs ont été perturbés, les chercheurs ont observé que les nucléoïdes tendaient à s'agglutiner en amas plutôt que de rester uniformément répartis.
Juan Landoni, chercheur postdoctoral ayant participé aux travaux, précise que ce phénomène remonte à plus d'un siècle, notant que la biologiste cellulaire Margaret Reed Lewis avait esquissé le perlage mitochondrial dès 1915. Selon l'équipe, le perlage a longtemps été considéré comme une curiosité associée au stress cellulaire, mais leurs conclusions soutiennent un rôle plus large de ce processus dans l'organisation de l'ADNmt.
Les auteurs soutiennent que ces résultats soulignent comment les changements de forme physique peuvent agir de concert avec la machinerie moléculaire pour organiser les composants cellulaires. Le résumé de recherche de l'EPFL note que le dysfonctionnement des mitochondries et de l'ADNmt est associé à des troubles métaboliques et neurologiques — notamment des conditions telles que l'insuffisance hépatique et l'encéphalopathie — et est également lié, dans la littérature scientifique, à des maladies neurodégénératives liées à l'âge comme la maladie d'Alzheimer et la maladie de Parkinson, bien que l'étude elle-même se concentre sur les mécanismes d'organisation de l'ADNmt plutôt que sur la démonstration d'un rôle causal direct du perlage dans ces pathologies.