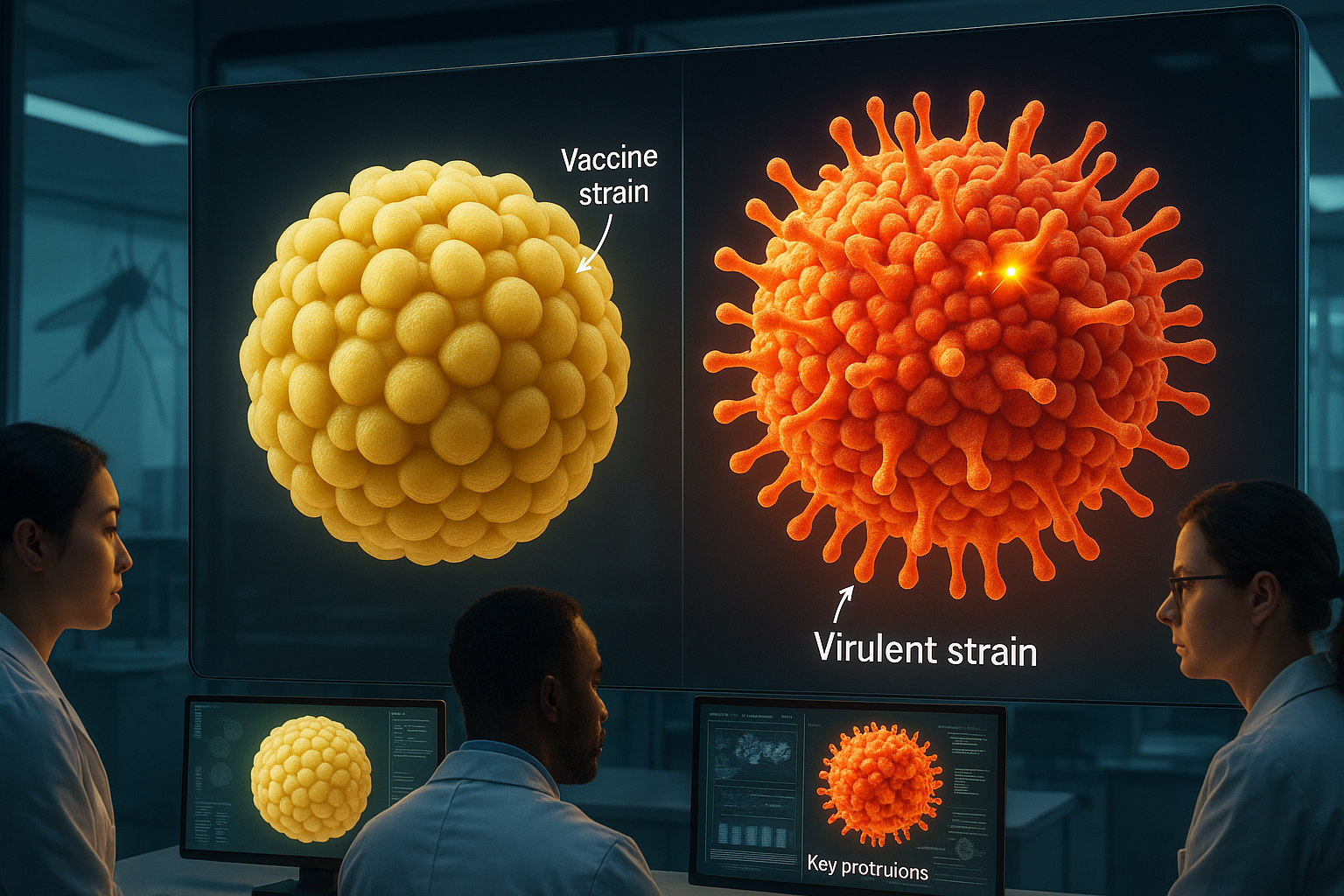
Cientistas da University of Queensland capturaram as primeiras imagens 3D de resolução quase atômica e alta resolução do vírus da febre amarela, detalhando como a superfície da cepa de vacina usada há muito tempo difere das cepas virulentas causadoras de doenças. O trabalho lança luz sobre como o vírus é reconhecido pelo sistema imunológico e pode apoiar vacinas aprimoradas para febre amarela e doenças relacionadas transmitidas por mosquitos.
O vírus da febre amarela (YFV) é uma infecção transmitida por mosquitos que pode danificar gravemente o fígado e é potencialmente fatal em casos graves. Pesquisadores da University of Queensland (UQ) agora produziram o que descrevem como a primeira estrutura tridimensional completa de uma partícula YFV totalmente madura em resolução quase atômica, usando microscopia crioeletrônica.
Para estudar o vírus com segurança, a equipe usou a plataforma do vírus Binjari, na qual os genes estruturais da febre amarela são combinados com o esqueleto de um vírus inofensivo. Essa abordagem permitiu imagens detalhadas enquanto evitava os riscos de manipular febre amarela totalmente patogênica. Como explicou a Dra. Summa Bibby da School of Chemistry and Molecular Bioscience da UQ em um comunicado divulgado pela UQ e relatado pela ScienceDaily, "Ao utilizar a plataforma do vírus Binjari bem estabelecida desenvolvida aqui na UQ, combinamos os genes estruturais da febre amarela com o esqueleto do vírus Binjari inofensivo e produzimos partículas virais que pudessem ser examinadas com segurança em um microscópio crioeletrônico."
As imagens de cryo-EM revelaram diferenças marcadas na superfície externa de diferentes cepas de YFV. De acordo com o comunicado de imprensa da UQ e cobertura de veículos como Phys.org e ScienceDaily, a cepa de vacina YFV-17D forma partículas com uma camada superficial lisa e estável, enquanto cepas virulentas causadoras de doenças mostram uma textura visivelmente irregular e ondulada.
Essas variações estruturais alteram como o sistema imunológico do corpo reconhece o vírus. "A superfície mais irregular e ondulada das cepas virulentas expõe partes do vírus que normalmente estão ocultas, permitindo que certos anticorpos se liguem mais facilmente," disse a Dra. Bibby. "As partículas de vacina lisas mantêm essas regiões cobertas, tornando-as mais difíceis de alcançar por anticorpos específicos."
A febre amarela continua sendo uma grande preocupação de saúde pública em partes da América do Sul e da África, onde o vírus é transmitido por mosquitos. Sem tratamentos antivirais aprovados disponíveis, a vacinação é o principal meio de prevenção, de acordo com o resumo do trabalho da UQ.
O professor Daniel Watterson da UQ disse que os achados fornecem uma nova visão importante sobre a biologia da febre amarela e ajudam a explicar o desempenho contínuo da vacina de longa data. "A vacina contra febre amarela continua eficaz contra cepas modernas e ver o vírus em tal detalhe fino nos permite entender melhor por que a cepa de vacina se comporta como o faz," disse ele. "Agora podemos identificar as características estruturais que tornam a vacina atual segura e eficaz. Os achados podem até informar o design futuro de vacinas para vírus relacionados como dengue, Zika e West Nile."
A pesquisa, que se concentra em como um único resíduo de aminoácido na proteína de envelope do vírus pode alterar a arquitetura do virion e antigenicidade, foi publicada na revista Nature Communications.