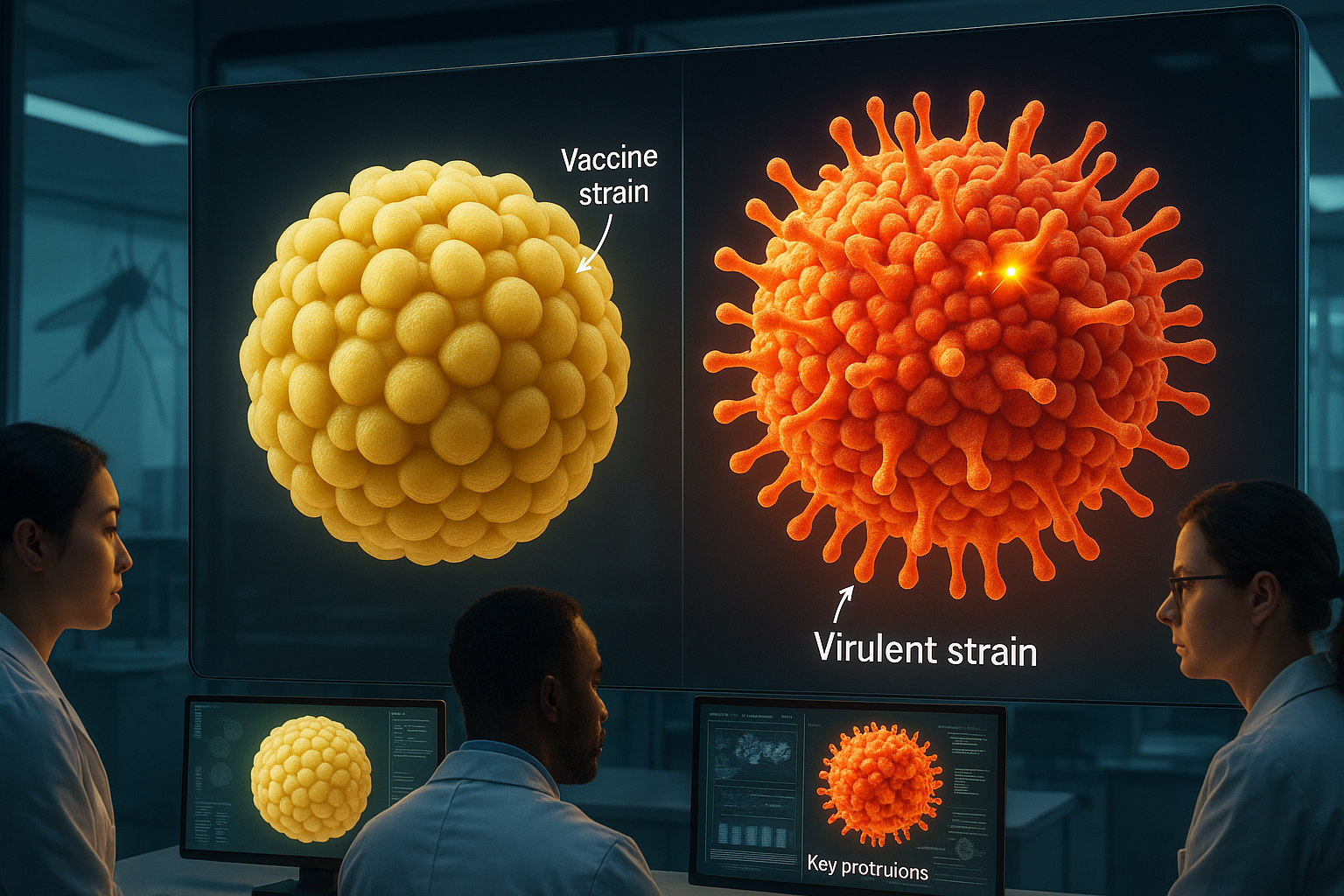
Des scientifiques de l’Université du Queensland ont capturé les premières images 3D quasi-atomiques à haute résolution du virus de la fièvre jaune, détaillant comment la surface de la souche vaccinale utilisée de longue date diffère des souches virulentes causant des maladies. Ce travail éclaire la manière dont le virus est reconnu par le système immunitaire et pourrait soutenir des vaccins améliorés pour la fièvre jaune et les maladies liées transmises par les moustiques.
Le virus de la fièvre jaune (YFV) est une infection transmise par les moustiques qui peut endommager gravement le foie et est potentiellement mortelle dans les cas graves. Des chercheurs de l’Université du Queensland (UQ) ont maintenant produit ce qu’ils décrivent comme la première structure tridimensionnelle complète d’une particule YFV totalement mature à résolution quasi-atomique, en utilisant la microscopie cryo-électronique.
Pour étudier le virus en toute sécurité, l’équipe a utilisé la plateforme du virus Binjari, dans laquelle les gènes structuraux de la fièvre jaune sont combinés avec le squelette d’un virus inoffensif. Cette approche a permis une imagerie détaillée tout en évitant les risques de manipulation de la fièvre jaune totalement pathogène. Comme l’a expliqué le Dr Summa Bibby de la School of Chemistry and Molecular Bioscience de l’UQ dans un communiqué publié par l’UQ et rapporté par ScienceDaily, « En utilisant la plateforme du virus Binjari bien établie développée ici à l’UQ, nous avons combiné les gènes structuraux de la fièvre jaune avec le squelette du virus Binjari inoffensif et produit des particules virales qui pouvaient être examinées en toute sécurité avec un microscope cryo-électronique. »
Les images cryo-EM ont révélé des différences marquées sur la surface externe des différentes souches de YFV. Selon le communiqué de presse de l’UQ et la couverture par des médias comme Phys.org et ScienceDaily, la souche vaccinale YFV-17D forme des particules avec une couche de surface lisse et stable, tandis que les souches virulentes causant des maladies montrent une texture visiblement bosselée et irrégulière.
Ces variations structurelles modifient la façon dont le système immunitaire du corps reconnaît le virus. « La surface plus bosselée et irrégulière des souches virulentes expose des parties du virus normalement cachées, permettant à certains anticorps de s’attacher plus facilement », a déclaré le Dr Bibby. « Les particules vaccinales lisses maintiennent ces régions couvertes, les rendant plus difficiles à atteindre pour certains anticorps. »
La fièvre jaune reste une préoccupation majeure de santé publique dans des parties de l’Amérique du Sud et de l’Afrique, où le virus est transmis par les moustiques. Sans traitements antiviraux approuvés disponibles, la vaccination est le principal moyen de prévention, selon le résumé du travail de l’UQ.
Le professeur Daniel Watterson de l’UQ a déclaré que ces découvertes fournissent un nouvel aperçu important de la biologie de la fièvre jaune et aident à expliquer les performances continues du vaccin de longue date. « Le vaccin contre la fièvre jaune reste efficace contre les souches modernes et voir le virus dans un tel détail fin nous permet de mieux comprendre pourquoi la souche vaccinale se comporte comme elle le fait », a-t-il dit. « Nous pouvons maintenant identifier les caractéristiques structurelles qui rendent le vaccin actuel sûr et efficace. Ces découvertes pourraient même informer la conception future de vaccins pour des virus apparentés comme la dengue, le Zika et le Nil occidental. »
La recherche, qui se concentre sur la manière dont un seul résidu d’acide aminé dans la protéine d’enveloppe du virus peut altérer l’architecture du virion et l’antigénicité, a été publiée dans la revue Nature Communications.