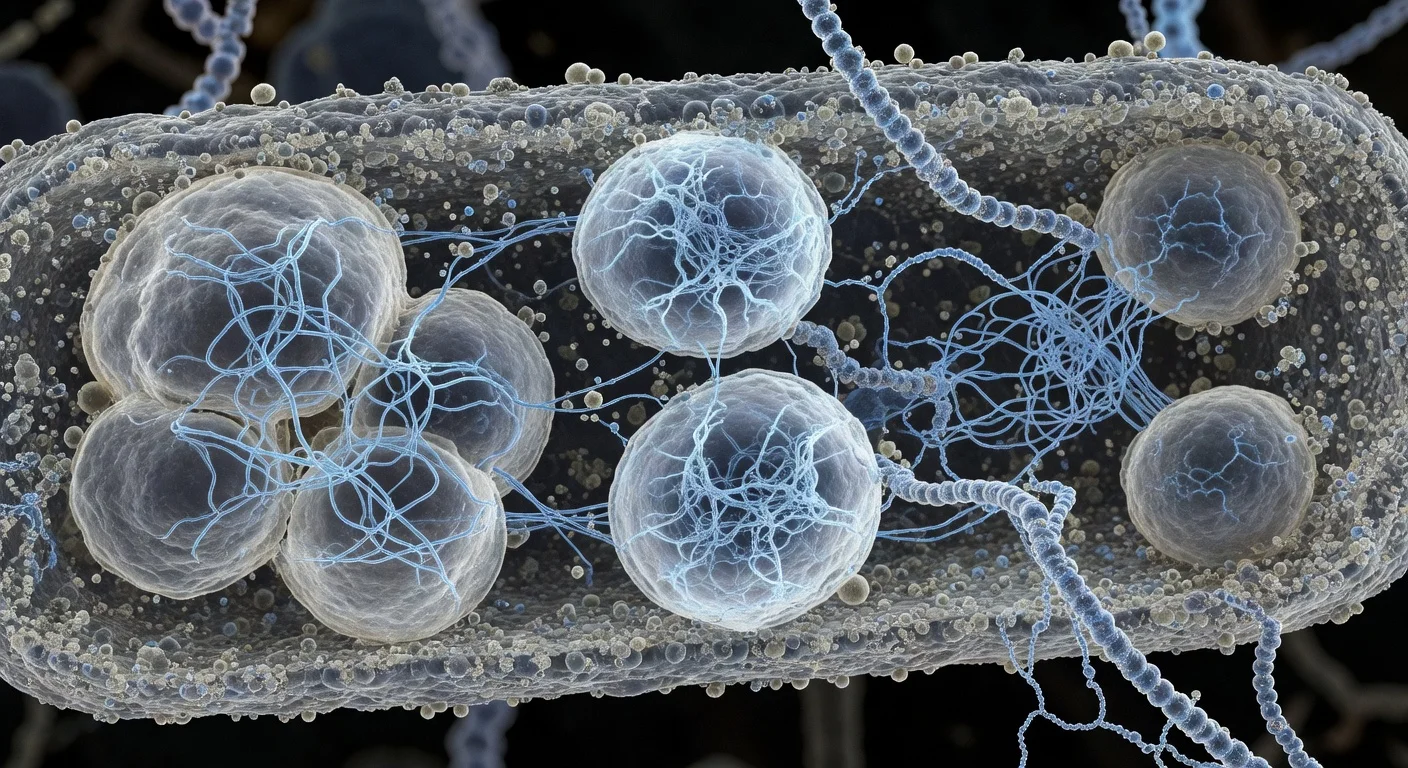
Tim yang dipimpin Universitas Otago, bekerja sama dengan kolaborator di Okinawa Institute of Science and Technology, telah menyelesaikan struktur 3D Bas63, bakteriofag yang menginfeksi E. coli. Diterbitkan di Science Advances (online pada 12 November 2025; edisi bertanggal 14 November 2025), karya ini merinci fitur ekor langka dan dapat memberi informasi untuk desain fage rasional untuk penggunaan medis, pertanian, dan industri.
Para peneliti telah menghasilkan peta struktural mendalam dari fage Escherichia JohannRWettstein (Bas63), menerangi bagaimana aparatus ekornya berinteraksi dengan bakteri dan bagaimana virus terkait mungkin telah berevolusi. Studi ini muncul di Science Advances (DOI: 10.1126/sciadv.adx0790) dan mencantumkan penulis dari Universitas Otago dan Okinawa Institute of Science and Technology (OIST). Catatan publikasi menunjukkan rilis online pada 12 November 2025 dan tanggal edisi 14 November 2025. (pubmed.ncbi.nlm.nih.gov)
Penulis utama Dr. James Hodgkinson‑Bean menggambarkan bakteriofag sebagai alternatif “sangat menarik” untuk antibiotik, mencatat bahwa “virus bakteriofag tidak berbahaya bagi semua kehidupan multiseluler dan mampu menargetkan dan membunuh bakteri target secara sangat selektif,” yang merupakan alasan mengapa mereka semakin dipelajari untuk terapi fage terhadap infeksi tahan obat. Komentar tersebut diterbitkan oleh Universitas Otago dan dibawa oleh ScienceDaily. (otago.ac.nz)
Menggunakan mikroskopi krioelektron, tim merekonstruksi Bas63 pada skala molekuler, mengidentifikasi koneksi kumis-dan-kerah langka antara kepala dan ekor, protein dekorasi di pusat heksamer pada kapsid, dan serat ekor ganda yang beragam—fitur yang membantu menjelaskan bagaimana virus mengenali dan menyerang inang bakterinya. Rilis berita OIST dan abstrak makalah menyoroti elemen-elemen ini, termasuk protein dekorasi β-tulip dan mirip Hoc, serta serat ekor panjang yang menyerupai yang ada di fage T4. (oist.jp)
Penulis senior Associate Professor Mihnea Bostina mengatakan bahwa “cetak biru rinci dari bakteriofag” dapat memajukan desain rasional untuk aplikasi mulai dari pengobatan infeksi hingga memerangi biofilm dalam pengolahan makanan dan sistem air, komentar yang diulang dalam pengumuman newsroom Otago. Peneliti juga membingkai karya ini di tengah meningkatnya resistensi antibiotik dan ancaman terhadap keamanan pangan global dari patogen tanaman. (otago.ac.nz)
Penulis lebih lanjut berargumen bahwa perbandingan struktural mengungkapkan hubungan evolusi yang jauh, termasuk hubungan antara bakteriofag dan virus herpes yang mungkin berasal dari miliaran tahun—sebuah perspektif yang diungkapkan oleh Hodgkinson‑Bean dalam rilis universitas. Artikel jurnal yang mendasarinya fokus pada konservasi struktural dalam genus Felixounavirus dan tidak menentukan tanggal hubungan tersebut, sehingga karakterisasi skala waktu disajikan di sini sebagai interpretasi peneliti. (otago.ac.nz)
Ini adalah struktur fage lengkap kedua dari kelompok ini pada 2025: pada April, anggota dari tim Otago–OIST yang sama melaporkan arsitektur tingkat atom dari fage φTE yang menargetkan patogen kentang di Nature Communications, karya yang mereka katakan menyediakan template untuk merancang agen pengendalian hayati dalam pertanian. (pmc.ncbi.nlm.nih.gov)