Ett team ledd av University of Otago, med samarbetspartners vid Okinawa Institute of Science and Technology, har löst 3D-strukturen av Bas63, en bakteriofag som infekterar E. coli. Publicerat i Science Advances (online den 12 november 2025; nummer daterat 14 november 2025), beskriver arbetet sällsynta svansdrag och kan informera rationell fagdesign för medicinska, jordbruks- och industriella användningar.
Forskare har producerat en djupgående strukturell karta av Escherichia-fagen JohannRWettstein (Bas63), som belyser hur dess svansapparat engagerar bakterier och hur relaterade virus kan ha utvecklats. Studien publiceras i Science Advances (DOI: 10.1126/sciadv.adx0790) och listar författare från University of Otago och Okinawa Institute of Science and Technology (OIST). Publiceringsregister visar en online-release den 12 november 2025 och ett nummerdatum den 14 november 2025. (pubmed.ncbi.nlm.nih.gov)
Huvudförfattaren Dr. James Hodgkinson‑Bean beskrev bakteriofager som ”extremt spännande” alternativ till antibiotika, och noterade att ”bakteriofagvirus är ofarliga för all flercellig liv och kan mycket selektivt rikta in sig på och döda en målbakterie”, vilket är varför de studeras alltmer för fagterapi mot läkemedelsresistenta infektioner. Dessa uttalanden publicerades av University of Otago och förmedlades av ScienceDaily. (otago.ac.nz)
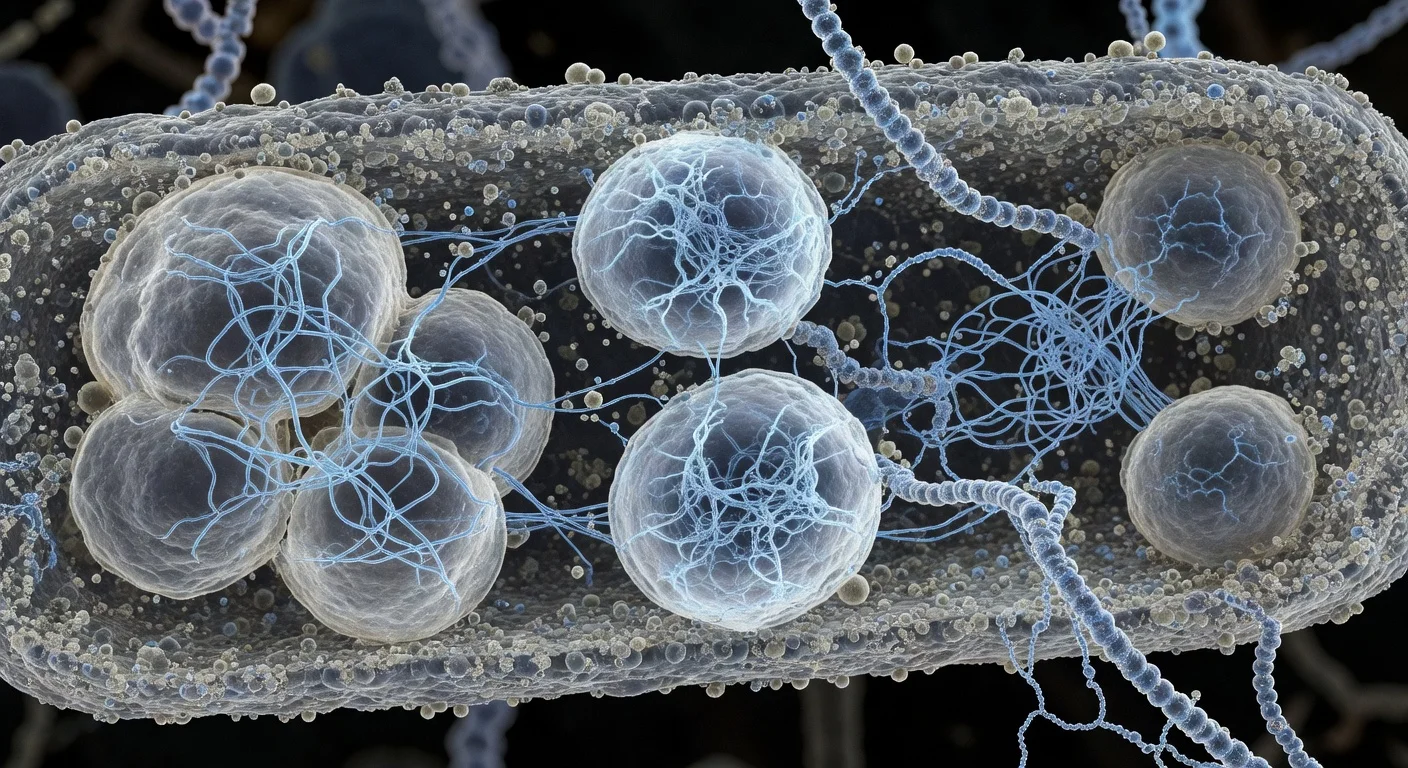
Med hjälp av kryo-elektronmikroskopi rekonstruerade teamet Bas63 i molekylär skala, och identifierade sällsynta polisong-och-krage-förbindelser mellan huvud och svans, dekorationsproteiner i hexamercentra på kapsiden, och flera, varierade svansfibrer—egenskaper som hjälper till att förklara hur viruset känner igen och attackerar sin bakteriella värd. OIST:s nyhetsmeddelande och artikelns sammanfattning framhäver dessa element, inklusive β-tulpan- och Hoc-liknande dekorationsproteiner, samt långa svansfibrer som liknar dem i fagen T4. (oist.jp)
Seniorförfattaren, docent Mihnea Bostina, sa att ”det detaljerade ritningen av en bakteriofag” kan främja rationell design för applikationer från behandling av infektioner till bekämpning av biofilmer i livsmedelsbearbetning och vattensystem, en kommentar som ekar i Otago:s nyhetsrummeddelande. Forskare ramar också in arbetet mitt i ökande antibiotikaresistens och hot mot global livsmedelssäkerhet från växtpatogener. (otago.ac.nz)
Författarna argumenterar vidare att strukturella jämförelser avslöjar avlägsna evolutionära länkar, inklusive relationer mellan bakteriofager och herpesvirus som kan spåras tillbaka miljarder år—ett perspektiv som Hodgkinson‑Bean artikulerade i universitetsmeddelandet. Den underliggande tidskriftsartikeln fokuserar på strukturell konservering inom släktet Felixounavirus och daterar inte dessa länkar, så tids skalans karakterisering presenteras här som forskarnas tolkning. (otago.ac.nz)
Detta är gruppens andra fullständiga fagstruktur 2025: i april rapporterade medlemmar i samma Otago–OIST-team den atomnivåarkitekturen av potatispatogen-målinriktad fagen φTE i Nature Communications, ett arbete som de säger ger en mall för att designa biocontrollmedel i jordbruket. (pmc.ncbi.nlm.nih.gov)