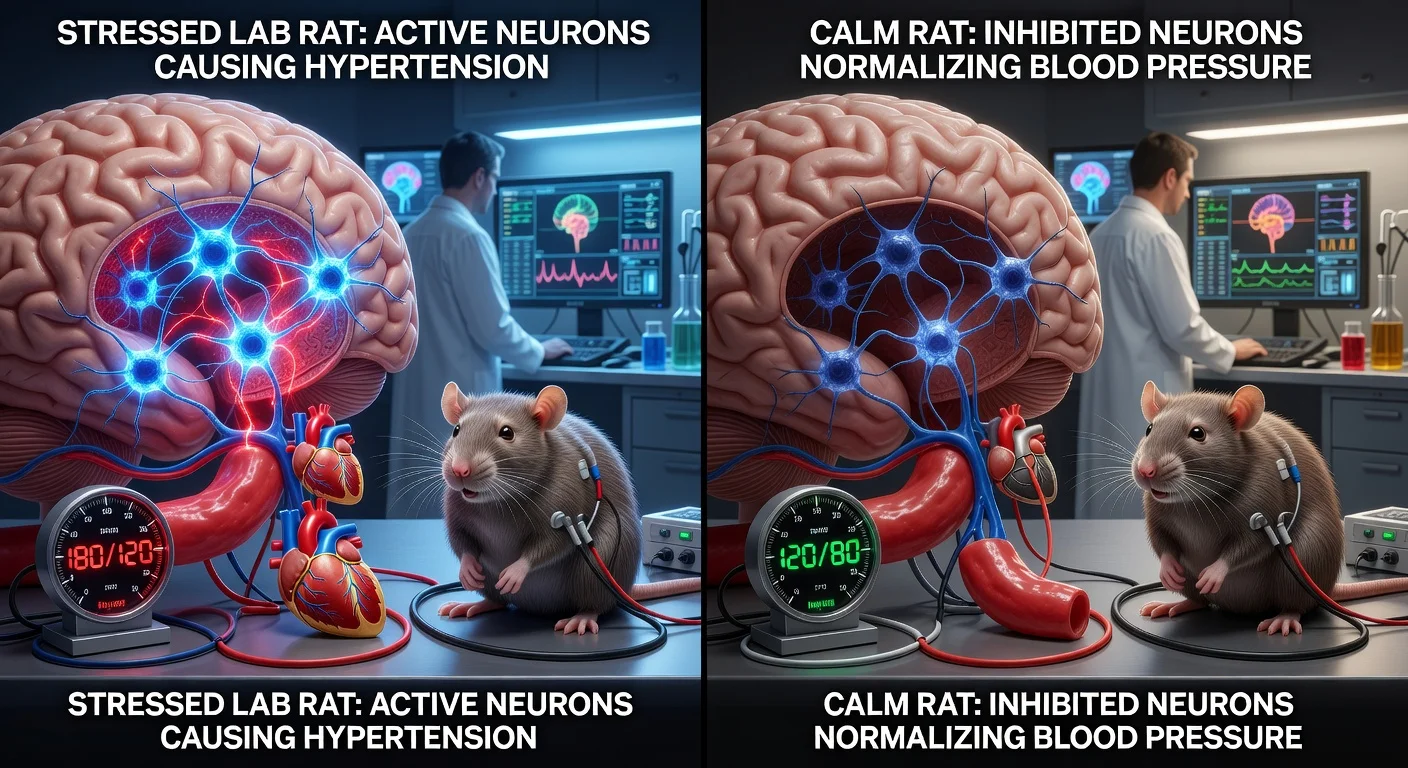
Para peneliti yang bekerja sama dengan University of Auckland dan University of São Paulo di Brasil melaporkan bahwa neuron di wilayah lateral parafacial (pFL) pada medula—yang dikenal karena perannya dalam mendorong embusan napas kuat—juga memperkuat aktivitas saraf simpatis dan dapat meningkatkan tekanan darah pada model hewan hipertensi neurogenik. Menghambat neuron-neuron ini menurunkan tekanan darah ke tingkat normal pada tikus hipertensi, sebagaimana temuan yang diterbitkan dalam Circulation Research.
Sebuah tim peneliti yang mencakup Profesor Julian Paton dari Manaaki Manawa – Centre for Heart Research di University of Auckland serta para kolaborator di Brasil telah melaporkan bukti bahwa wilayah kecil di batang otak yang terlibat dalam pernapasan mungkin berkontribusi terhadap tekanan darah tinggi pada model hewan.
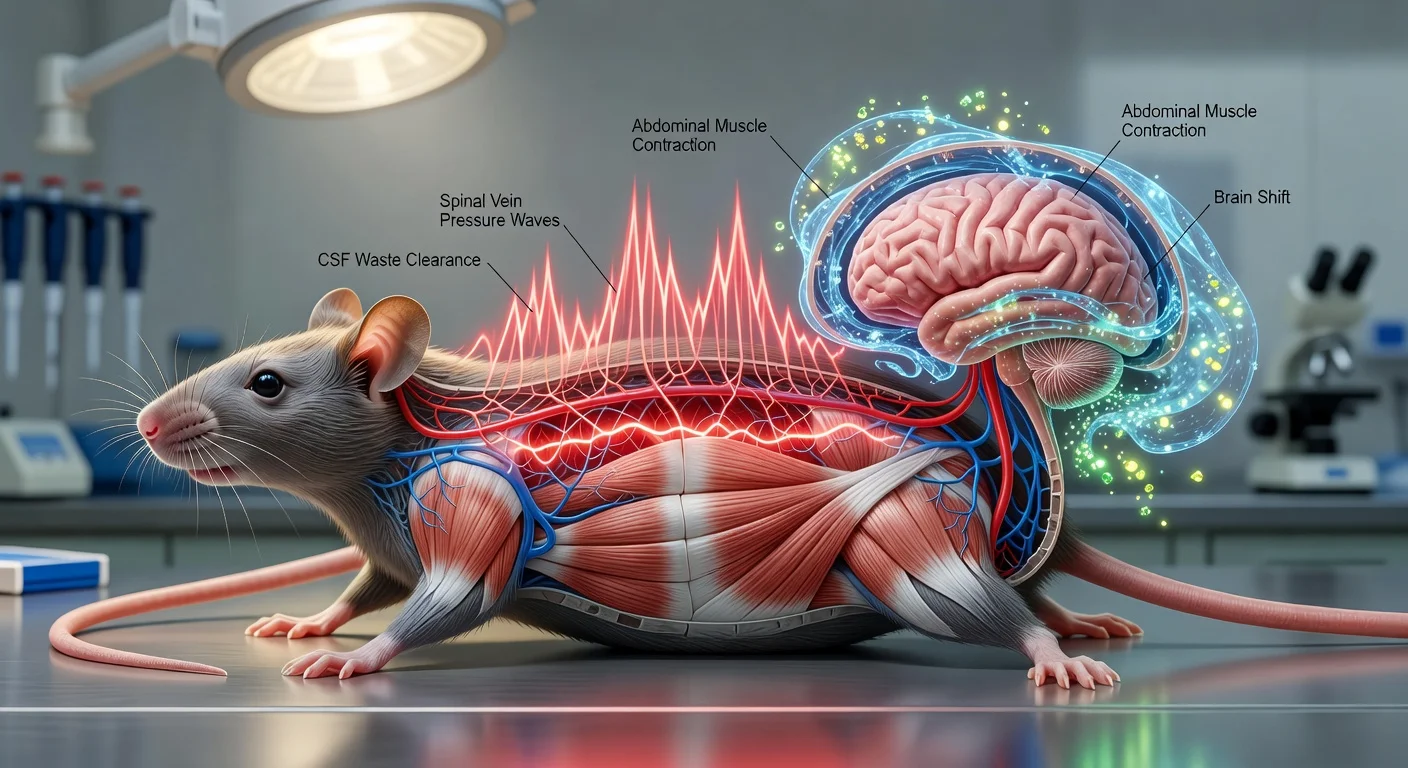
Menurut rilis University of Auckland, wilayah lateral parafacial di batang otak diaktifkan selama embusan napas kuat—seperti tertawa, batuk, atau berolahraga—yang menggunakan otot perut alih-alih mengandalkan pantulan elastis paru-paru. Paton mengatakan wilayah tersebut “diaktifkan” selama embusan napas “paksaan” ini.
Dalam makalah yang telah ditinjau oleh sejawat, para peneliti berfokus pada neuron di wilayah lateral parafacial (pFL) medula dan menguji bagaimana neuron tersebut memengaruhi jalur simpatis yang mengatur tonus pembuluh darah. Dalam eksperimen pada tikus, aktivasi optogenetik neuron pFL memicu ekspirasi aktif dan meningkatkan aktivitas simpatis selama ekspirasi, sehingga menaikkan tekanan arteri. Studi tersebut juga melaporkan bahwa neuron pFL memproyeksikan ke neuron presimpatis di medula ventrolateral rostral (RVLM) dan wilayah pontine A5; pada hewan hipertensi, transmisi sinaptik pada jalur pFL-ke-RVLM meningkat.
Untuk memodelkan hipertensi neurogenik, para peneliti menggunakan hipoksia intermiten kronis pada tikus. Mereka melaporkan bahwa penghambatan farmakogenetik neuron pFL menghilangkan eksitasi simpatis yang terkait dengan ekspirasi dan menormalkan tekanan arteri pada tikus hipertensi.
Rilis University of Auckland lebih lanjut berpendapat bahwa wilayah pFL dapat didorong oleh sinyal yang berasal dari luar otak—khususnya dari badan karotis, struktur sensor oksigen di dekat arteri karotis di leher. Berdasarkan hal itu, Paton mengatakan bahwa timnya bertujuan untuk mengurangi aktivitas badan karotis dengan obat yang dialihfungsikan guna meredam sirkuit batang otak secara “jarak jauh,” yang berpotensi menghindari penggunaan obat-obatan yang harus menembus otak.
Rilis tersebut juga menyarankan bahwa temuan ini mungkin relevan dengan tekanan darah tinggi yang terkait dengan apnea tidur, di mana aktivitas badan karotis dapat meningkat saat napas berhenti selama tidur. Para peneliti menekankan bahwa pekerjaan ini dilakukan pada hewan.
Studi ini berjudul “Lateral Parafacial Neurons Evoked Expiratory Oscillations Driving Neurogenic Hypertension,” yang diterbitkan daring pada 17 Desember 2025, dan tercantum dalam edisi 16 Januari 2026 Circulation Research (vol. 138, no. 2) dengan DOI: 10.1161/CIRCRESAHA.125.326674.