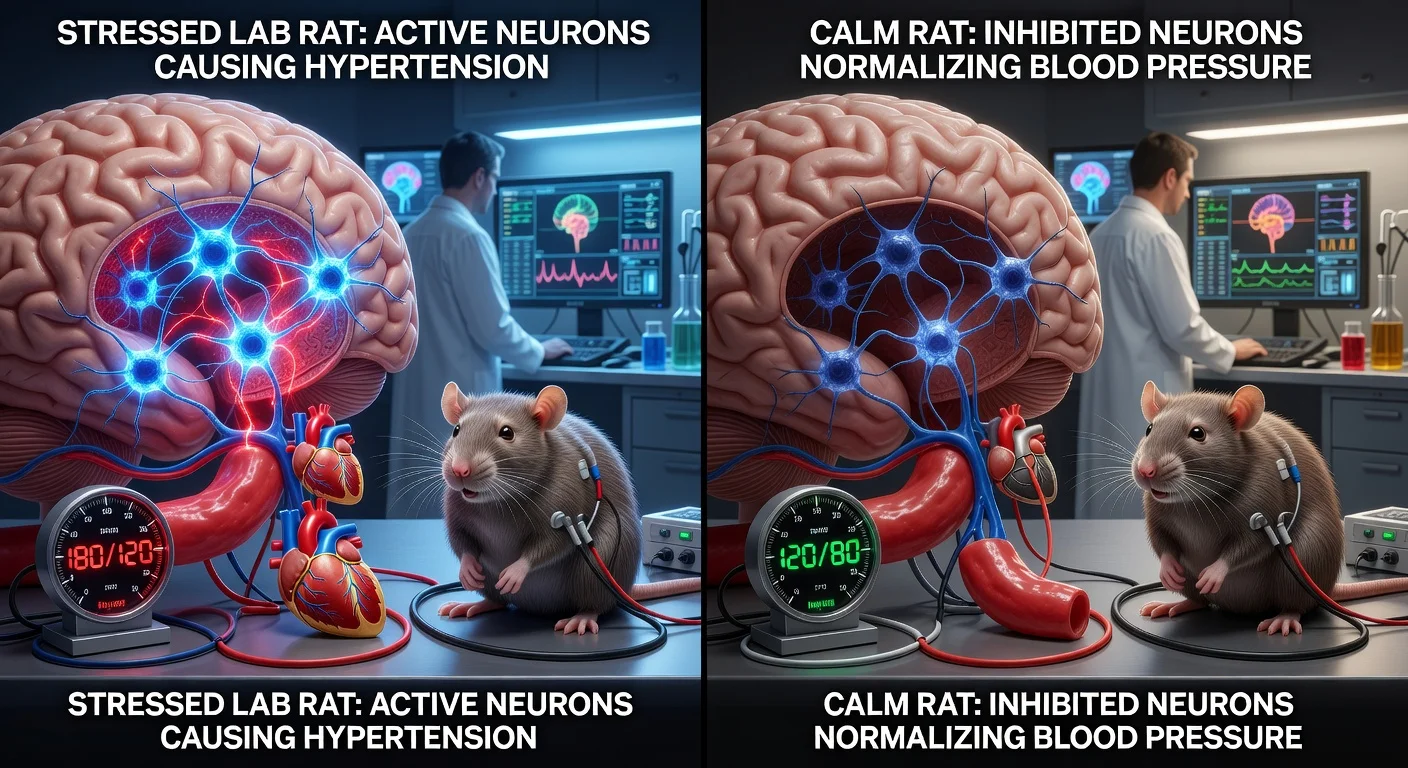
Investigadores que colaboran con la Universidad de Auckland y la Universidad de São Paulo en Brasil informan que las neuronas en la región parafacial lateral (pFL) del bulbo raquídeo —conocida principalmente por contribuir a la exhalación forzada— también amplifican la actividad del sistema nervioso simpático y pueden elevar la presión arterial en un modelo animal de hipertensión neurogénica. La inhibición de estas neuronas redujo la presión arterial a niveles normales en ratas hipertensas, según los hallazgos publicados en Circulation Research.
Un equipo de investigación que incluye al profesor Julian Paton, del Manaaki Manawa – Centre for Heart Research de la Universidad de Auckland, junto con colaboradores en Brasil, ha reportado evidencia de que una pequeña región del tronco encefálico involucrada en la respiración podría contribuir a la presión arterial alta en un modelo animal.
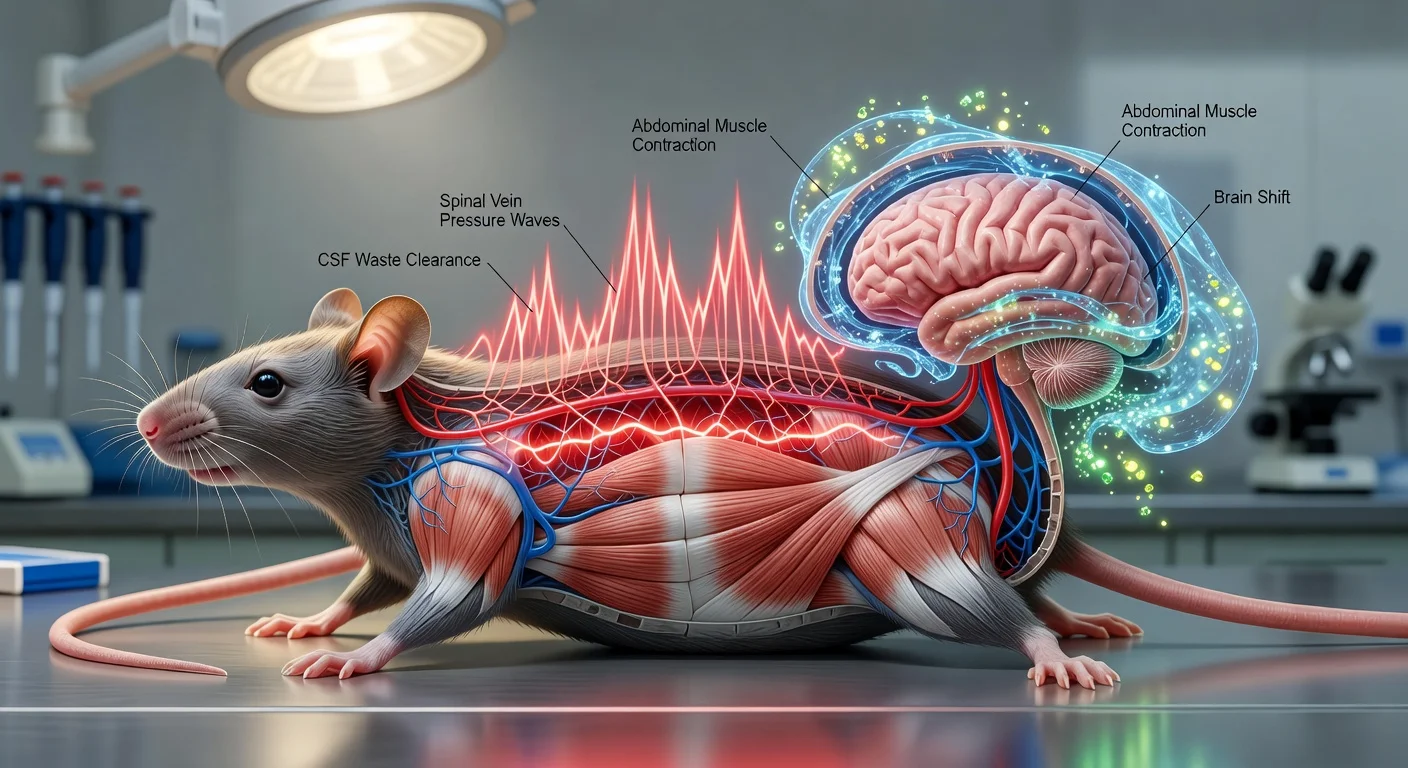
Según el comunicado de la Universidad de Auckland, la región parafacial lateral del tronco encefálico se activa durante las exhalaciones forzadas —como al reír, toser o hacer ejercicio—, las cuales utilizan los músculos abdominales en lugar de depender principalmente del retroceso elástico de los pulmones. Paton señaló que la región es «reclutada para entrar en acción» durante estas exhalaciones «forzadas».
En el artículo revisado por pares, los investigadores se centraron en las neuronas de la región parafacial lateral (pFL) del bulbo raquídeo y probaron cómo influyen en las vías simpáticas que regulan el tono de los vasos sanguíneos. En experimentos realizados con ratas, la activación optogenética de las neuronas pFL desencadenó una expiración activa y aumentó la actividad simpática durante la expiración, elevando la presión arterial. El estudio también informó que las neuronas pFL se proyectan hacia neuronas presimpáticas en la médula ventrolateral rostral (RVLM) y en la región pontina A5; en animales hipertensos, la transmisión sináptica en la vía pFL-a-RVLM se vio potenciada.
Para modelar la hipertensión neurogénica, los investigadores utilizaron hipoxia intermitente crónica en ratas. Informaron que la inhibición farmacogenética de las neuronas pFL eliminó la excitación simpática vinculada a la expiración y normalizó la presión arterial en las ratas hipertensas.
El comunicado de la Universidad de Auckland argumenta, además, que la región pFL puede ser activada por señales que se originan fuera del cerebro, específicamente desde los cuerpos carotídeos, estructuras sensoras de oxígeno situadas cerca de la arteria carótida en el cuello. Sobre esta base, Paton indicó que el grupo pretende reducir la actividad del cuerpo carotídeo con un fármaco reutilizado para atenuar el circuito del tronco encefálico de forma «remota», evitando potencialmente medicamentos que deban penetrar en el cerebro.
El comunicado también sugiere que los hallazgos podrían ser relevantes para la presión arterial alta asociada a la apnea del sueño, donde la actividad del cuerpo carotídeo puede aumentar cuando la respiración se detiene durante el sueño. Los investigadores enfatizaron que el trabajo se llevó a cabo en animales.
El estudio se titula "Lateral Parafacial Neurons Evoked Expiratory Oscillations Driving Neurogenic Hypertension", publicado en línea el 17 de diciembre de 2025 e incluido en el número del 16 de enero de 2026 de Circulation Research (vol. 138, n.º 2) con el DOI: 10.1161/CIRCRESAHA.125.326674.