Investigadores del Cold Spring Harbor Laboratory informan que las células de soporte conocidas como fibroblastos asociados al cáncer miofibroblásticos (myCAFs) pueden reclutar fibras nerviosas simpáticas en lesiones pancreáticas tempranas, creando un bucle de retroalimentación que puede ayudar al cáncer pancreático a establecerse antes de que se formen tumores completos. En experimentos con ratones, interrumpir la actividad nerviosa simpática redujo la activación de los fibroblastos y se asoció con una reducción de casi el 50% en el crecimiento tumoral.
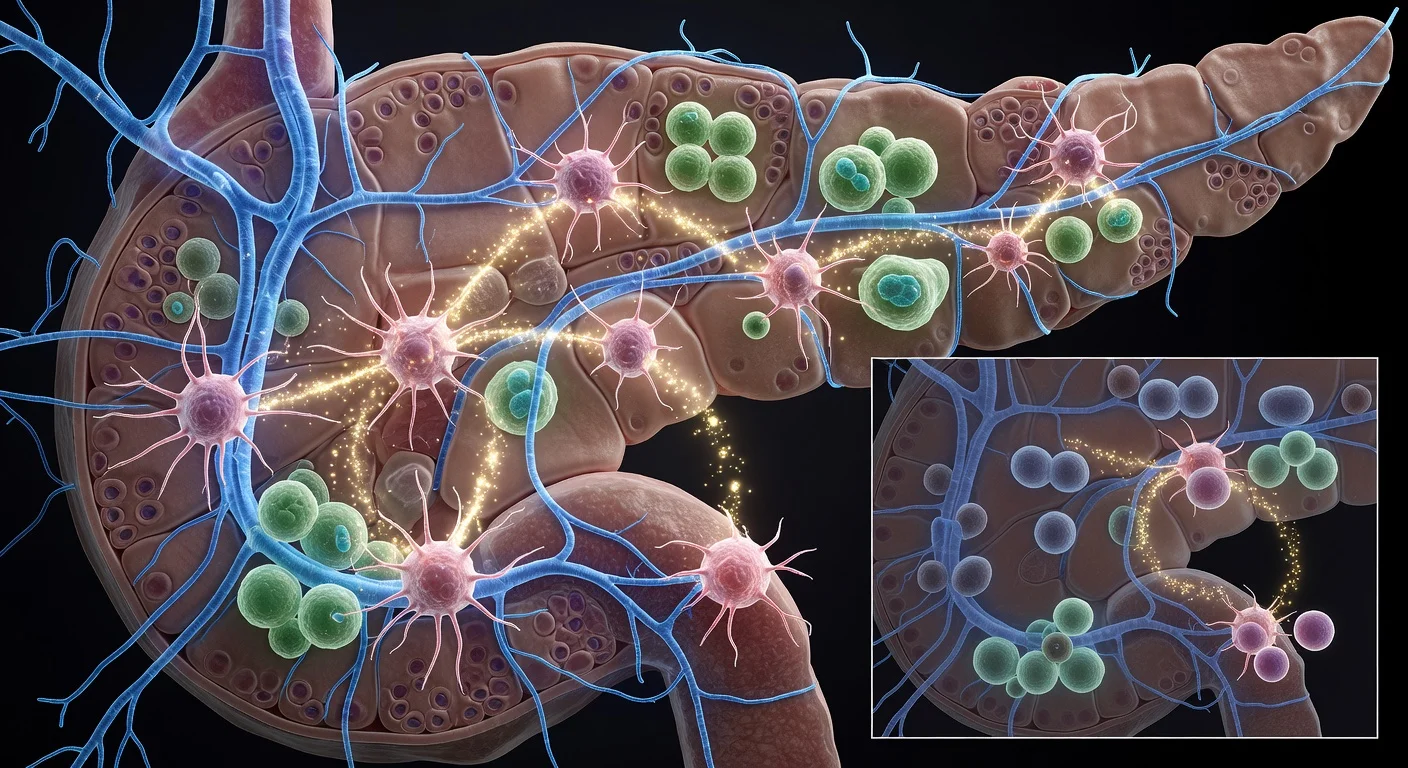
El cáncer de páncreas es difícil de detectar en etapas tempranas y a menudo responde mal a los tratamientos estándar, factores que han impulsado a los científicos a buscar nuevas formas de ralentizar la enfermedad antes de que progrese. nnUn equipo del Cold Spring Harbor Laboratory (CSHL), liderado por el investigador postdoctoral Jérémy Nigri en el laboratorio del profesor David Tuveson, se centró en cómo el sistema nervioso puede influir en las etapas más tempranas del cáncer de páncreas. Nigri señaló que los investigadores han reconocido desde hace tiempo la invasión perineural —un proceso en el que las células cancerosas se extienden a lo largo de los nervios— como una forma en que los tumores pancreáticos pueden diseminarse. nn## Los nervios están presentes antes de que los tumores se formen completamente nnEn el nuevo trabajo, los investigadores informan evidencia de que los nervios pueden desempeñar un papel activo incluso antes que la invasión perineural, apareciendo en y alrededor de lesiones pancreáticas precancerosas. nnUtilizando inmunofluorescencia de montaje completo para generar imágenes tridimensionales, el equipo observó redes nerviosas densas entretejidas a través de las lesiones pancreáticas y estrechamente asociadas con fibroblastos promotores de tumores conocidos como myCAFs. En vistas bidimensionales convencionales, las mismas estructuras nerviosas pueden aparecer como pequeñas puntuaciones dispersas. nn> «Cuando vimos esta imagen por primera vez, me quedé impactado», dijo Nigri. «Ni siquiera podía imaginar la lesión así. Solo la había visto en 2D». nn## Un bucle de retroalimentación propuesto que involucra nervios simpáticos nnBasados en experimentos con ratones y sistemas de células humanas, los investigadores describen un ciclo en el que los myCAFs emiten señales que atraen fibras del sistema nervioso simpático, que regula la respuesta de lucha o huida del cuerpo. Esas fibras nerviosas liberan norepinefrina, y el estudio informa que la norepinefrina puede unirse a los fibroblastos y desencadenar un aumento en el calcio intracelular. El aumento resultante de calcio activa aún más los myCAFs, una respuesta que los investigadores dicen que puede promover el crecimiento precanceroso mientras atrae fibras nerviosas adicionales, reforzando el bucle. nn## Interrumpir la actividad nerviosa redujo el crecimiento tumoral en ratones nnPara probar si interrumpir esta señalización podía ralentizar la enfermedad, el equipo utilizó una neurotoxina en un experimento con ratones para desactivar la actividad del sistema nervioso simpático. Informaron una activación reducida de fibroblastos y una reducción de casi el 50% en el crecimiento tumoral. nn> «En un experimento, utilizamos una neurotoxina para desactivar el sistema nervioso simpático», dijo Nigri. «Mostramos una activación reducida de fibroblastos y una reducción de casi el 50% en el crecimiento tumoral». nn## Implicaciones para el tratamiento y próximos pasos nnLos hallazgos se publicaron en Cancer Discovery, una revista de la American Association for Cancer Research. Los investigadores sugieren que, dado que la interacción nervio-myCAF aparece temprano, puede representar un objetivo terapéutico potencial. También señalan fármacos clínicamente disponibles, incluidos doxazosin, como candidatos para explorar en combinación con enfoques establecidos como la quimioterapia o la inmunoterapia. nn> «El siguiente paso será estudiar esto con más detalle e intentar encontrar una forma de bloquear la interacción entre fibroblastos y nervios», dijo Nigri. nnEl CSHL dijo que el trabajo fue apoyado por múltiples financiadores, incluida la Lustgarten Foundation y la Pancreatic Cancer Action Network. n