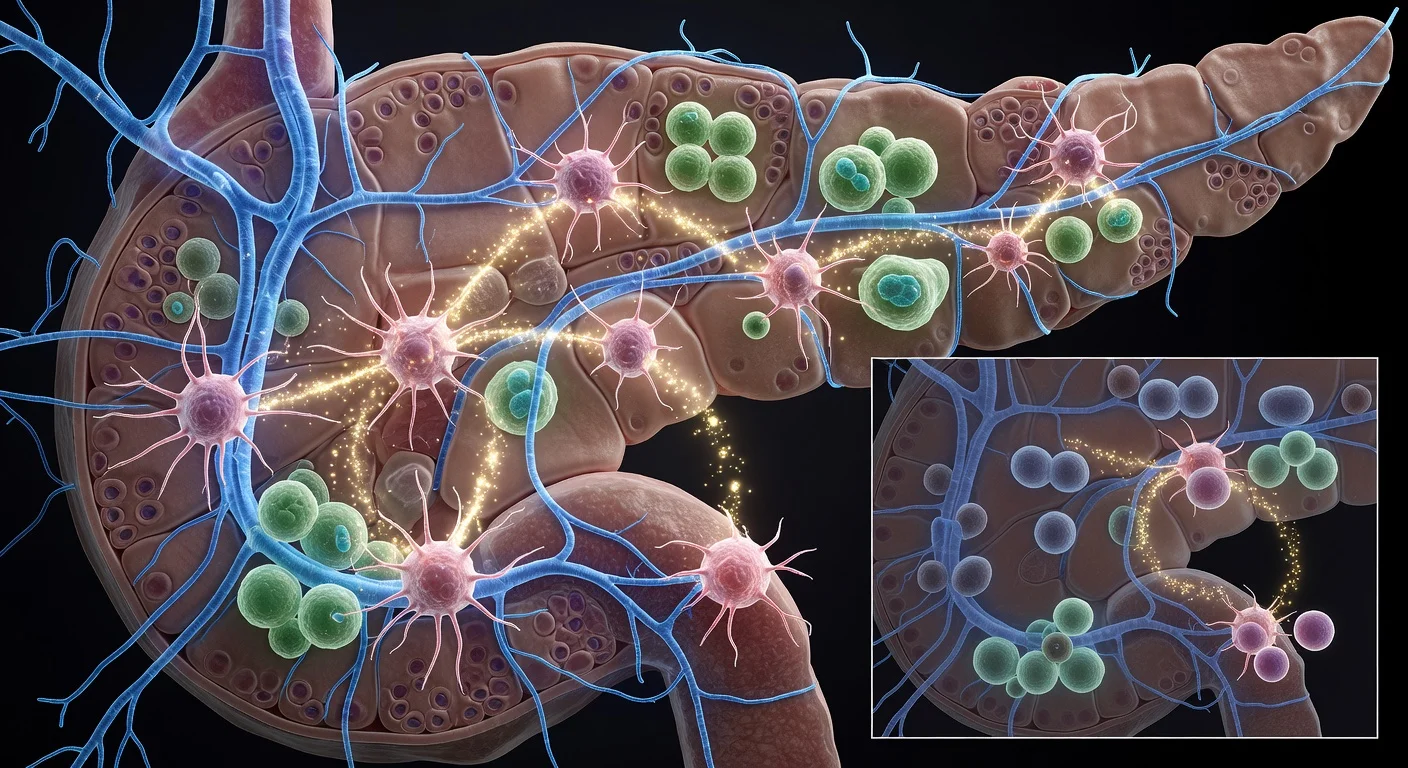
Des chercheurs du Cold Spring Harbor Laboratory rapportent que des cellules de soutien connues sous le nom de fibroblastes associés au cancer myofibroblastiques (myCAFs) peuvent recruter des fibres nerveuses sympathiques dans des lésions pancréatiques précoces, créant une boucle de rétroaction qui peut aider le cancer du pancréas à s'établir avant la formation de tumeurs complètes. Dans des expériences sur des souris, perturber l'activité nerveuse sympathique a réduit l'activation des fibroblastes et a été associée à une réduction de près de 50 % de la croissance tumorale.
Le cancer du pancréas est difficile à détecter précocement et répond souvent mal aux traitements standards, des facteurs qui ont poussé les scientifiques à chercher de nouvelles façons de ralentir la maladie avant qu'elle ne progresse. nnUne équipe du Cold Spring Harbor Laboratory (CSHL), dirigée par le chercheur postdoctoral Jérémy Nigri dans le laboratoire du professeur David Tuveson, s'est concentrée sur la manière dont le système nerveux peut influencer les stades les plus précoces du cancer du pancréas. Nigri a noté que les chercheurs ont depuis longtemps reconnu l'invasion périneurale — un processus par lequel les cellules cancéreuses se propagent le long des nerfs — comme une façon dont les tumeurs pancréatiques peuvent se disséminer. nn## Les nerfs présents avant la formation complète des tumeurs nnDans ce nouveau travail, les chercheurs rapportent des preuves que les nerfs peuvent jouer un rôle actif encore plus tôt que l'invasion périneurale, apparaissant dans et autour des lésions pancréatiques précancéreuses. nnEn utilisant l'immunofluorescence en monture entière pour générer des images tridimensionnelles, l'équipe a observé des réseaux nerveux denses entrelacés à travers les lésions pancréatiques et étroitement associés à des fibroblastes promoteurs de tumeurs connus sous le nom de myCAFs. Dans des vues bidimensionnelles conventionnelles, les mêmes structures nerveuses peuvent apparaître comme de petites puncta dispersées. nn> «Quand nous avons vu cette image pour la première fois, j'ai été choqué», a déclaré Nigri. «Je ne pouvais même pas imaginer la lésion comme ça. Je ne l'avais vue qu'en 2D.» nn## Une boucle de rétroaction proposée impliquant des nerfs sympathiques nnSur la base d'expériences sur des souris et des systèmes cellulaires humains, les chercheurs décrivent un cycle dans lequel les myCAFs émettent des signaux qui attirent des fibres du système nerveux sympathique, qui régit la réponse combat ou fuite du corps. Ces fibres nerveuses libèrent de la norépinéphrine, et l'étude rapporte que la norépinéphrine peut se lier aux fibroblastes et déclencher une augmentation du calcium intracellulaire. La montée de calcium résultante active davantage les myCAFs, une réponse que les chercheurs disent pouvoir promouvoir la croissance précancéreuse tout en attirant des fibres nerveuses supplémentaires — renforçant la boucle. nn## Interrompre l'activité nerveuse a réduit la croissance tumorale chez les souris nnPour tester si perturber cette signalisation pouvait ralentir la maladie, l'équipe a utilisé une neurotoxine dans une expérience sur souris pour désactiver l'activité du système nerveux sympathique. Ils ont rapporté une activation réduite des fibroblastes et une réduction de près de 50 % de la croissance tumorale. nn> «Dans une expérience, nous utilisons une neurotoxine pour désactiver le système nerveux sympathique», a déclaré Nigri. «Nous montrons une activation réduite des fibroblastes et une réduction de près de 50 % de la croissance tumorale.» nn## Implications thérapeutiques et prochaines étapes nnLes résultats ont été publiés dans Cancer Discovery, une revue de l'American Association for Cancer Research. Les chercheurs suggèrent que, comme l'interaction nerf-myCAF apparaît tôt, elle pourrait représenter une cible thérapeutique potentielle. Ils pointent également des médicaments cliniquement disponibles — y compris le doxazosin — comme candidats à explorer en combinaison avec des approches établies telles que la chimiothérapie ou l'immunothérapie. nn> «La prochaine étape sera d'étudier cela plus en détail et d'essayer de trouver un moyen de bloquer la crosstalk entre les fibroblastes et les nerfs», a déclaré Nigri. nnLe CSHL a indiqué que le travail a été soutenu par plusieurs financeurs, y compris la Lustgarten Foundation et le Pancreatic Cancer Action Network. n