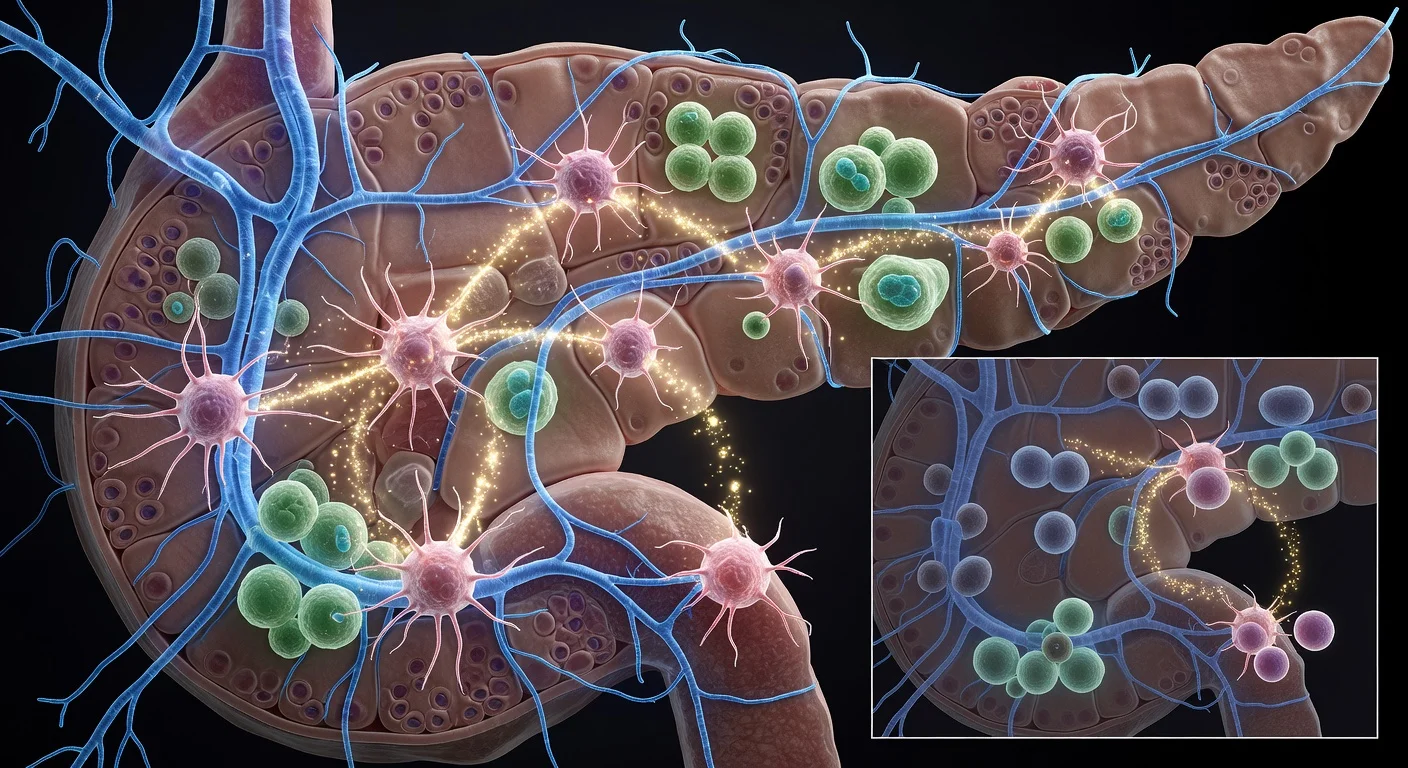
Pesquisadores do Cold Spring Harbor Laboratory relatam que células de suporte conhecidas como fibroblastos associados ao câncer miofibroblásticos (myCAFs) podem recrutar fibras nervosas simpáticas para lesões pancreáticas iniciais, criando um laço de feedback que pode ajudar o câncer pancreático a se estabelecer antes da formação de tumores completos. Em experimentos com camundongos, interromper a atividade nervosa simpática reduziu a ativação de fibroblastos e foi associada a uma redução de quase 50% no crescimento tumoral.
O câncer pancreático é difícil de detectar precocemente e frequentemente responde mal aos tratamentos padrão, fatores que impulsionaram os cientistas a buscar novas maneiras de retardar a doença antes que avance. nnUma equipe do Cold Spring Harbor Laboratory (CSHL), liderada pelo pesquisador pós-doutoral Jérémy Nigri no laboratório do Professor David Tuveson, focou em como o sistema nervoso pode influenciar os estágios iniciais do câncer pancreático. Nigri observou que os pesquisadores há muito reconhecem a invasão perineural — um processo em que as células cancerosas se espalham ao longo dos nervos — como uma forma pela qual os tumores pancreáticos podem se disseminar. nn## Nervos presentes antes dos tumores se formarem completamente nnNo novo trabalho, os pesquisadores relatam evidências de que os nervos podem desempenhar um papel ativo ainda antes da invasão perineural, aparecendo em e ao redor de lesões pancreáticas pré-cancerosas. nnUsando imunofluorescência de montagem completa para gerar imagens tridimensionais, a equipe observou redes nervosas densas entrelaçadas através de lesões pancreáticas e intimamente associadas a fibroblastos promotores de tumores conhecidos como myCAFs. Em visualizações bidimensionais convencionais, as mesmas estruturas nervosas podem aparecer como pequenas punctas espalhadas. nn> «Quando vimos esta imagem pela primeira vez, fiquei chocado», disse Nigri. «Eu nem conseguia imaginar a lesão assim. Eu só a tinha visto em 2D.» nn## Um laço de feedback proposto envolvendo nervos simpáticos nnCom base em experimentos com camundongos e sistemas de células humanas, os pesquisadores descrevem um ciclo em que myCAFs emitem sinais que atraem fibras do sistema nervoso simpático, que governa a resposta de luta ou fuga do corpo. Essas fibras nervosas liberam norepinefrina, e o estudo relata que a norepinefrina pode se ligar a fibroblastos e desencadear um aumento no cálcio intracelular. O surto de cálcio resultante ativa ainda mais os myCAFs, uma resposta que os pesquisadores dizem poder promover o crescimento pré-canceroso enquanto atrai fibras nervosas adicionais — reforçando o laço. nn## Interromper a atividade nervosa reduziu o crescimento tumoral em camundongos nnPara testar se interromper essa sinalização poderia retardar a doença, a equipe usou uma neurotoxina em um experimento com camundongos para desativar a atividade do sistema nervoso simpático. Eles relataram ativação reduzida de fibroblastos e uma redução de quase 50% no crescimento tumoral. nn> «Em um experimento, usamos uma neurotoxina para desativar o sistema nervoso simpático», disse Nigri. «Mostramos ativação reduzida de fibroblastos e uma redução de quase 50% no crescimento tumoral.» nn## Implicações para tratamento e próximos passos nnOs achados foram publicados em Cancer Discovery, uma revista da American Association for Cancer Research. Os pesquisadores sugerem que, como a interação nervo–myCAF aparece cedo, pode representar um alvo terapêutico potencial. Eles também apontam drogas clinicamente disponíveis — incluindo doxazosin — como candidatas a explorar em combinação com abordagens estabelecidas como quimioterapia ou imunoterapia. nn> «O próximo passo será estudar isso em mais detalhes e tentar encontrar uma maneira de bloquear a crosstalk entre fibroblastos e nervos», disse Nigri. nnO CSHL disse que o trabalho foi apoiado por múltiplos financiadores, incluindo a Lustgarten Foundation e a Pancreatic Cancer Action Network. n