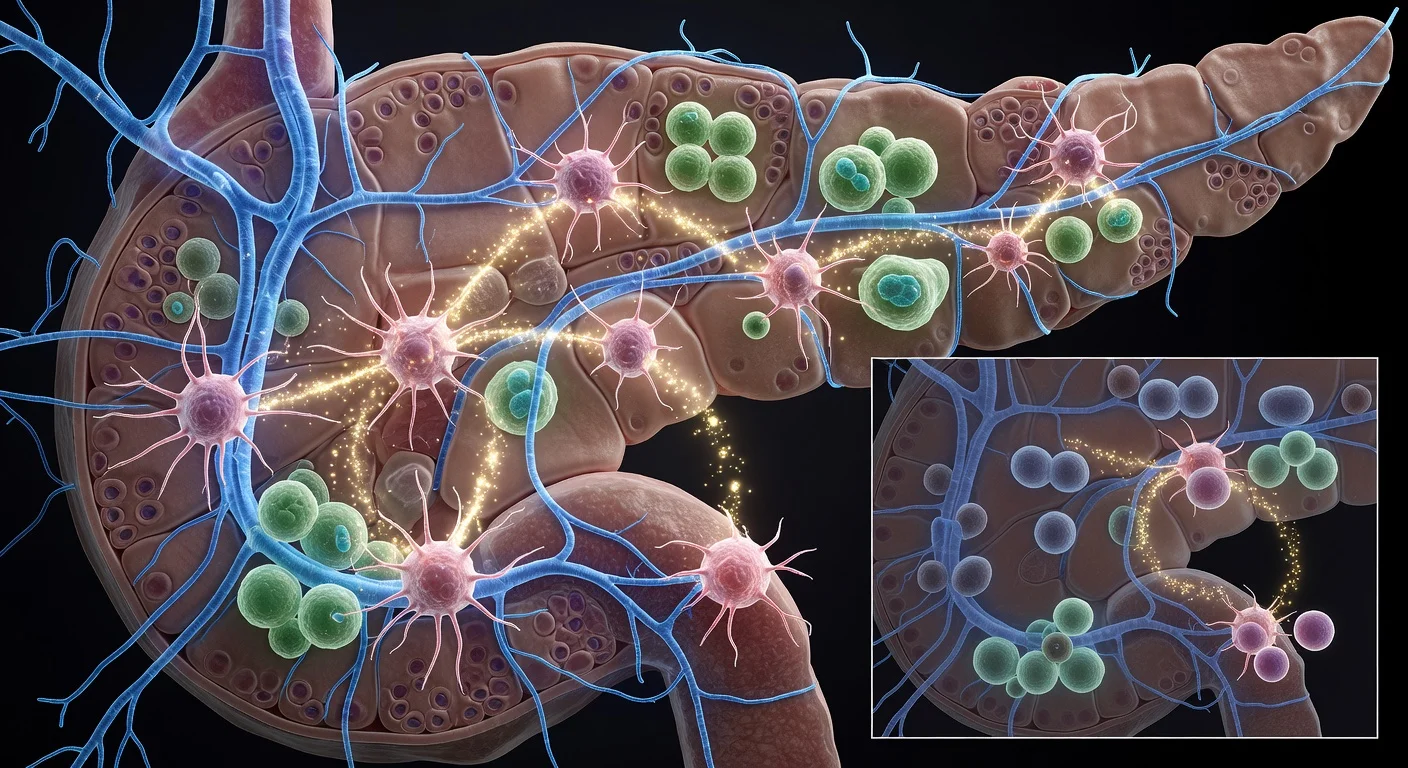
Peneliti di Cold Spring Harbor Laboratory melaporkan bahwa sel pendukung yang dikenal sebagai fibroblas terkait kanker miofibroblastik (myCAFs) dapat merekrut serat saraf simpatik ke lesi pankreas dini, menciptakan lingkaran umpan balik yang dapat membantu kanker pankreas bertahan sebelum tumor penuh terbentuk. Dalam eksperimen pada tikus, mengganggu aktivitas saraf simpatik mengurangi aktivasi fibroblas dan dikaitkan dengan pengurangan hampir 50% dalam pertumbuhan tumor.
Kanker pankreas sulit dideteksi dini dan sering merespons buruk terhadap pengobatan standar, faktor-faktor yang mendorong para ilmuwan mencari cara baru untuk memperlambat penyakit sebelum berkembang. nnTim di Cold Spring Harbor Laboratory (CSHL), yang dipimpin oleh peneliti pascadoktoral Jérémy Nigri di laboratorium Profesor David Tuveson, fokus pada bagaimana sistem saraf dapat memengaruhi tahap awal kanker pankreas. Nigri mencatat bahwa para peneliti telah lama mengenali invansi perineural—proses di mana sel kanker menyebar sepanjang saraf—sebagai salah satu cara tumor pankreas dapat menyebar. nn## Saraf hadir sebelum tumor terbentuk sepenuhnya nnDalam penelitian baru, para peneliti melaporkan bukti bahwa saraf mungkin berperan aktif bahkan lebih awal daripada invansi perineural, muncul di dan sekitar lesi pankreas pra-kanker. nnMenggunakan imunofluoresensi whole-mount untuk menghasilkan gambar tiga dimensi, tim mengamati jaringan saraf padat yang terjalin melalui lesi pankreas dan erat terkait dengan fibroblas pendorong tumor yang dikenal sebagai myCAFs. Dalam tampilan dua dimensi konvensional, struktur saraf yang sama dapat tampak sebagai titik-titik kecil yang tersebar. nn> «Ketika pertama kali melihat gambar ini, saya terkejut,» kata Nigri. «Saya bahkan tidak bisa membayangkan lesi seperti ini. Saya hanya pernah melihatnya dalam 2D.» nn## Lingkaran umpan balik yang diusulkan melibatkan saraf simpatik nnBerdasarkan eksperimen pada tikus dan sistem sel manusia, para peneliti menggambarkan siklus di mana myCAFs mengeluarkan sinyal yang menarik serat dari sistem saraf simpatik, yang mengatur respons fight-or-flight tubuh. Serat saraf tersebut melepaskan norepinefrin, dan studi melaporkan bahwa norepinefrin dapat mengikat fibroblas dan memicu peningkatan kalsium intraseluler. Lonjakan kalsium yang dihasilkan semakin mengaktifkan myCAFs, respons yang menurut para peneliti dapat mempromosikan pertumbuhan pra-kanker sambil menarik serat saraf tambahan—memperkuat lingkaran tersebut. nn## Mengganggu aktivitas saraf mengurangi pertumbuhan tumor pada tikus nnUntuk menguji apakah mengganggu sinyal ini dapat memperlambat penyakit, tim menggunakan neurotoksin dalam satu eksperimen tikus untuk menonaktifkan aktivitas sistem saraf simpatik. Mereka melaporkan aktivasi fibroblas yang berkurang dan pengurangan hampir 50% dalam pertumbuhan tumor. nn> «Dalam satu eksperimen, kami menggunakan neurotoksin untuk menonaktifkan sistem saraf simpatik,» kata Nigri. «Kami menunjukkan aktivasi fibroblas yang berkurang dan pengurangan hampir 50% dalam pertumbuhan tumor.» nn## Implikasi pengobatan dan langkah selanjutnya nnTemuan ini diterbitkan di Cancer Discovery, jurnal dari American Association for Cancer Research. Para peneliti menyarankan bahwa karena interaksi saraf–myCAF muncul dini, itu mungkin menjadi target terapeutik potensial. Mereka juga menunjuk obat-obatan yang tersedia secara klinis—termasuk doxazosin—sebagai kandidat untuk dieksplorasi dalam kombinasi dengan pendekatan yang sudah ada seperti kemoterapi atau imunoterapi. nn> «Langkah selanjutnya adalah mempelajari ini lebih detail dan mencoba menemukan cara untuk memblokir crosstalk antara fibroblas dan saraf,» kata Nigri. nnCSHL mengatakan bahwa pekerjaan ini didukung oleh beberapa pendana, termasuk Lustgarten Foundation dan Pancreatic Cancer Action Network. n