Cold Spring Harbor Laboratoryの研究者らは、筋線維芽細胞様がん関連線維芽細胞(myCAFs)と呼ばれる支持細胞が、早期膵臓病変に交感神経繊維を募集し、完全腫瘍形成前に膵臓がんが定着するのを助けるフィードバックループを作成できると報告した。マウス実験では、交感神経活動を阻害すると線維芽細胞活性化が減少し、腫瘍成長がほぼ50%減少したことが関連付けられた。
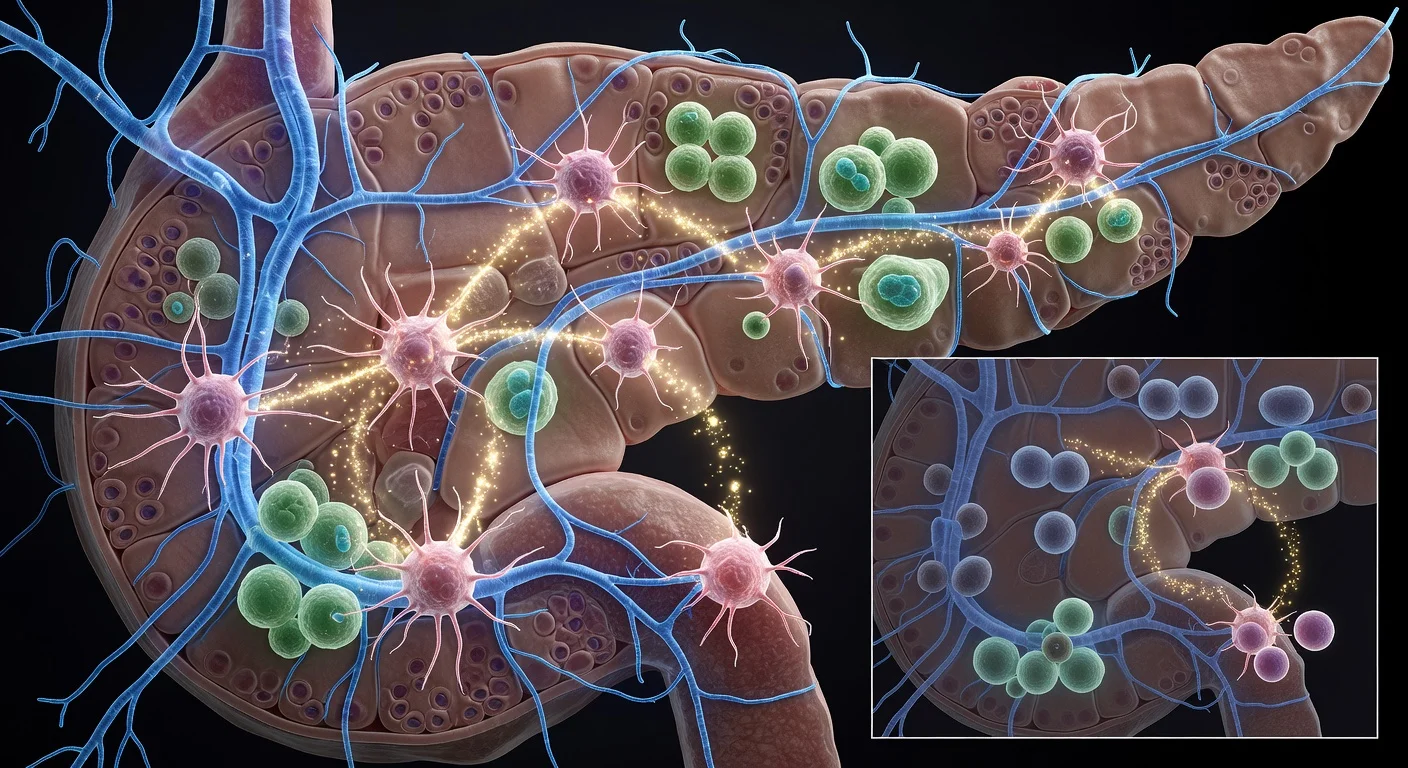
膵臓がんは早期発見が難しく、標準治療への反応も悪いことが多く、これらの要因が科学者たちを疾患進行前に遅らせる新たな方法を探す駆動力となっている。 nnCold Spring Harbor Laboratory(CSHL)のチームは、教授David Tuveson研究室の博士研究員Jérémy Nigri氏が率い、膵臓がんの最も初期段階で神経系がどのように影響を与えるかに焦点を当てた。Nigri氏は、研究者らが長年神経周囲浸潤—がん細胞が神経に沿って広がるプロセス—を膵臓腫瘍が拡散する一つの方法として認識してきたと指摘した。 nn## 腫瘍が完全に形成される前に神経が存在 nn新たな研究では、神経が神経周囲浸潤よりもさらに早く積極的な役割を果たす可能性があり、前がん性膵臓病変内および周囲に現れる証拠を報告した。 nn*whole-mount immunofluorescenceを使用して3次元画像を生成したところ、チームは膵臓病変を通り抜ける密集した神経ネットワークを観察し、腫瘍促進性線維芽細胞であるmyCAFsと密接に関連していることがわかった。通常の2次元ビューでは、同じ神経構造が小さな散在する点として見える。 nn> 「この画像を初めて見た時、衝撃を受けました」とNigri氏。「こんな病変は想像もできませんでした。2Dでしか見たことがありませんでした。」 nn## 交感神経を含む提案されたフィードバックループ nnマウスとヒト細胞系での実験に基づき、研究者らはmyCAFsが交感神経系(体のfight-or-flight反応を司る)からの繊維を引きつけるシグナルを発し、その神経繊維がノルエピネフリンを放出すると記述した。研究では、ノルエピネフリンが線維芽細胞に結合し、細胞内カルシウムの上昇を引き起こすと報告されており、そのカルシウム急増がmyCAFsをさらに活性化し、前がん性成長を促進しながら追加の神経繊維を引きつけ—ループを強化する。 nn## 神経活動の中断がマウスで腫瘍成長を減少 nnこのシグナルを阻害することで疾患を遅らせるかをテストするため、チームはマウス実験で神経毒を使用して交感神経系の活動を無効化した。線維芽細胞活性化の減少と腫瘍成長のほぼ50%減少を報告した。 nn> 「一つの実験で、神経毒を使って交感神経系を無効化しました」とNigri氏。「線維芽細胞活性化の減少と腫瘍成長のほぼ50%減少を示しました。」 nn## 治療への示唆と次のステップ nnこの発見はAmerican Association for Cancer Researchの雑誌*Cancer Discoveryに掲載された。研究者らは、神経–myCAF相互作用が早期に現れるため、潜在的な治療標的となり得ると提案し、化学療法や免疫療法などの確立されたアプローチと組み合わせる候補として臨床的に利用可能な薬—doxazosinを含む—を挙げている。 nn> 「次のステップはこれをより詳細に研究し、線維芽細胞と神経間のクロストークをブロックする方法を見つけることです」とNigri氏。 nnCSHLによると、この研究はLustgarten FoundationやPancreatic Cancer Action Networkを含む複数の資金提供者により支援された。 n