Forskare vid Cold Spring Harbor Laboratory rapporterar att stödceller kända som myofibroblastiska cancerassocierade fibroblaster (myCAFs) kan rekrytera sympatiska nervfibrer till tidiga pankreasläsioner, vilket skapar en feedbackloop som kan hjälpa pankreascancer att etablera sig innan fullständiga tumörer bildas. I musexperiment minskade störning av sympatisk nervaktivitet fibroblastaktivering och var associerad med en minskning med nästan 50 procent av tumörtillväxten.
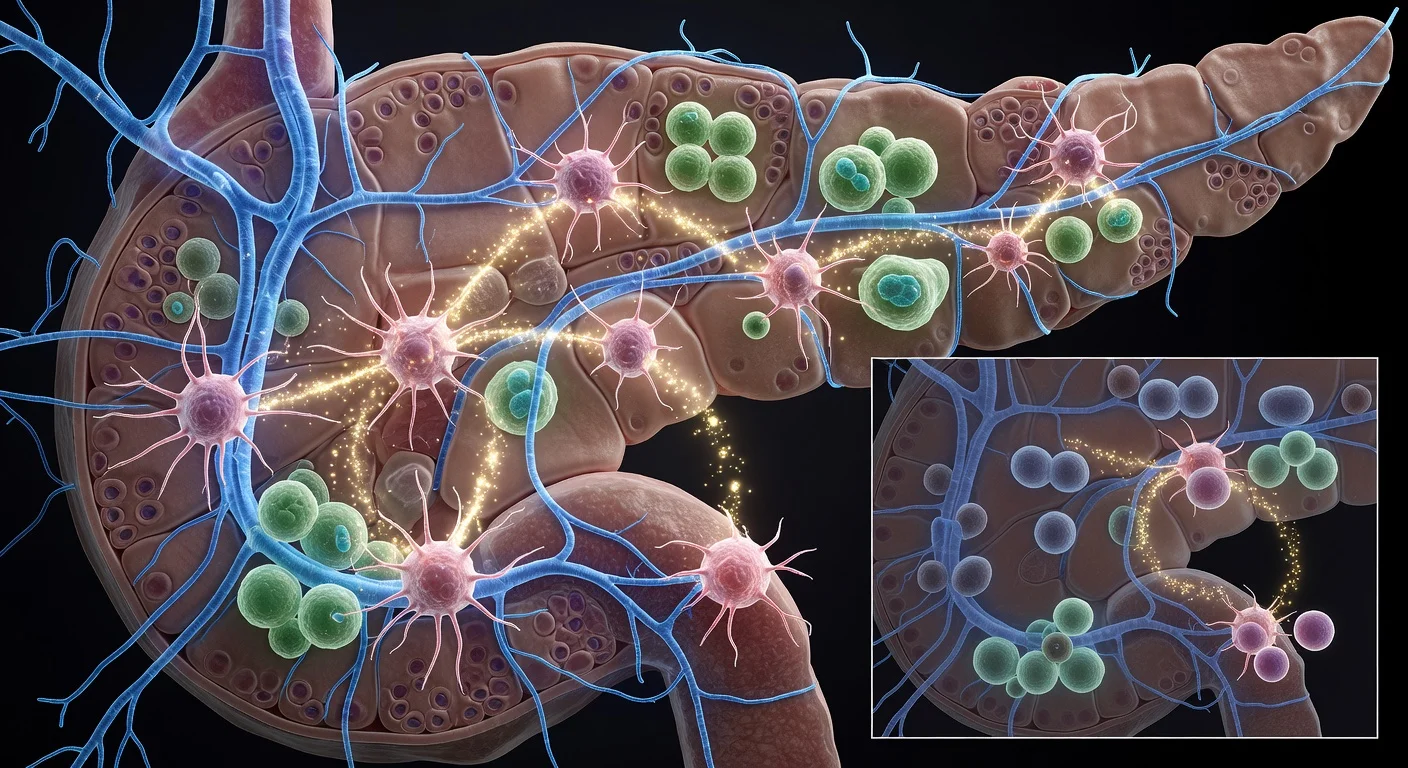
Pankreascancer är svår att upptäcka tidigt och svarar ofta dåligt på standardbehandlingar, faktorer som drivit forskare att leta efter nya sätt att bromsa sjukdomen innan den fortskrider. nnEtt team vid Cold Spring Harbor Laboratory (CSHL), lett av postdoktorala forskaren Jérémy Nigri i professor David Tuvesons laboratorium, fokuserade på hur nervsystemet kan påverka pankreascancerns tidigaste stadier. Nigri noterade att forskare länge känt till perineural invasion – en process där cancerceller sprider sig längs nerver – som ett sätt som pankreastumörer kan spridas på. nn## Nerver närvarande innan tumörer bildas helt nnI det nya arbetet rapporterar forskarna bevis för att nerver kan spela en aktiv roll ännu tidigare än perineural invasion, och dyka upp i och runt prekankrosa pankreasläsioner. nnMed hjälp av whole-mount immunofluorescence för att skapa tredimensionella bilder observerade teamet täta nervnätverk vävda genom pankreasläsioner och nära associerade med tumörfrämjande fibroblaster kända som myCAFs. I konventionella tvådimensionella vyer kan samma nervstrukturer se ut som små spridda punkter. nn> «När vi först såg den här bilden blev jag chockad», sa Nigri. «Jag kunde inte ens föreställa mig lesionen så här. Jag hade bara sett den i 2D.» nn## En föreslagen feedbackloop med sympatiska nerver nnBaserat på experiment på möss och humana cellsystem beskriver forskarna en cykel där myCAFs avger signaler som attraherar fibrer från det sympatiska nervsystemet, som styr kroppens fight-or-flight-svar. Dessa nervfibrer frisätter noradrenalin, och studien rapporterar att noradrenalin kan binda till fibroblaster och utlösa en ökning av intracellulärt kalcium. Den resulterande kalciumtoppen aktiverar myCAFs ytterligare, en reaktion som forskarna säger kan främja prekancros tillväxt samtidigt som den drar till sig fler nervfibrer – och förstärker loopen. nn## Att avbryta nervaktivitet minskade tumörtillväxt hos möss nnFör att testa om att störa denna signalering kunde bromsa sjukdomen använde teamet en neurotoxin i ett musexperiment för att inaktivera sympatisk nervsystemaktivitet. De rapporterade minskad fibroblastaktivering och en minskning med nästan 50 procent av tumörtillväxten. nn> «I ett experiment använder vi en neurotoxin för att inaktivera det sympatiska nervsystemet», sa Nigri. «Vi visar minskad fibroblastaktivering och en minskning med nästan 50 procent av tumörtillväxten.» nn## Behandlingsimplikationer och nästa steg nnResultaten publicerades i Cancer Discovery, en tidskrift från American Association for Cancer Research. Forskarna föreslår att eftersom nerv–myCAF-interaktionen uppträder tidigt kan den vara ett potentiellt terapeutiskt mål. De pekar också på kliniskt tillgängliga läkemedel – inklusive doxazosin – som kandidater att utforska i kombination med etablerade metoder som kemoterapi eller immunterapi. nn> «Nästa steg blir att studera detta mer i detalj och försöka hitta ett sätt att blockera krosstalken mellan fibroblaster och nerver», sa Nigri. nnCSHL uppgav att arbetet stöddes av flera finansiärer, inklusive Lustgarten Foundation och Pancreatic Cancer Action Network. n