باحثون في جامعة واشنطن للطب في سانت لويس، بالتعاون مع علماء في جامعة نورث ويسترن، طوروا علاجًا نانويًا أنفيًا غير جراحي ينشط الجهاز المناعي لمهاجمة أورام الدماغ العدوانية في الفئران. من خلال تسليم أحماض نووية كروية تثير مسار STING المناعي مباشرة من الأنف إلى الدماغ، قضى النهج على أورام الغليوبلاستوما في نماذج الفئران عند دمجه مع أدوية تعزز نشاط خلايا T، وفقًا لدراسة في *Proceedings of the National Academy of Sciences*.
الغليوبلاستوما، أكثر أورام الدماغ الخبيثة شيوعًا، تصيب حوالي ثلاثة من كل 100,000 شخص في الولايات المتحدة وتتقدم بسرعة، مع كون المرض قاتلاً تقريبًا دائمًا. يتطور من النجميات، نوع من خلايا الدماغ، وهو صعب العلاج بشكل خاص لأنه من الصعب تسليم الأدوية عبر حاجز الدماغ الدموي.
في دراسة ما قبل السريرية جديدة، يبلغ باحثون في جامعة واشنطن للطب في سانت لويس وجامعة نورث ويسترن عن بديل واعد: أحماض نووية كروية مبنية على نوى nanopartículas de oro التي تنشط مسار STING المناعي عند تسليمها كقطرات أنفية. العمل، بقيادة المؤلفين المشتركين المقابلين ألكسندر إتش. ستيغ، دكتوراه، من جامعة واشنطن، وتشار أ. ميركين، دكتوراه، من جامعة نورث ويسترن، موصوف في مجلة Proceedings of the National Academy of Sciences.
مسار STING —اختصار لـ stimulator of interferon genes— يساعد في إثارة الدفاعات المناعية عندما تكتشف الخلايا الحمض النووي الأجنبي، وقد كان هدفًا رئيسيًا لتحويل الأورام "الباردة" مثل الغليوبلاستوما إلى أورام "ساخنة" تستجيب للعلاج المناعي. أظهرت دراسات سابقة أن الأدوية المصممة لتنشيط STING يمكن أن تعد الجهاز المناعي لمهاجمة الغليوبلاستوما، لكن هذه العوامل تتحلل بسرعة في الجسم وعادة ما يجب حقنها مباشرة في الورم، غالبًا ما تتطلب إجراءات متكررة شديدة التوغل.
"أردنا تغيير هذه الواقعية وتطوير علاج غير جراحي ينشط الاستجابة المناعية لمهاجمة الغليوبلاستوما"، قال ستيغ، وفقًا لجامعة واشنطن. أضاف أن نتائج الفريق تظهر أن النانوهياكل المصممة بدقة المعروفة باسم الأحماض النووية الكروية يمكن أن تنشط مسارات مناعية قوية داخل الدماغ بأمان وفعالية.
لمعالجة قيود محفزات STING الحالية، عمل الباحثون مع ميركين، الذي اخترع الأحماض النووية الكروية —هياكل نانوية تتكون فيها خيوط الحمض النووي أو الريبونوكلييك سميكة حول نواة nanopartícula—. معًا، صمم الفرق فئة جديدة من الأحماض النووية الكروية تحتوي على نوى nanopartículas de oro مغطاة بمقاطع قصيرة من الحمض النووي تنشط مسار STING في خلايا مناعية محددة. للتسليم إلى الدماغ، اختاروا الأنف كطريق الدخول.
تم استكشاف العلاج الأنفي داخلي كوسيلة لتوجيه الأدوية إلى الدماغ، لكن، وفقًا لجامعة واشنطن وScienceDaily، لم تظهر أي علاج نانوي سابقًا القدرة على تنشيط استجابات مناعية ضد سرطانات الدماغ عبر هذا الطريق. "أردنا حقًا تقليل اضطرار المرضى للخضوع لـ[حقن الورم المباشرة] عندما يكونون مرضى بالفعل، واعتقدت أننا يمكننا استخدام منصات الأحماض النووية الكروية لتسليم هذه الأدوية بطريقة غير جراحية"، قالت المؤلفة الأولى أكانكشا ماهاجان، دكتوراه، باحثة ما بعد الدكتوراه المرتبطة في مختبر ستيغ.
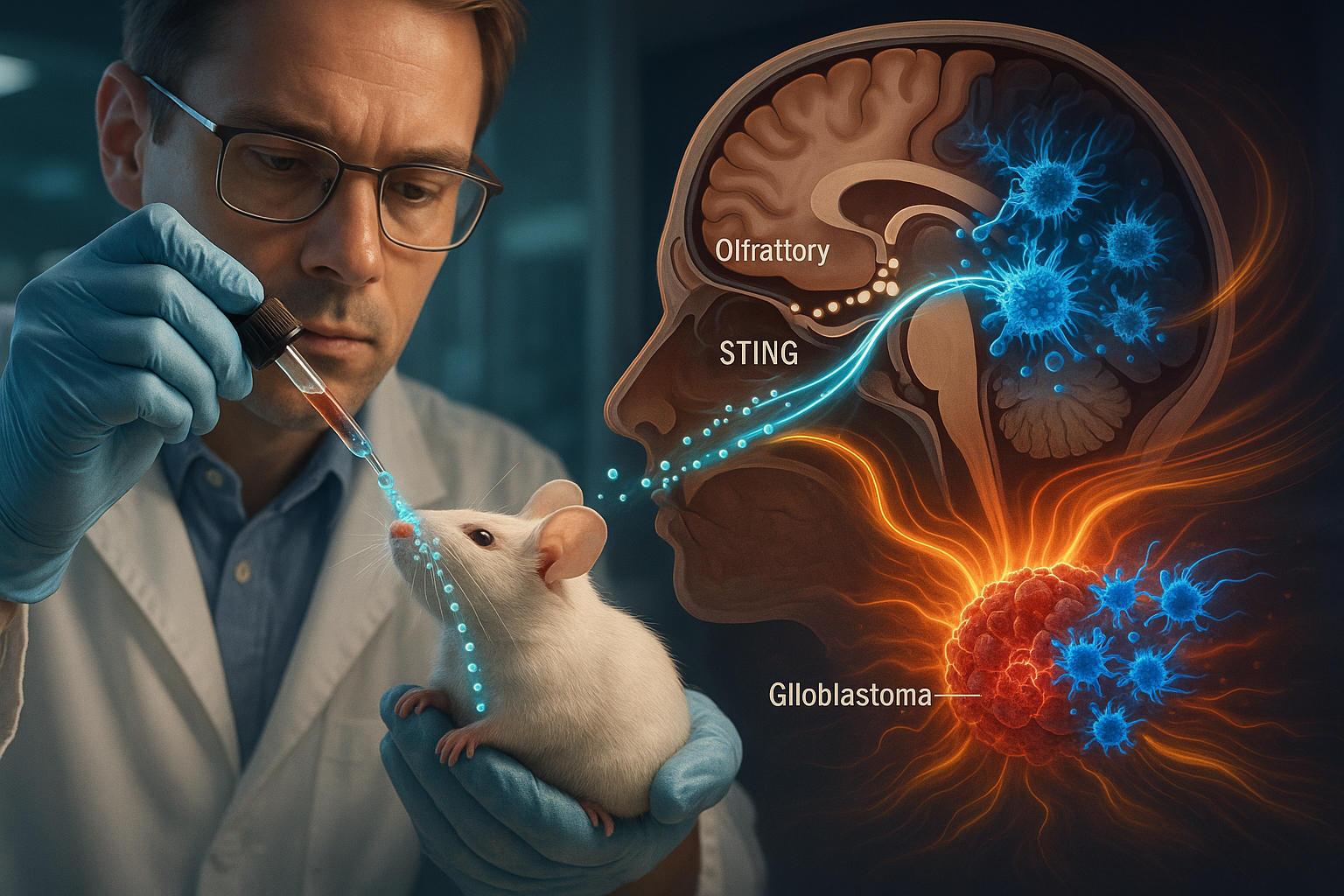
وسم الفريق الأحماض النووية الكروية بعلامة جزيئية مرئية تحت ضوء الأشعة تحت الحمراء القريبة لتتبع حركتها. في الفئران المصابة بالغليوبلاستوما، سافرت القطرات النانوية المعطاة في الممرات الأنفية على طول مسار العصب الرئيسي الذي يربط مناطق الوجه بالدماغ. بمجرد الوصول إلى الدماغ، تركزت النانودواء في الخلايا المناعية داخل الورم ومن حوله وأظهرت أيضًا نشاطًا في العقد الليمفاوية القريبة، بينما تجنبت في الغالب التوزيع إلى الأعضاء الأخرى، يبلغ الباحثون.
أظهرت تحليلات الخلايا المناعية داخل الأورام وقربها أن العلاج نشط مسار cGAS–STING وخلق بيئة ورمية أكثر التهابًا غنية بخلايا T الفعالة والماكروفاجات المؤيدة للالتهاب، متسقة مع دراسة PNAS الأساسية.
عند دمج النانو العلاج الأنفي داخلي مع أدوية مصممة لتنشيط الخلايا اللمفاوية T —مثل مثبطات نقاط التفتيش المناعية— قضت جرعة واحدة أو اثنتان على أورام الغليوبلاستوما في نماذج الفئران وأحدثت مناعة طويلة الأمد منعت عودة السرطانات، وفقًا لجامعة واشنطن وتقرير PNAS. أدى العلاج المشترك إلى تثبيط نمو الورم بشكل أكثر فعالية وأنتج بقاءً أطول من العلاجات المستهدفة لـSTING المختبرة حاليًا في نماذج مشابهة.
حذر ستيغ من أن تشغيل مسار STING ببساطة غير محتمل أن يعالج الغليوبلاستوما لوحده لأن الورم يستخدم آليات متعددة لكبح أو إغلاق الاستجابات المناعية. يستكشف مجموعته الآن طرقًا لإضافة قدرات إضافية لتنشيط المناعة إلى النانوهياكل بحيث يمكن معالجة عدة أهداف علاجية في علاج واحد.
الدراسة، المنشورة في عدد نوفمبر 2025 من Proceedings of the National Academy of Sciences، دعمتها منح من المعهد الوطني للسرطان وبرامج أخرى من المعاهد الوطنية للصحة، بالإضافة إلى مؤسسات تركز على الأمراض وتمويل مراكز السرطان المؤسسية، وفقًا لجامعة واشنطن وScienceDaily. تشمل الإفصاحات حيازة ستيغ لأسهم في Exicure Inc.، التي تطور منصات علاجية أحماض نووية كروية، وحيازة ميركين لأسهم في Flashpoint Therapeutics، التي تطور علاجات قائمة على SNA. كما أن ستيغ وميركين هما مخترعان مشتركان في براءة اختراع تصف نانوكونجوجات SNA مصممة لعبور حاجز الدماغ الدموي.