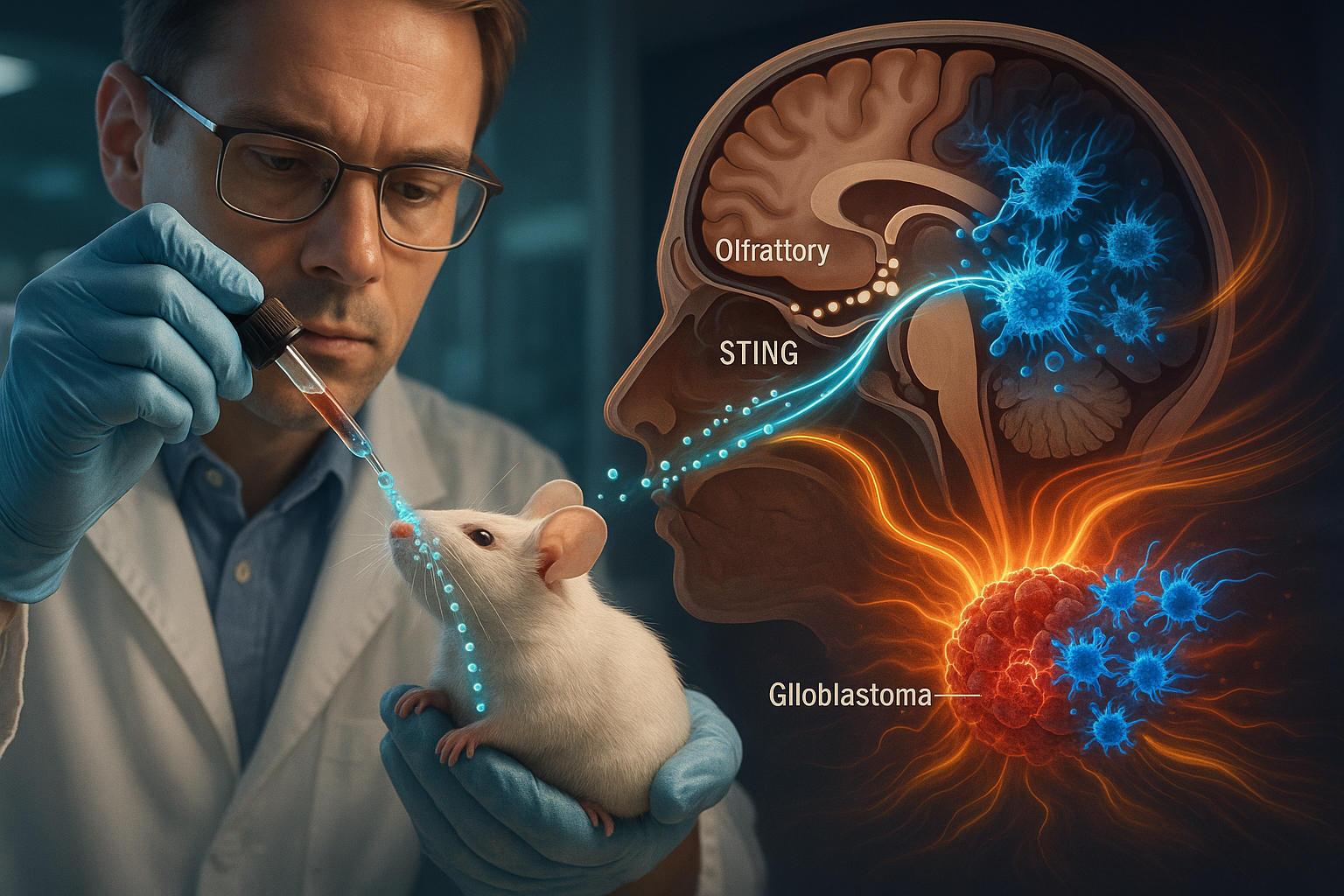
セントルイスのワシントン大学医学部研究者らが、北西部大学の科学者らと協力し、マウスにおける攻撃的な脳腫瘍を免疫系が攻撃するよう活性化する非侵襲的な鼻腔ナノ療法を開発した。STING免疫経路を活性化する球状核酸を鼻から直接脳に送達することで、このアプローチはT細胞活性向上薬と組み合わせた際にマウスモデルでグリオブラストーマ腫瘍を排除した、と全米科学アカデミー紀要に掲載された研究で明らかになった。
グリオブラストーマは最も一般的な悪性脳腫瘍で、米国では10万人あたり約3人に影響し、急速に進行し、ほぼ常に致死的である。この腫瘍は脳細胞の一種である星状細胞から発生し、血液脳関門を通過して薬物を送達するのが難しいため、特に治療が困難である。
新たな前臨床研究で、セントルイスのワシントン大学医学部と北西部大学の研究者らは有望な代替法を報告した。金ナノ粒子コア上に構築された球状核酸で、鼻滴として投与するとSTING免疫経路を活性化する。この研究は、ワシントン大学のAlexander H. Stegh博士と北西部大学のChad A. Mirkin博士による共同筆頭著者によるもので、全米科学アカデミー紀要に掲載された。
STING経路(インターフェロン遺伝子刺激因子)は、細胞が異物DNAを検知すると免疫防御を誘導し、グリオブラストーマのような「冷たい」腫瘍を免疫療法に応答する「熱い」腫瘍に変える主要標的となっている。過去の研究では、STINGを活性化する薬剤が免疫系をグリオブラストーマ攻撃に備えさせることを示したが、これらの薬剤は体内で急速に分解され、通常腫瘍に直接注入する必要があり、しばしば繰り返しの高度侵襲的手技を要する。
「この現実を変え、グリオブラストーマを攻撃する免疫応答を活性化する非侵襲的治療を開発したかった」とStegh氏はワシントン大学によると述べた。彼は、チームの結果が球状核酸と呼ばれる精密設計ナノ構造が脳内で強力な免疫経路を安全かつ効果的に活性化できることを示していると付け加えた。
既存のSTING作動薬の限界に対処するため、研究者らは球状核酸を発明したMirkin氏と協力した。球状核酸とは、ナノ粒子コア周囲にDNAまたはRNA鎖が密集したナノスケール構造である。両チームは、金ナノ粒子コアを短いDNA断片でコーティングし、特定の免疫細胞でSTING経路を活性化する新型球状核酸を設計した。脳への送達には鼻腔を入口とした。
鼻腔内療法は脳への薬物標的化として検討されてきたが、ワシントン大学とScienceDailyによると、この経路で脳がんに対する免疫応答を活性化するナノ療法はこれまで実証されていなかった。「患者がすでに病気の状態で[腫瘍直接注入]を避けたいと思い、球状核酸プラットフォームで非侵襲的にこれらの薬を送達できると考えた」と、Stegh研究室の博士研究員で初著者のAkanksha Mahajan博士は語った。
チームは球状核酸に近赤外光下で可視の分子ラベルを付与し、移動を追跡した。グリオブラストーマ保有マウスで鼻腔に投与したナノ滴は、顔面領域から脳を結ぶ主神経経路を進んだ。脳内では腫瘍内外の免疫細胞に集中し、近傍リンパ節でも活性が見られ、他の臓器への分布をほぼ回避したと研究者らは報告。
腫瘍内外の免疫細胞解析では、療法がcGAS–STING経路を活性化し、効果器T細胞とプロ炎症性マクロファージに富むよりプロ炎症性腫瘍微小環境を形成したことが、基盤PNAS研究と一致した。
鼻腔内ナノ療法をTリンパ球活性化薬(例:免疫チェックポイント阻害剤)と組み合わせると、1~2回の投与でマウスモデルにおけるグリオブラストーマ腫瘍を根絶し、がん再発を防ぐ長期免疫を誘導した、とワシントン大学とPNAS報告。併用療法は類似モデルでの現行STING標的療法より腫瘍増殖をより効果的に抑制し、生存期間を延長した。
Stegh氏は、STING経路の単純活性化だけでは腫瘍が免疫応答を複数機構で抑制するためグリオブラストーマを治癒しない可能性が高いと警告した。彼のグループは現在、ナノ構造に追加免疫活性化機能を加え、単一治療で複数標的を扱う方法を探っている。
2025年11月号のProceedings of the National Academy of Sciencesに掲載されたこの研究は、国立がん研究所や他のNIHプログラムからの助成金、疾患特化財団、機関がんセンター資金により支援された、とワシントン大学とScienceDaily。開示事項として、Stegh氏は球状核酸治療プラットフォームを開発するExicure Inc.の株式保有、Mirkin氏はSNAベース治療を開発するFlashpoint Therapeuticsの株式保有がある。Stegh氏とMirkin氏は血液脳関門通過用SNAナノ複合体の特許共同発明者でもある。