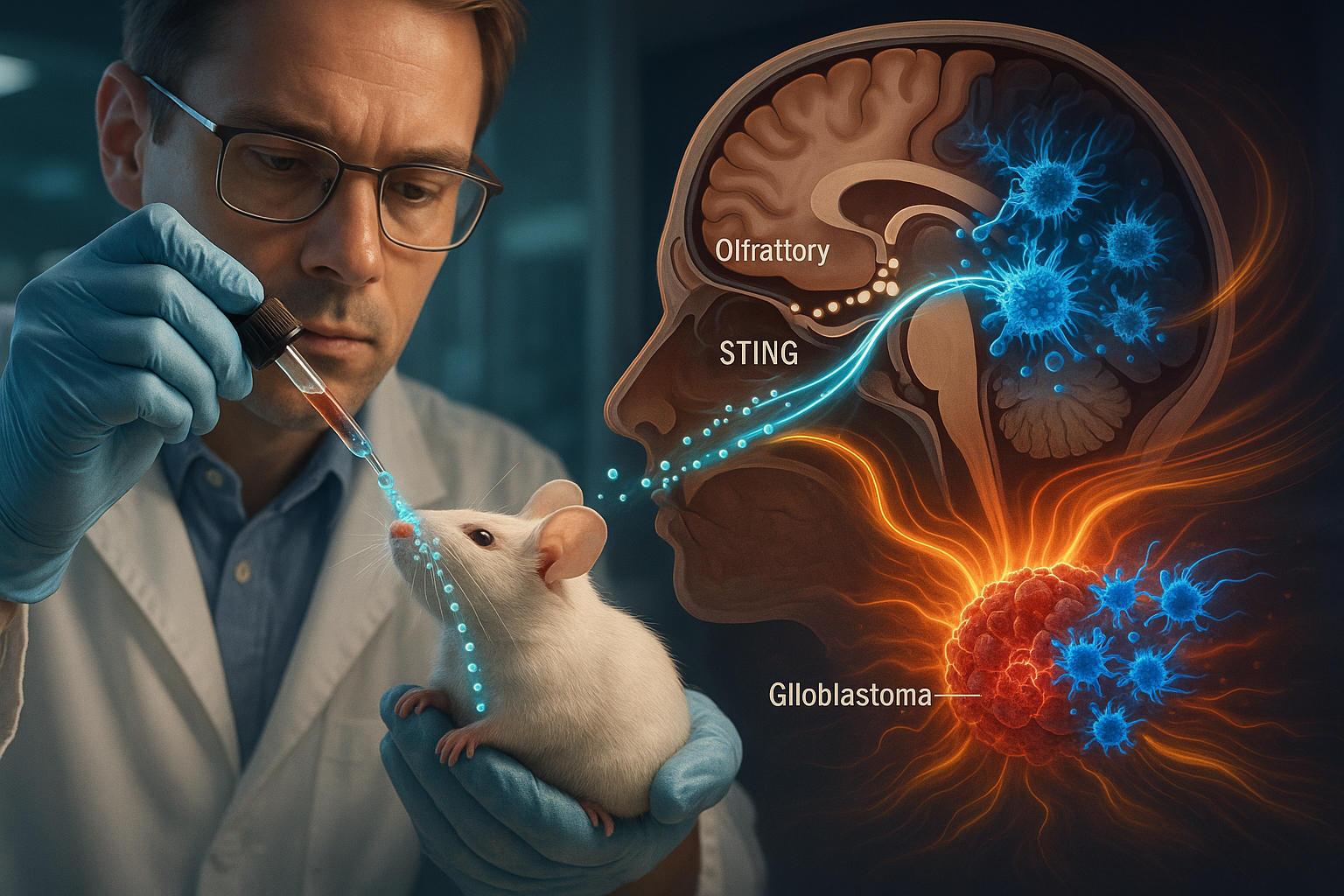
Investigadores de la Washington University School of Medicine en St. Louis, en colaboración con científicos de la Northwestern University, han desarrollado una nanoterapia nasal no invasiva que activa el sistema inmunitario para atacar tumores cerebrales agresivos en ratones. Al entregar ácidos nucleicos esféricos que activan la vía inmunitaria STING directamente desde la nariz al cerebro, el enfoque eliminó tumores de glioblastoma en modelos de ratones cuando se combinó con fármacos que potencian la actividad de las células T, según un estudio en los *Proceedings of the National Academy of Sciences*.
El glioblastoma, el tumor cerebral maligno más común, afecta a unas tres de cada 100.000 personas en Estados Unidos y progresa rápidamente, siendo la enfermedad casi siempre mortal. Se desarrolla a partir de astrocitos, un tipo de célula cerebral, y es particularmente difícil de tratar porque es complicado administrar fármacos a través de la barrera hematoencefálica.
En un nuevo estudio preclínico, investigadores de la Washington University School of Medicine en St. Louis y la Northwestern University informan de una alternativa prometedora: ácidos nucleicos esféricos construidos sobre núcleos de nanopartículas de oro que activan la vía inmunitaria STING cuando se administran como gotas nasales. El trabajo, liderado por los coautores correspondientes Alexander H. Stegh, PhD, de la Washington University, y Chad A. Mirkin, PhD, de la Northwestern University, se describe en la revista Proceedings of the National Academy of Sciences.
La vía STING —siglas en inglés de estimulador de genes de interferón— ayuda a activar las defensas inmunitarias cuando las células detectan ADN extraño, y ha sido un objetivo principal para convertir tumores "fríos" como el glioblastoma en tumores "calientes" que responden a la inmunoterapia. Estudios anteriores han demostrado que fármacos diseñados para activar STING pueden preparar el sistema inmunitario para atacar el glioblastoma, pero estos agentes se degradan rápidamente en el cuerpo y normalmente deben inyectarse directamente en el tumor, a menudo requiriendo procedimientos repetidos y altamente invasivos.
"Queríamos cambiar esta realidad y desarrollar un tratamiento no invasivo que active la respuesta inmunitaria para atacar el glioblastoma", dijo Stegh, según la Washington University. Añadió que los resultados del equipo muestran que nanogestructuras precisamente diseñadas conocidas como ácidos nucleicos esféricos pueden activar de manera segura y efectiva vías inmunitarias potentes en el cerebro.
Para abordar las limitaciones de los agonistas existentes de STING, los investigadores colaboraron con Mirkin, quien inventó los ácidos nucleicos esféricos —nanogestructuras en las que hebras de ADN o ARN están densamente dispuestas alrededor de un núcleo de nanopartícula—. Juntos, los equipos diseñaron una nueva clase de ácidos nucleicos esféricos con núcleos de nanopartículas de oro recubiertos con fragmentos cortos de ADN que activan la vía STING en células inmunitarias específicas. Para la entrega al cerebro, eligieron la nariz como vía de entrada.
La terapia intranasal se ha explorado como una forma de dirigir medicamentos al cerebro, pero, según la Washington University y ScienceDaily, ninguna nanoterapia había demostrado previamente la capacidad de activar respuestas inmunitarias contra cánceres cerebrales por esta vía. "Realmente queríamos minimizar que los pacientes tuvieran que someterse a [inyecciones directas en el tumor] cuando ya están enfermos, y pensé que podíamos usar las plataformas de ácidos nucleicos esféricos para entregar estos fármacos de manera no invasiva", dijo la primera autora Akanksha Mahajan, PhD, investigadora postdoctoral asociada en el laboratorio de Stegh.
El equipo etiquetó los ácidos nucleicos esféricos con una etiqueta molecular visible bajo luz infrarroja cercana para rastrear su movimiento. En ratones con glioblastoma, las nanogotas administradas en las fosas nasales viajaron a lo largo del trayecto del principal nervio que conecta las regiones faciales con el cerebro. Una vez en el cerebro, la nanomedicina se concentró en células inmunitarias dentro y alrededor del tumor y también mostró actividad en ganglios linfáticos cercanos, evitando en gran medida la distribución a otros órganos, informan los investigadores.
Análisis de células inmunitarias en y cerca de los tumores mostraron que la terapia activó la vía cGAS–STING y creó un microambiente tumoral más proinflamatorio enriquecido con células T efectoras y macrófagos proinflamatorios, consistente con el estudio subyacente de PNAS.
Cuando la nanoterapia intranasal se combinó con fármacos diseñados para activar linfocitos T —como inhibidores de puntos de control inmunitarios—, una o dos dosis erradicaron tumores de glioblastoma en modelos de ratones e indujeron inmunidad a largo plazo que previno el regreso de los cánceres, según la Washington University y el informe de PNAS. El tratamiento combinado inhibió el crecimiento tumoral de manera más efectiva y produjo una supervivencia más larga que las terapias dirigidas a STING actualmente probadas en modelos similares.
Stegh advirtió que simplemente activar la vía STING es poco probable que cure el glioblastoma por sí solo porque el tumor utiliza múltiples mecanismos para embotar o apagar las respuestas inmunitarias. Su grupo ahora está explorando formas de añadir más capacidades activadoras inmunitarias a las nanogestructuras para que varios objetivos terapéuticos puedan abordarse en un solo tratamiento.
El estudio, publicado en el número de noviembre de 2025 de Proceedings of the National Academy of Sciences, fue apoyado por subvenciones del National Cancer Institute y otros programas de los National Institutes of Health, así como por fundaciones enfocadas en enfermedades y financiación de centros de cáncer institucionales, según la Washington University y ScienceDaily. Las divulgaciones incluyen la participación accionarial de Stegh en Exicure Inc., que desarrolla plataformas terapéuticas de ácidos nucleicos esféricos, y la de Mirkin en Flashpoint Therapeutics, que desarrolla terapéuticos basados en SNA. Stegh y Mirkin también son coinventores de una patente que describe nanoconjugados SNA diseñados para cruzar la barrera hematoencefálica.