Researchers at the University of Chicago have shown that ultraviolet radiation can disable a protein that normally restrains inflammation in skin cells, promoting conditions that favor tumor development. The protein, YTHDF2, helps prevent harmful immune responses to sun-induced damage. The findings, published in the journal Nature Communications, suggest new strategies for reducing the risk of UV‑related skin cancer by targeting RNA–protein interactions.
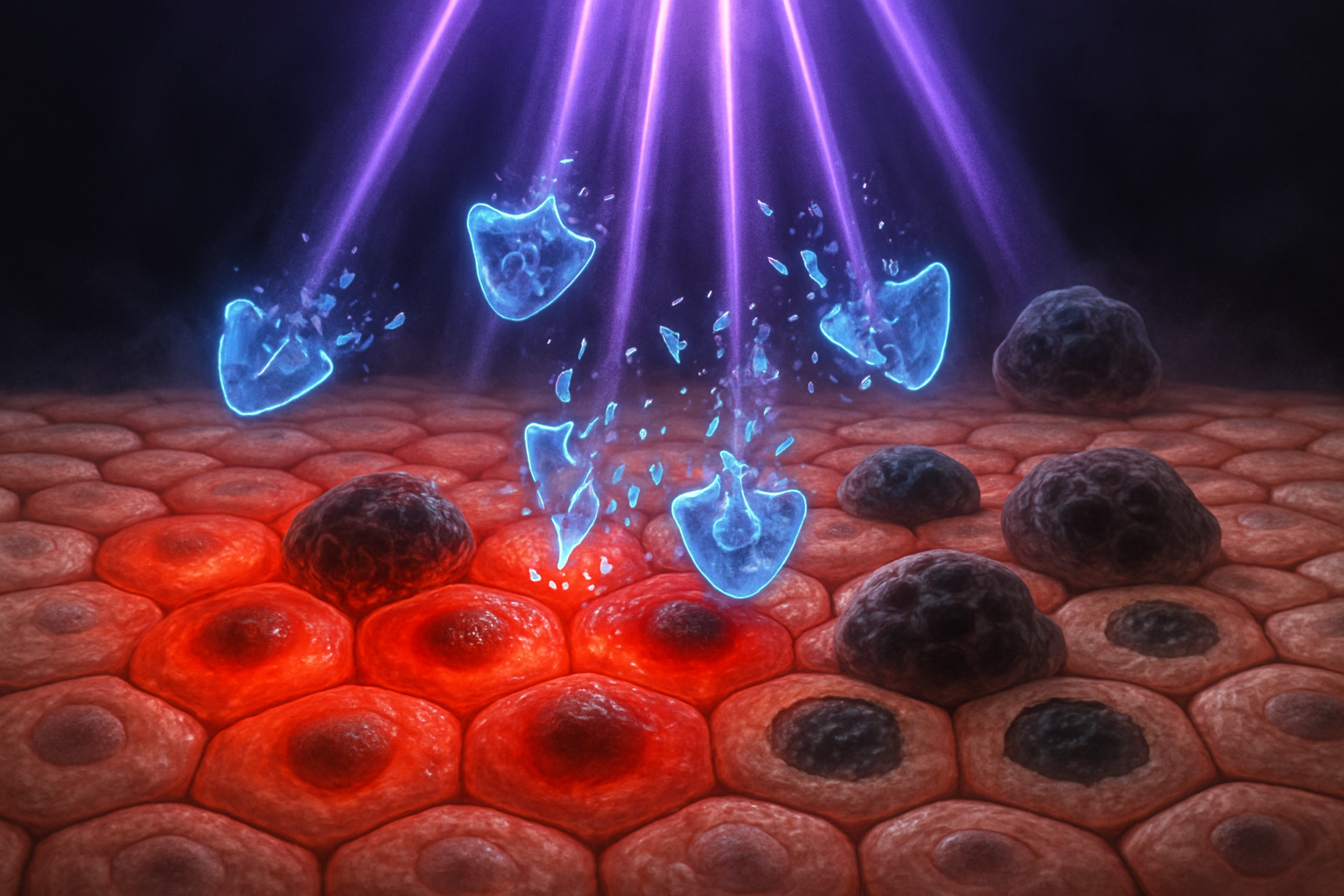
Sunlight is essential for vitamin D production, but prolonged exposure to ultraviolet (UV) rays is a major risk factor for skin cancer. UV radiation damages DNA and generates oxidative stress, which in turn triggers inflammation that can appear as sunburn, with symptoms such as redness and blistering.
According to background data from the American Cancer Society and other public health agencies, millions of skin cancer cases are diagnosed in the United States each year, and a large proportion are linked to UV exposure. However, the specific molecular pathways that connect UV‑induced inflammation to cancer development have remained only partly understood.
In the new study, led by Yu‑Ying He, PhD, a professor of medicine in dermatology at the University of Chicago, scientists investigated how UV‑induced inflammation is controlled at the RNA level. The team focused on YTHDF2, a protein that recognizes RNA molecules carrying N6‑methyladenosine (m6A) modifications and helps regulate their stability and activity.
Using human skin cells and mouse models, the researchers found that UVB exposure reduces YTHDF2 activity by inducing its dephosphorylation and autophagic degradation. When YTHDF2 is lost or depleted, inflammatory responses to UVB become markedly stronger, according to the Nature Communications paper and a University of Chicago Medicine summary.
"When we removed YTHDF2 from skin cells, we saw that UV‑triggered inflammation was much worse," He said in a statement released by UChicago Medicine. "This suggests that the YTHDF2 protein plays a key role in suppressing inflammatory responses."
Further experiments showed that YTHDF2 binds to a non‑coding RNA known as U6, a small nuclear RNA (snRNA) that carries m6A modifications. The study reports that, under UV stress, levels of U6 increase and this RNA can bind to toll‑like receptor 3 (TLR3), an immune sensor that activates inflammatory pathways linked to tumor formation.
The researchers found that these interactions occur within endosomes, cellular compartments not typically associated with U6 snRNA. The team identified SIDT2, a transmembrane protein, as responsible for transporting U6 into endosomes, where both U6 and YTHDF2 are present.
"We spent a lot of time figuring out how these non‑coding RNAs get to the endosome, since that’s not where they usually reside," He explained in the UChicago Medicine article. "For the first time, we showed that a protein called SDT2 transports U6 into the endosome, and YTHDF2 travels with it." The underlying research paper identifies this transporter as SIDT2, a known endosomal membrane protein.
Once in the endosome, YTHDF2 normally promotes decay of m6A‑modified U6 and blocks its ability to activate TLR3. In the absence of YTHDF2—such as after UVB‑induced inhibition of the protein—U6 more readily engages TLR3, driving heightened inflammatory signaling.
In mouse experiments, skin‑specific deletion of Ythdf2 increased UVB‑induced skin inflammation and promoted tumor initiation, supporting a role for YTHDF2 in suppressing UV‑driven skin cancer development.
The research, titled "YTHDF2 regulates self non‑coding RNA metabolism to control inflammation and tumorigenesis," was published in Nature Communications. According to the University of Chicago Medicine, the work was supported by grants from the National Institutes of Health, the University of Chicago Medicine Comprehensive Cancer Center, the ChicAgo Center for Health and EnvironmenT (CACHET), and the University of Chicago Friends of Dermatology Endowment Fund. The authors say the findings open potential avenues for therapies that target RNA–protein interactions regulating inflammation to help prevent or treat UV‑associated skin cancer.