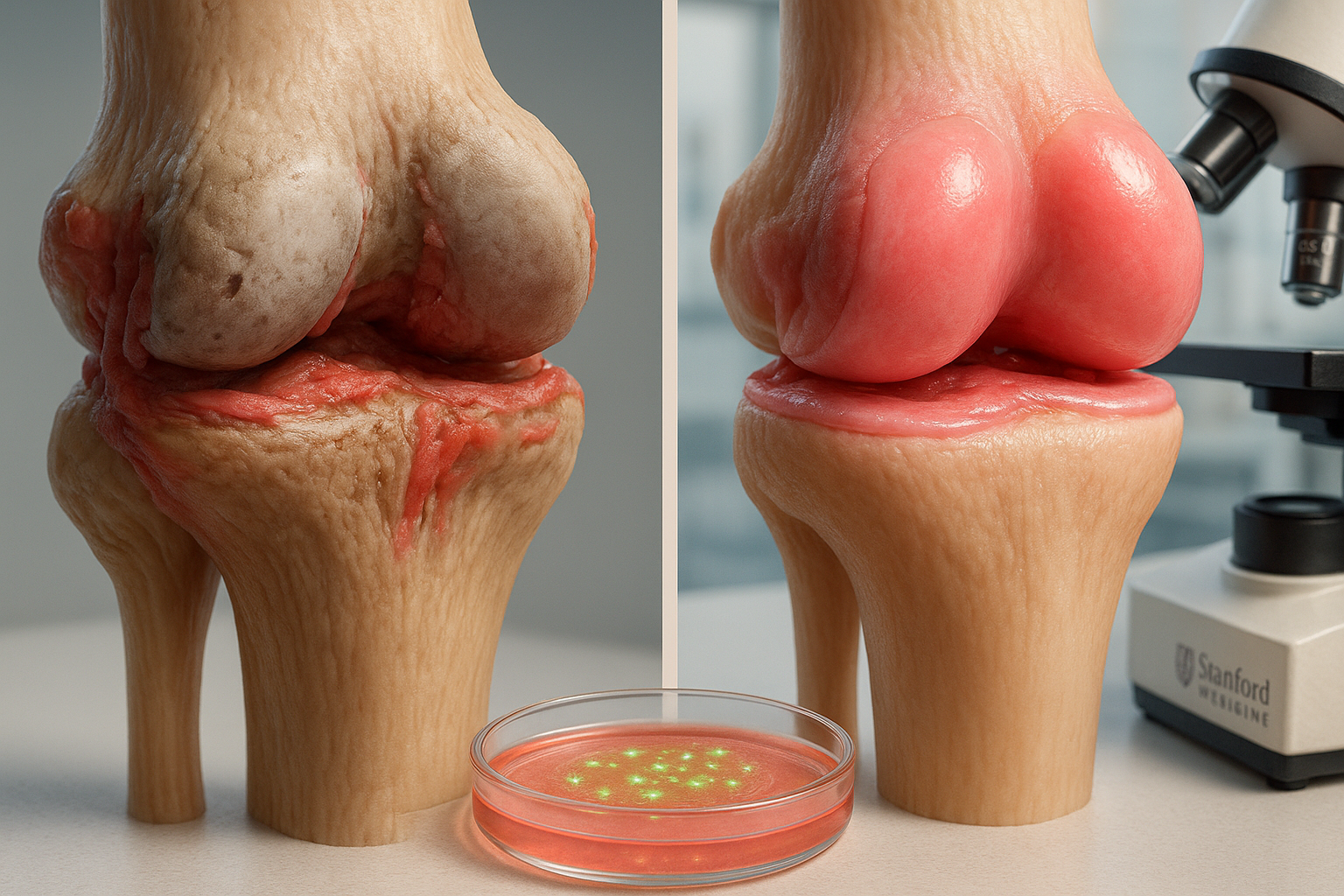
Peneliti di ETH Zurich melaporkan bahwa faktor induksibel hipoksia 1 (HIF1) dapat secara aktif mendorong perubahan tendon yang merugikan terkait kondisi seperti nyeri tendon Achilles dan siku tenis. Dalam model tikus dan sel tendon manusia yang dikumpulkan selama operasi, HIF1 yang meningkat dikaitkan dengan pemodelan ulang patologis yang membuat jaringan tendon lebih rapuh dan disertai pertumbuhan neurovaskular yang mungkin membantu menjelaskan nyeri.
Tendinopati —istilah payung yang digunakan dokter untuk gangguan tendon kronis dan menyakitkan— mencakup nyeri tendon Achilles, siku tenis, bahu perenang, dan lutut penjumper. Kondisi ini dapat memengaruhi atlet muda maupun orang dewasa tua, dan sering dikaitkan dengan ketegangan dan beban berulang. nn“Tendon pada dasarnya rentan terhadap penggunaan berlebih,” kata Jess Snedeker, profesor biomekanik ortopedi di ETH Zurich dan Rumah Sakit Universitas Balgrist di Zurich. Snedeker mencatat bahwa tendon harus mentransmisikan gaya otot tinggi melalui struktur jaringan ikat yang relatif tipis. nnDalam studi yang diterbitkan di Science Translational Medicine, Snedeker dan Katrien De Bock, profesor olahraga dan kesehatan di ETH Zurich, serta rekan-rekannya fokus pada faktor induksibel hipoksia 1 (HIF1), kompleks protein yang terlibat dalam respons seluler terhadap oksigen rendah. Bagian dari HIF1 berfungsi sebagai faktor transkripsi yang mengatur aktivitas gen. nnPenelitian sebelumnya melaporkan HIF1 yang meningkat pada tendon yang sakit, tetapi tidak jelas apakah itu hanya terkait dengan cedera atau berkontribusi langsung pada penyakit. Tim ETH Zurich melaporkan bukti yang mendukung peran kausal: dalam eksperimen tikus, hewan dengan HIF1 yang diaktifkan secara persisten mengembangkan penyakit tendon bahkan tanpa ketegangan mekanis berlebih, sementara menonaktifkan HIF1 pada jaringan tendon melindungi tikus dari mengembangkan penyakit tendon bahkan ketika tendon kelebihan beban. nnPeneliti juga menganalisis sel tendon manusia yang diperoleh selama operasi tendon. Mereka melaporkan bahwa aktivitas HIF1 yang lebih tinggi bertepatan dengan perubahan struktural pada jaringan tendon, termasuk peningkatan ikatan silang dalam serat kolagen. nn“Ini membuat tendon lebih rapuh dan merusak fungsi mekanisnya,” kata Greta Moschini, mahasiswa doktoral di kelompok De Bock dan Snedeker serta penulis utama studi. Tim juga mengamati peningkatan pertumbuhan pembuluh darah dan saraf ke dalam jaringan tendon; Moschini mengatakan pertumbuhan neurovaskular ini “bisa menjadi penjelasan untuk nyeri yang umum diamati pada tendinopati.” nnSnedeker mengatakan temuan ini menekankan pentingnya menangani masalah tendon sejak dini, terutama pada atlet muda. Ia mengatakan kerusakan yang terkait dengan aktivitas HIF1 dapat terakumulasi dan, seiring waktu, menjadi ireversibel—pada titik itu fisioterapi mungkin tidak lagi membantu dan pengangkatan jaringan tendon yang sakit secara bedah mungkin menjadi opsi yang tersisa. nnDe Bock memperingatkan bahwa mematikan HIF1 secara langsung di seluruh tubuh bisa menyebabkan efek samping karena perannya yang lebih luas dalam mendeteksi oksigen. Sebaliknya, para peneliti mengatakan mereka sedang mengeksplorasi jalur molekuler hilir HIF1 untuk mengidentifikasi pendekatan yang lebih tertarget yang bisa lebih aman untuk mengobati tendinopati.