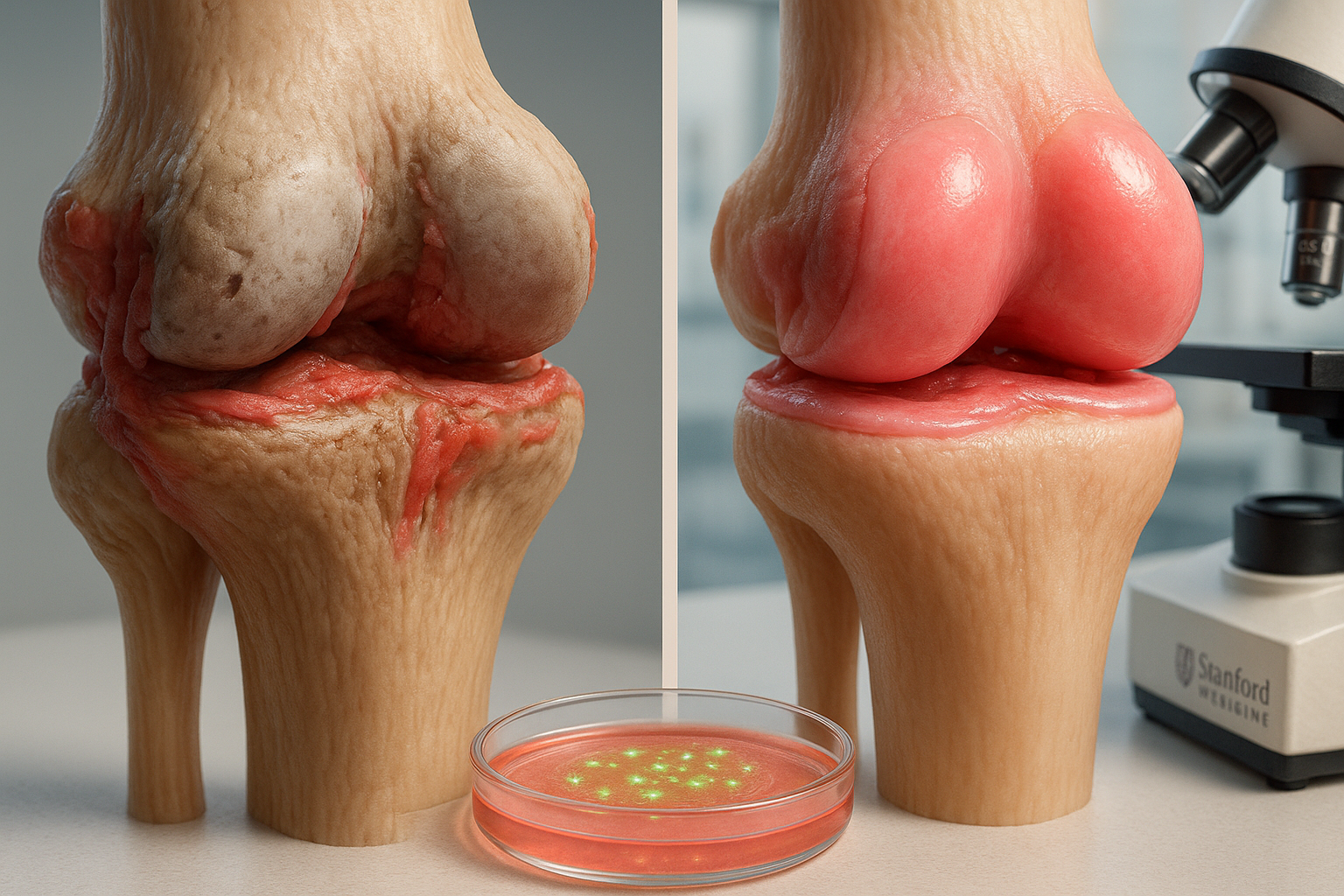
Peneliti Stanford Medicine melaporkan bahwa memblokir enzim 15-PGDH membalikkan kehilangan tulang rawan terkait usia pada tikus tua dan mengurangi kerusakan seperti osteoarthritis setelah cedera lutut mirip ACL. Dalam eksperimen lab, tulang rawan dari operasi penggantian lutut juga menunjukkan tanda-tanda regenerasi awal setelah terpapar inhibitor, temuan yang diterbitkan di *Science*.
Osteoarthritis memengaruhi sekitar satu dari lima orang dewasa di Amerika Serikat dan terkait dengan biaya perawatan kesehatan langsung sekitar 65 miliar dolar AS per tahun, menurut ringkasan Stanford Medicine. Perawatan saat ini sebagian besar fokus pada bantuan gejala atau penggantian sendi bedah, dan tidak ada obat yang disetujui yang dapat memperlambat atau membalikkan kerusakan tulang rawan mendasar. Dalam studi yang diterbitkan di Science, ilmuwan Stanford Medicine fokus pada 15-hidroksi prostaglandin dehidrogenase (15-PGDH), enzim yang mereka gambarkan sebagai “gerozim” karena kadarnya meningkat seiring usia. Tim melaporkan bahwa kadar 15-PGDH meningkat pada tulang rawan artikular tikus tua dan tikus dengan cedera sendi, dan bahwa menghambat enzim mengubah perilaku sel tulang rawan dengan cara yang konsisten dengan perbaikan. Pada tikus tua, peneliti menemukan bahwa pengobatan dengan inhibitor 15-PGDH molekul kecil—diberikan secara sistemik atau disuntik ke lutut—mengentalkan tulang rawan di seluruh permukaan sendi. Tes menunjukkan jaringan baru adalah tulang rawan hialin (artikular), bukan fibrokartilago, yang biasanya kurang fungsional. Inhibitor yang sama juga mengurangi perkembangan osteoarthritis dalam model tikus cedera lutut yang menyerupai robekan ACL. Studi melaporkan bahwa tikus yang diobati dua kali seminggu selama empat minggu setelah cedera kurang mungkin mengembangkan osteoarthritis dan menunjukkan gerakan serta penahan beban yang lebih baik pada anggota tubuh yang cedera daripada hewan yang tidak diobati. Peneliti juga menguji tulang rawan manusia dari pasien yang menjalani penggantian lutut total untuk osteoarthritis. Setelah seminggu paparan inhibitor di lab, jaringan menunjukkan sel penghasil 15-PGDH lebih sedikit, ekspresi gen yang terkait dengan kerusakan tulang rawan dan fibrokartilago lebih rendah, dan tanda-tanda awal yang konsisten dengan regenerasi tulang rawan artikular. Studi menunjukkan perbaikan tulang rawan terjadi tanpa mengaktifkan sel punca. Sebaliknya, analisis menunjukkan bahwa sel tulang rawan yang ada (kondrosit) mengubah program ekspresi gen mereka menuju keadaan yang lebih muda dan memproduksi matriks. “Ini adalah cara baru untuk meregenerasi jaringan dewasa, dan memiliki janji klinis signifikan untuk mengobati arthritis akibat penuaan atau cedera,” kata penulis senior Helen Blau, profesor mikrobiologi dan imunologi Stanford, dalam rilis Stanford Medicine. Penulis co-senior Nidhi Bhutani, profesor associate bedah ortopedi Stanford, mengatakan inhibitor tersebut “menyebabkan regenerasi tulang rawan yang dramatis.” Peneliti mencatat bahwa inhibitor 15-PGDH oral sudah dievaluasi dalam pengujian klinis Fase 1 yang ditargetkan pada kelemahan otot terkait usia, dan mereka berharap uji coba manusia serupa akan diluncurkan untuk menguji regenerasi tulang rawan.