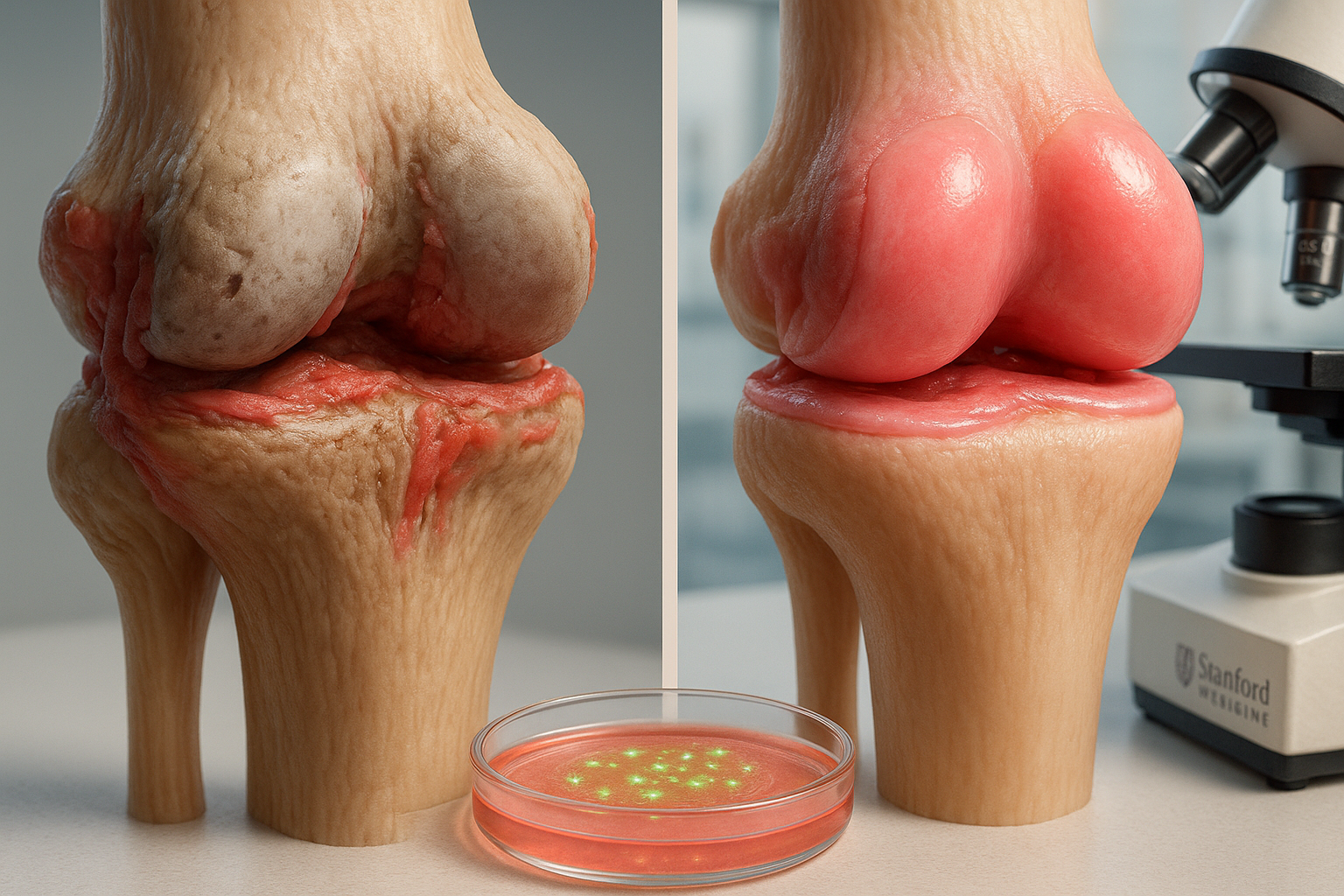
Des chercheurs de Stanford Medicine rapportent que le blocage de l'enzyme 15-PGDH a inversé la perte de cartilage liée à l'âge chez des souris âgées et réduit les dommages similaires à l'arthrose après des lésions du genou de type ACL. Dans des expériences en laboratoire, du cartilage prélevé lors d'opérations de prothèse de genou a également montré des signes précoces de régénération après exposition à l'inhibiteur, résultats publiés dans *Science*.
L'arthrose touche environ un adulte sur cinq aux États-Unis et est associée à des coûts de soins de santé directs estimés à 65 milliards de dollars par an, selon le résumé de Stanford Medicine. Les soins actuels se concentrent principalement sur le soulagement des symptômes ou le remplacement chirurgical des articulations, et il n'existe aucun médicament approuvé capable de ralentir ou d'inverser les dommages sous-jacents au cartilage. Dans une étude publiée dans Science, des scientifiques de Stanford Medicine se sont concentrés sur la 15-hydroxy prostaglandine déshydrogénase (15-PGDH), une enzyme qu'ils décrivent comme un «gérozyme» car ses niveaux augmentent avec l'âge. L'équipe a rapporté que les niveaux de 15-PGDH ont augmenté dans le cartilage articulaire de souris âgées et de souris ayant subi des lésions articulaires, et que l'inhibition de l'enzyme a modifié le comportement des cellules du cartilage de manière cohérente avec une réparation. Chez des souris âgées, les chercheurs ont constaté que le traitement par un inhibiteur de 15-PGDH à petite molécule —administré de manière systémique ou injecté dans le genou— a épaissi le cartilage sur toute la surface de l'articulation. Les tests ont indiqué que le nouveau tissu était du cartilage hyalin (articulaire), plutôt que du fibrocartilage, qui est généralement moins fonctionnel. Le même inhibiteur a également réduit le développement de l'arthrose dans un modèle de souris de lésion du genou ressemblant à une déchirure du LCA. L'étude a rapporté que les souris traitées deux fois par semaine pendant quatre semaines après la lésion étaient moins susceptibles de développer une arthrose et présentaient un meilleur mouvement et une meilleure capacité portante sur le membre lésé que les animaux non traités. Les chercheurs ont également testé du cartilage humain prélevé chez des patients subissant une prothèse totale de genou pour arthrose. Après une semaine d'exposition à l'inhibiteur en laboratoire, le tissu a montré moins de cellules produisant 15-PGDH, une expression plus faible des gènes associés à la dégradation du cartilage et au fibrocartilage, et des signes précoces cohérents avec une régénération du cartilage articulaire. L'étude suggère que la réparation du cartilage s'est produite sans activer les cellules souches. Au lieu de cela, les analyses ont indiqué que les chondrocytes existants ont modifié leurs programmes d'expression génique vers un état plus jeune et producteur de matrice. «C'est une nouvelle façon de régénérer un tissu adulte, et elle a un potentiel clinique significatif pour traiter l'arthrite due au vieillissement ou à des blessures», a déclaré l'auteure principale Helen Blau, professeure de microbiologie et d'immunologie à Stanford, dans le communiqué de Stanford Medicine. La co-auteure principale Nidhi Bhutani, professeure associée de chirurgie orthopédique à Stanford, a déclaré que l'inhibiteur «provoque une régénération dramatique du cartilage». Les chercheurs ont noté qu'un inhibiteur oral de 15-PGDH est déjà évalué dans des essais cliniques de phase 1 visant la faiblesse musculaire liée à l'âge, et ils espèrent que des essais humains similaires seront lancés pour tester la régénération du cartilage.