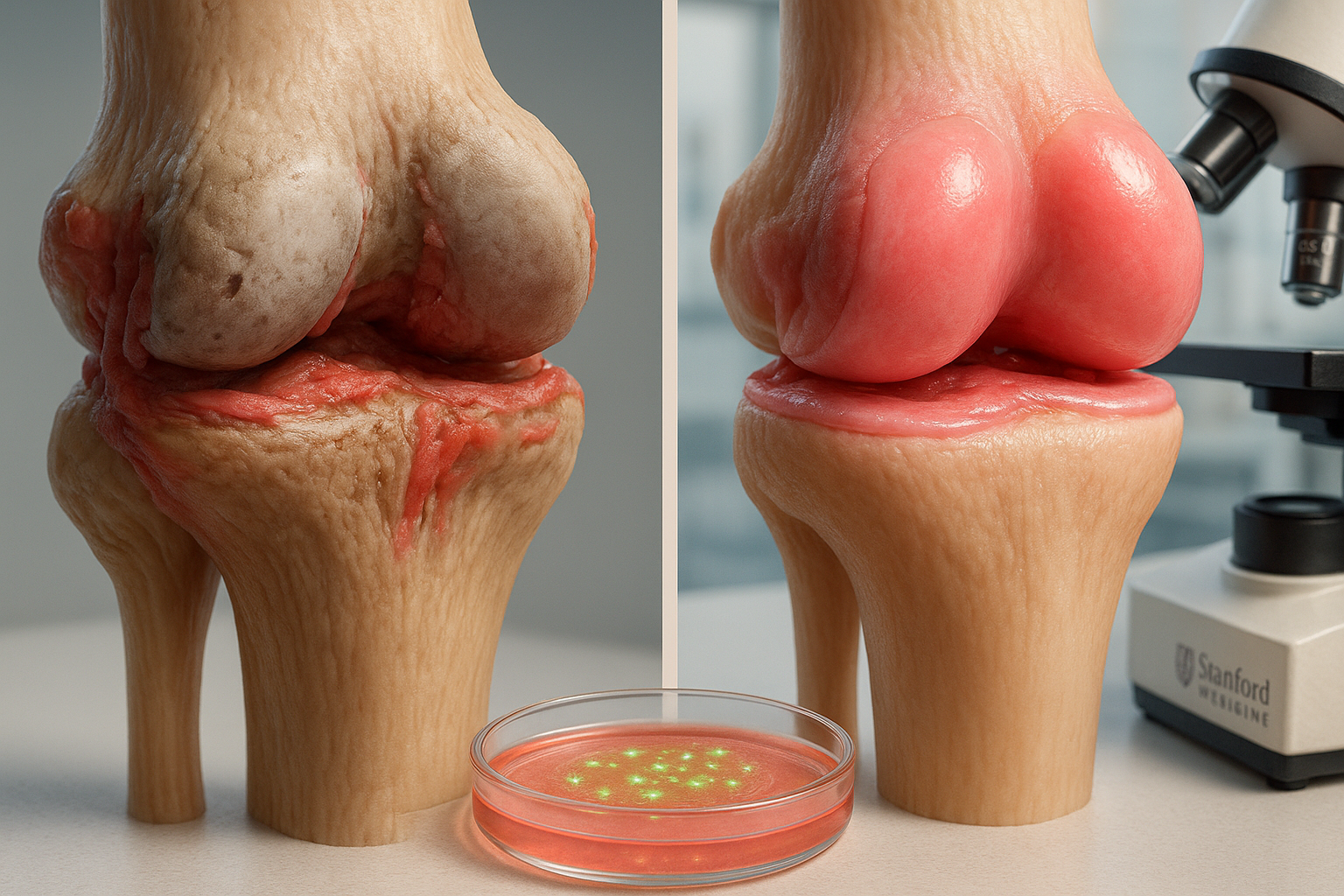
Forskare vid Stanford Medicine rapporterar att blockering av enzymet 15-PGDH vände åldersrelaterad broskförlust hos äldre möss och minskade artrosliknande skador efter knäskador liknande ACL. I labbexperiment visade brosk från knäprotesoperationer också tidiga tecken på regeneration efter exponering för hämmaren, fynd publicerade i *Science*.
Artros drabbar cirka en av fem vuxna i USA och är förknippat med uppskattade 65 miljarder dollar per år i direkta sjukvårdskostnader, enligt Stanford Medicines sammanfattning. Nuvarande vård fokuserar främst på symtomlindring eller kirurgiskt ledbyte, och det finns inga godkända läkemedel som kan bromsa eller vända den underliggande broskskadan. I en studie publicerad i Science fokuserade forskare vid Stanford Medicine på 15-hydroxiprostaglandin dehydrogenas (15-PGDH), ett enzym de beskriver som en ”gerozym” eftersom nivåerna stiger med åldern. Teamet rapporterade att 15-PGDH-nivåer ökade i ledbrusk hos åldrande möss och möss med ledskador, och att hämning av enzymet ändrade broskcellers beteende på sätt förenliga med reparation. Hos äldre möss fann forskarna att behandling med en småmolekyl 15-PGDH-hämmare – given systemiskt eller injicerat i knäet – förtjockade brosket över ledytan. Tester visade att nytt vävnad var hyalin (led-)brosk, snarare än fibrobrusk som vanligtvis är mindre funktionellt. Samma hämmare minskade också artrosutveckling i en mössmodell av knäskada liknande ACL-ruptur. Studien rapporterade att möss behandlade två gånger i veckan i fyra veckor efter skada var mindre benägna att utveckla artros och visade bättre rörelse och viktbärning på det skadade benet än obehandlade djur. Forskarna testade också människobrosk från patienter som genomgick total knäprotes för artros. Efter en veckas exponering för hämmaren i labb visade vävnaden färre 15-PGDH-producerande celler, lägre uttryck av gener associerade med brosknedbrytning och fibrobrusk, samt tidiga tecken förenliga med ledbruskregeneration. Studien tyder på att broskreparation skedde utan att aktivera stamceller. Istället indikerade analyser att befintliga broskceller (kondrocyter) skiftade sina genuttryckprogram mot ett mer ungdomligt, matrixproducerande tillstånd. ”Detta är ett nytt sätt att regenerera vuxen vävnad, och det har betydande klinisk potential för behandling av artros orsakad av åldrande eller skada”, säger huvudförfattaren Helen Blau, professor i mikrobiologi och immunologi vid Stanford, i Stanford Medicines pressmeddelande. Medhuvudförfattaren Nidhi Bhutani, docent i ortopedisk kirurgi vid Stanford, säger att hämmaren ”orsakar en dramatisk regeneration av brosk”. Forskarna noterade att en oral 15-PGDH-hämmare redan utvärderas i fas 1-kliniska prövningar mot åldersrelaterad muskelsvaghet, och de hoppas på liknande humana prövningar för att testa broskregeneration.