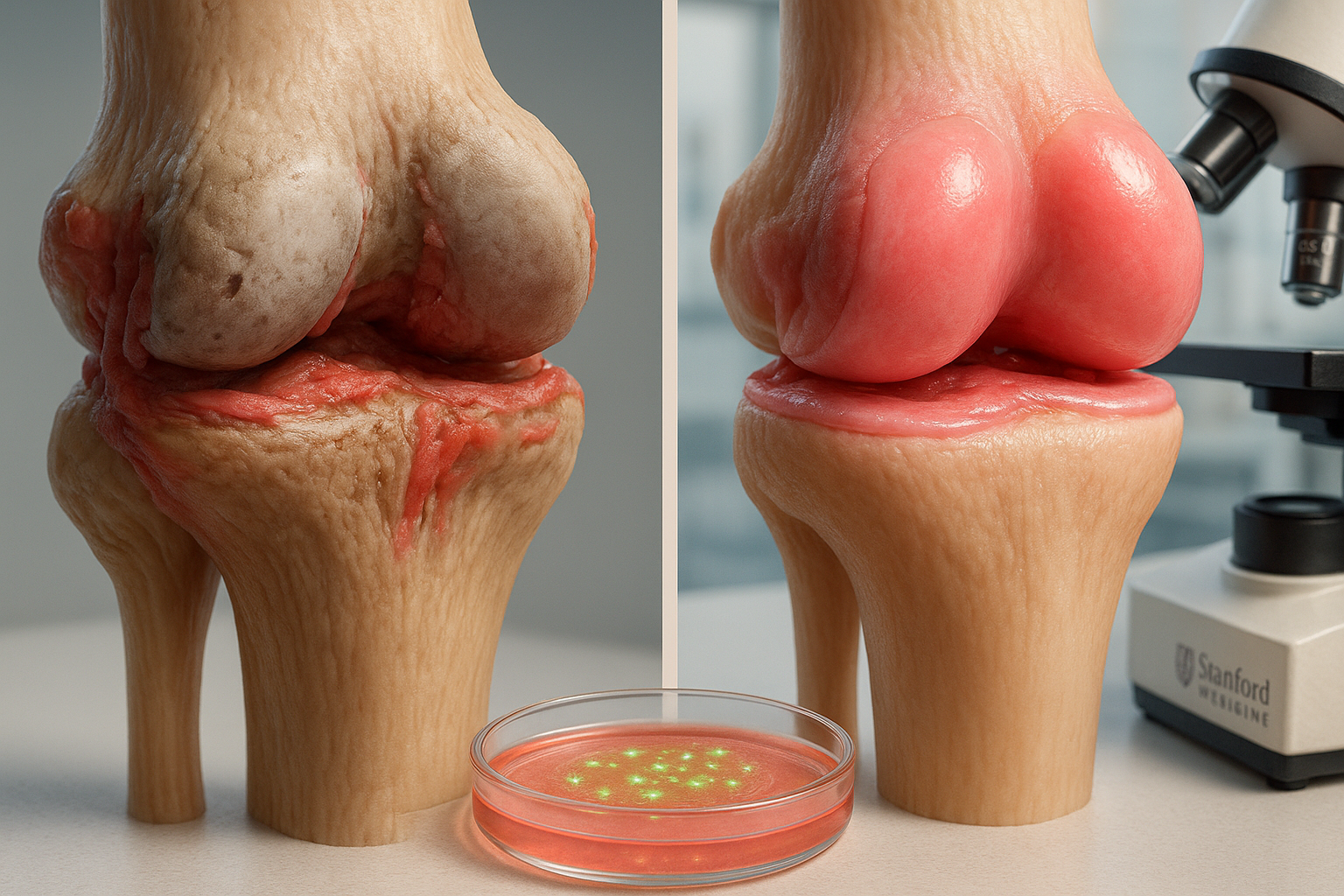
Des chercheurs de l’ETH Zurich rapportent que le facteur induisible par l’hypoxie 1 (HIF1) peut activement favoriser des changements préjudiciables des tendons liés à des affections telles que la douleur au tendon d’Achille et le tennis-elbow. Dans des modèles murins et dans des cellules de tendons humains prélevées lors d’interventions chirurgicales, un HIF1 élevé était associé à une remodelage pathologique rendant le tissu tendineux plus fragile et accompagné d’une ingrowth neurovasculaire qui pourrait expliquer la douleur.
Les tendinopathies — terme générique utilisé par les médecins pour désigner les troubles chroniques et douloureux des tendons — englobent la douleur au tendon d’Achille, le tennis-elbow, l’épaule du nageur et le genou du sauteur. Elles peuvent toucher aussi bien les jeunes athlètes que les adultes plus âgés, et sont souvent associées à des contraintes et des surcharges répétées. nn«Les tendons sont fondamentalement sensibles à une utilisation excessive», a déclaré Jess Snedeker, professeur de biomécanique orthopédique à l’ETH Zurich et à l’hôpital universitaire Balgrist à Zurich. Snedeker a noté que les tendons doivent transmettre des forces musculaires élevées à travers des structures de tissu conjonctif relativement minces. nnDans une étude publiée dans Science Translational Medicine, Snedeker et Katrien De Bock, professeure d’exercice et de santé à l’ETH Zurich, et leurs collègues se sont concentrés sur le facteur induisible par l’hypoxie 1 (HIF1), un complexe protéique impliqué dans les réponses cellulaires à un faible niveau d’oxygène. Une partie du HIF1 fonctionne comme un facteur de transcription qui régule l’activité génique. nnDes recherches antérieures avaient rapporté un HIF1 élevé dans les tendons malades, mais il n’était pas clair s’il était simplement associé à la lésion ou contribuait directement à la maladie. L’équipe de l’ETH Zurich a rapporté des preuves soutenant un rôle causal : dans des expériences sur des souris, les animaux avec un HIF1 activé de manière persistante ont développé une maladie tendineuse même sans contrainte mécanique excessive, tandis que la désactivation du HIF1 dans le tissu tendineux a protégé les souris contre le développement de la maladie tendineuse même lorsque les tendons étaient surchargés. nnLes chercheurs ont également analysé des cellules de tendons humains obtenues lors d’interventions chirurgicales sur les tendons. Ils ont rapporté qu’une activité HIF1 plus élevée coïncidait avec des changements structurels dans le tissu tendineux, y compris une augmentation des liaisons croisées au sein des fibres de collagène. nn«Cela rend les tendons plus fragiles et altère leur fonction mécanique», a déclaré Greta Moschini, doctorante dans les groupes de De Bock et Snedeker et auteure principale de l’étude. L’équipe a également observé une augmentation de la croissance de vaisseaux sanguins et de nerfs dans le tissu tendineux ; Moschini a indiqué que cette ingrowth neurovasculaire «pourrait être l’explication de la douleur couramment observée dans les tendinopathies». nnSnedeker a déclaré que ces résultats soulignent l’importance de traiter les problèmes tendineux précocement, en particulier chez les jeunes athlètes. Il a ajouté que les dommages liés à l’activité du HIF1 peuvent s’accumuler et devenir, avec le temps, irréversibles — point à partir duquel la physiothérapie peut ne plus aider et l’ablation chirurgicale du tissu tendineux malade peut être la seule option restante. nnDe Bock a mis en garde contre le fait d’éteindre directement le HIF1 dans tout le corps, ce qui pourrait entraîner des effets secondaires en raison de son rôle plus large dans la détection de l’oxygène. Au lieu de cela, les chercheurs ont indiqué qu’ils explorent les voies moléculaires en aval du HIF1 pour identifier des approches plus ciblées qui pourraient être plus sûres pour traiter les tendinopathies.