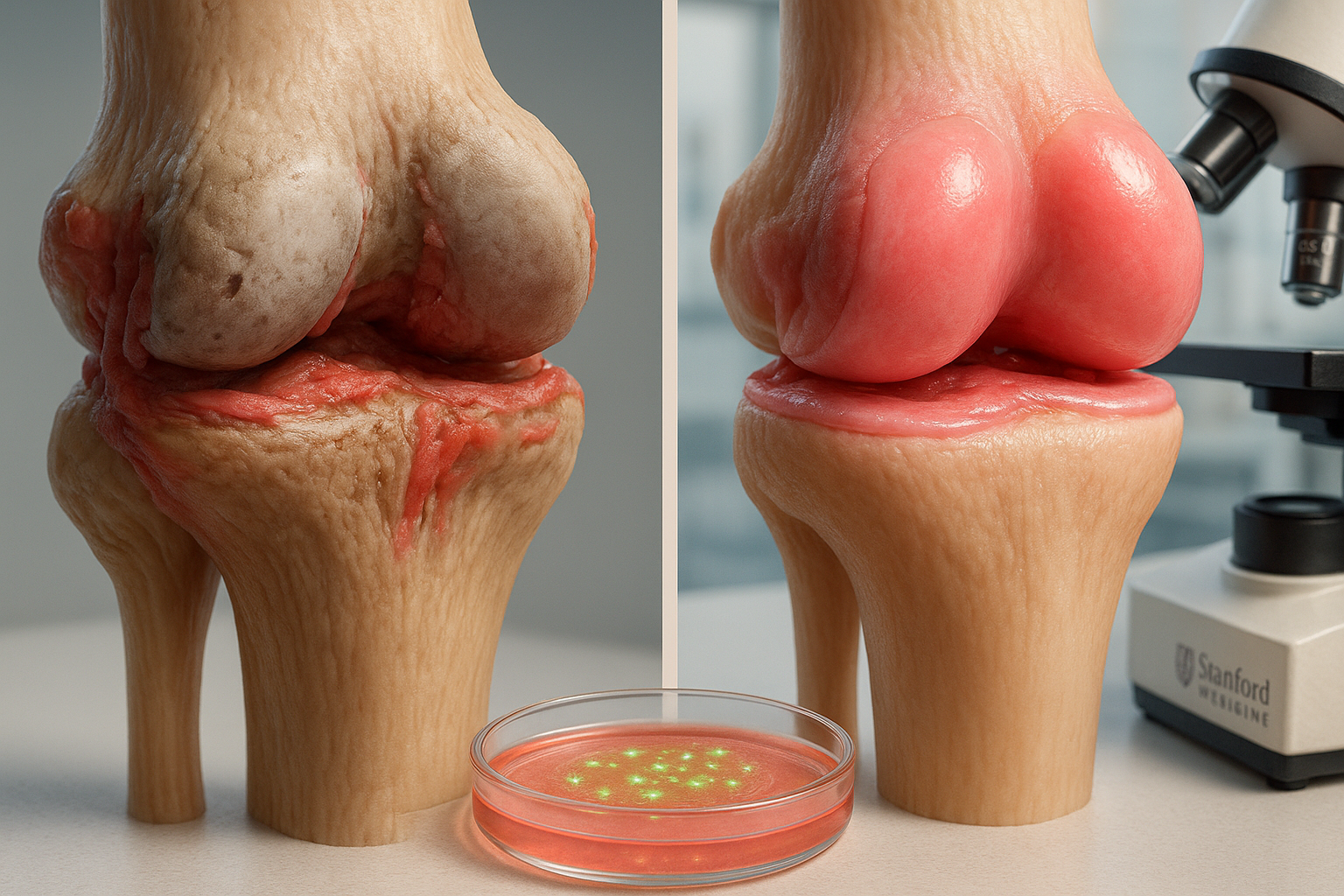
Pesquisadores da ETH Zurich relatam que o fator induzível por hipóxia 1 (HIF1) pode impulsionar ativamente mudanças prejudiciais nos tendões ligadas a condições como dor no tendão de Aquiles e cotovelo de tênis. Em modelos de camundongos e em células de tendões humanos coletadas durante cirurgias, o HIF1 elevado foi associado a remodelação patológica que tornou o tecido tendíneo mais frágil e foi acompanhado por crescimento neurovascular que pode ajudar a explicar a dor.
Tendinopatias — termo guarda-chuva usado por médicos para distúrbios crônicos e dolorosos dos tendões — incluem dor no tendão de Aquiles, cotovelo de tênis, ombro de nadador e joelho de saltador. Podem afetar tanto atletas jovens quanto adultos mais velhos, e frequentemente estão associadas a tensão e sobrecarga repetidas. nn«Os tendões são fundamentalmente suscetíveis ao uso excessivo», disse Jess Snedeker, professor de biomecânica ortopédica na ETH Zurich e no Hospital Universitário Balgrist em Zurique. Snedeker observou que os tendões devem transmitir forças musculares elevadas através de estruturas de tecido conjuntivo comparativamente finas. nnEm um estudo publicado em Science Translational Medicine, Snedeker e Katrien De Bock, professora de exercício e saúde na ETH Zurich, e seus colegas focaram no fator induzível por hipóxia 1 (HIF1), um complexo proteico envolvido nas respostas celulares a baixo oxigênio. Parte do HIF1 funciona como um fator de transcrição que regula a atividade gênica. nnPesquisas anteriores relataram HIF1 elevado em tendões doentes, mas não estava claro se era meramente associado à lesão ou contribuía diretamente para a doença. A equipe da ETH Zurich relatou evidências que apoiam um papel causal: em experimentos com camundongos, animais com HIF1 persistentemente ativado desenvolveram doença tendínea mesmo sem tensão mecânica excessiva, enquanto desativar o HIF1 no tecido tendíneo protegeu os camundongos de desenvolver doença tendínea mesmo quando os tendões estavam sobrecarregados. nnOs pesquisadores também analisaram células de tendões humanos obtidas durante cirurgias de tendões. Eles relataram que maior atividade de HIF1 coincidiu com mudanças estruturais no tecido tendíneo, incluindo aumento de ligações cruzadas dentro das fibras de colágeno. nn«Isso torna os tendões mais frágeis e prejudica sua função mecânica», disse Greta Moschini, estudante de doutorado nos grupos de De Bock e Snedeker e autora principal do estudo. A equipe também observou aumento no crescimento de vasos sanguíneos e nervos no tecido tendíneo; Moschini disse que esse crescimento neurovascular «pode ser a explicação para a dor comumente observada na tendinopatia». nnSnedeker disse que os achados sublinham a importância de abordar problemas tendíneos precocemente, particularmente em atletas jovens. Ele disse que danos ligados à atividade de HIF1 podem se acumular e, com o tempo, tornar-se irreversíveis — ponto em que a fisioterapia pode não ajudar mais e a remoção cirúrgica do tecido tendíneo doente pode ser a opção restante. nnDe Bock alertou que desligar diretamente o HIF1 em todo o corpo poderia causar efeitos colaterais devido ao seu papel mais amplo na detecção de oxigênio. Em vez disso, os pesquisadores disseram que estão explorando as vias moleculares downstream do HIF1 para identificar abordagens mais direcionadas que poderiam ser mais seguras para tratar tendinopatia.