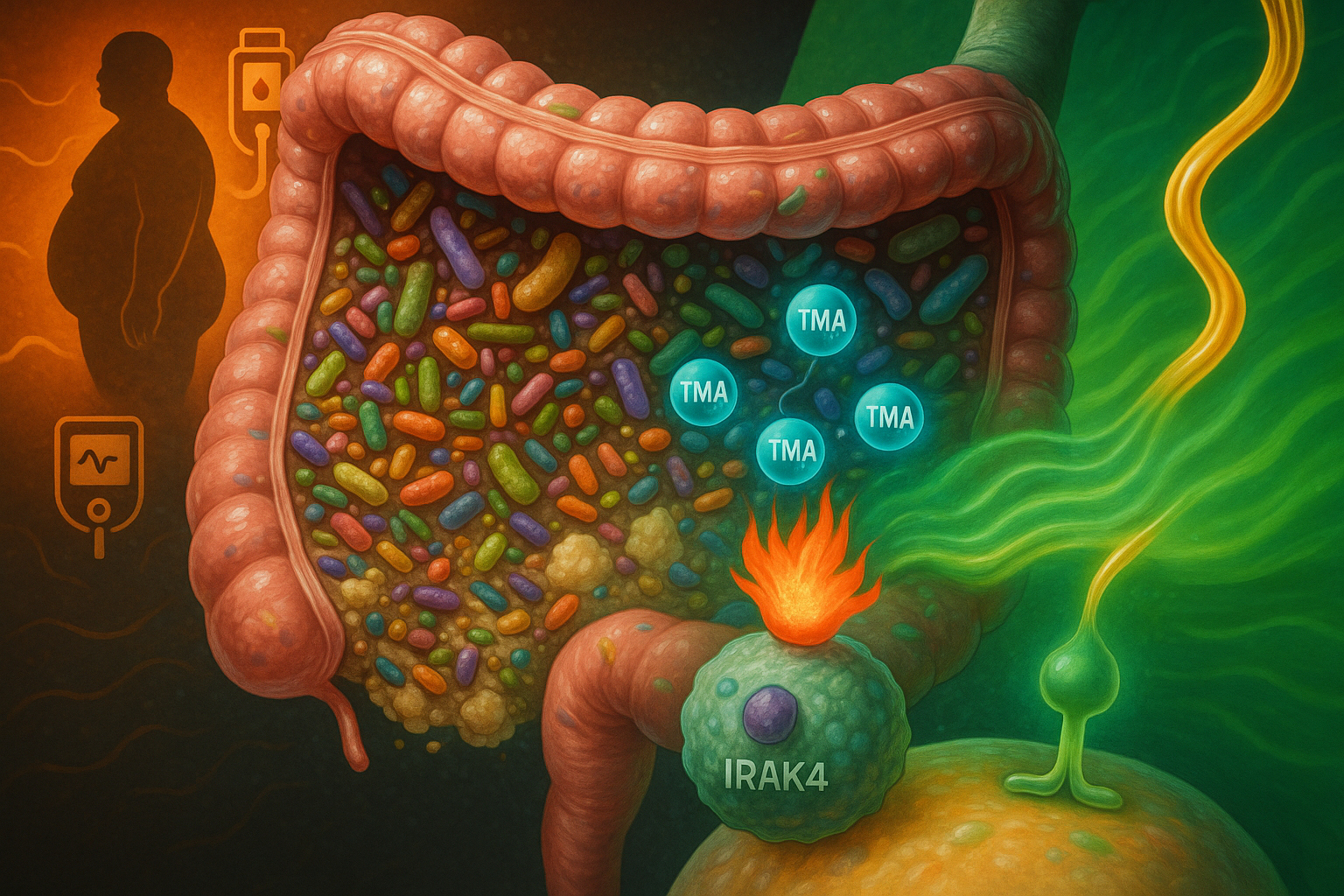
新たな研究で、化学療法による腸管内壁の損傷が予期せずマイクロバイオタを再構築し、がんの広がりに対する免疫防御を強化する化合物を作り出すことが明らかになった。このプロセスは免疫抑制細胞を減らし、特に肝臓での転移耐性を高める。患者データでは、この化合物の高レベルが大腸がん症例の生存率向上と関連している。
化学療法は、消化器系に深刻な副作用をもたらすことで悪名高いが、がんの進行を防ぐ予期せぬ利点がある可能性がある。研究によると、この治療は腸管内壁を損傷し、栄養素の利用可能性を乱し、腸内細菌の組成変化を引き起こす。 これらの変化は、トリプトファンというアミノ酸由来の代謝物であるインドール-3-プロピオン酸(IPA)の産生を増加させる。IPAは血流を通じて骨髄に運ばれ、免疫細胞の発達に影響を与える。具体的に、骨髄系造血を変化させ、通常がん細胞が検出を逃れ転移成長を促進する免疫抑制性単球の数を減少させる。 「化学療法の副作用としてしばしば付随的損傷と見なされるものが、こうした構造化された全身反応を引き起こすとは驚きでした。腸内マイクロバイオタを再構築することで、化学療法は免疫を再配線し、体を転移に対して許容しにくくする出来事の連鎖を起こします」と、研究の第一著者であるLudivine Bersier氏は述べた。 この免疫シフトはT細胞機能を強化し、潜在的な転移部位での相互作用を変化させ、特に肝臓で腫瘍の定着に抵抗的な環境を生み出す。前臨床モデルでこれらの効果が明確に示されている。 支援証拠は、日揮大学病院のThibaud Koessler博士との共同で収集した臨床データから得られた。大腸がん患者では、化学療法後のIPA高レベルが単球減少と良好な生存率と相関した。 「この研究は、化学療法の効果が腫瘍自体を超えて及ぶことを示しています。腸、骨髄、転移部位を結ぶ機能的軸を発見することで、転移進行を永続的に制限するための全身機構を強調します」と、責任著者のTatiana Petrova氏はコメントした。 スイス国立科学財団やスイス癌連盟などの組織から資金提供されたこの研究は、マイクロバイオタ由来代謝物の癌治療強化の可能性を提案する。2025年にNature Communicationsに掲載され、化学療法の長期抗転移効果を説明する腸-骨髄-肝臓軸を提唱している。