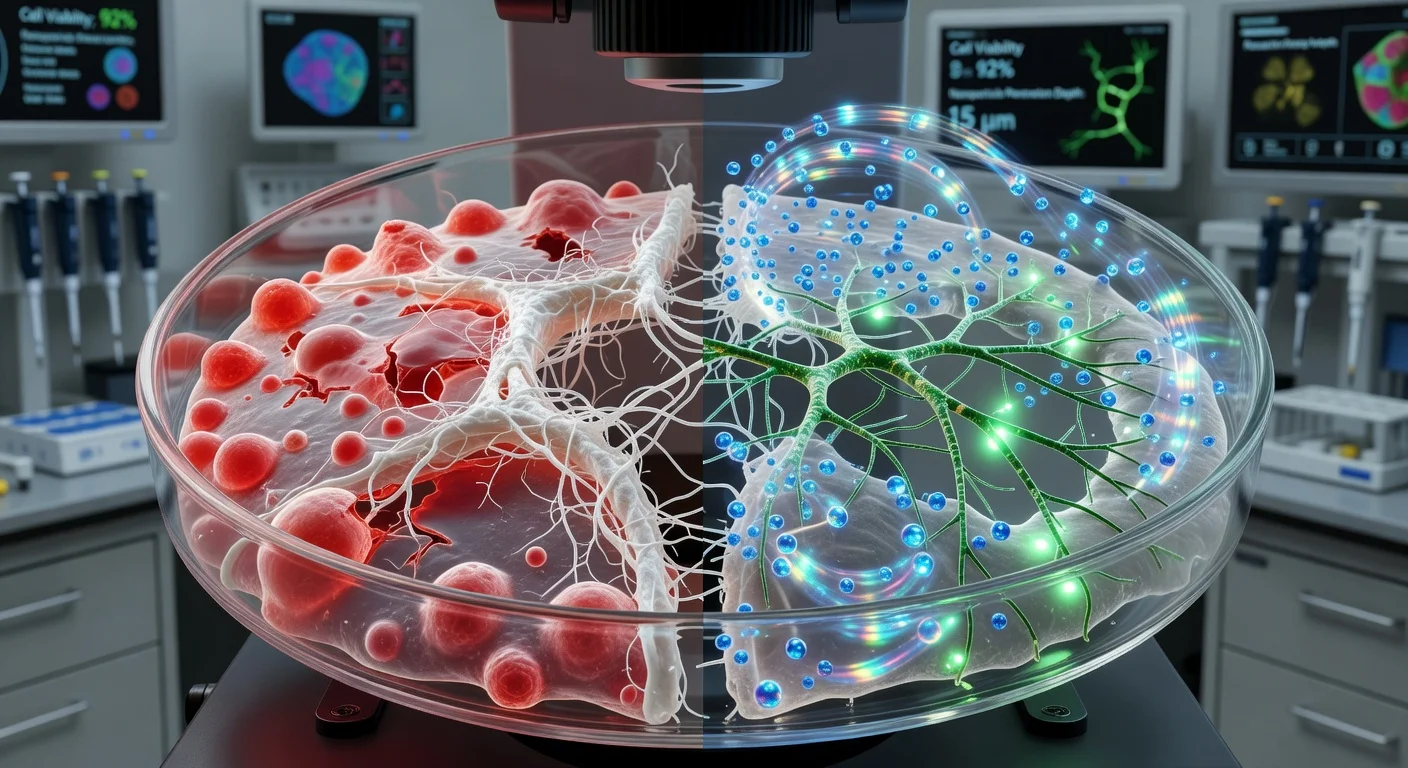
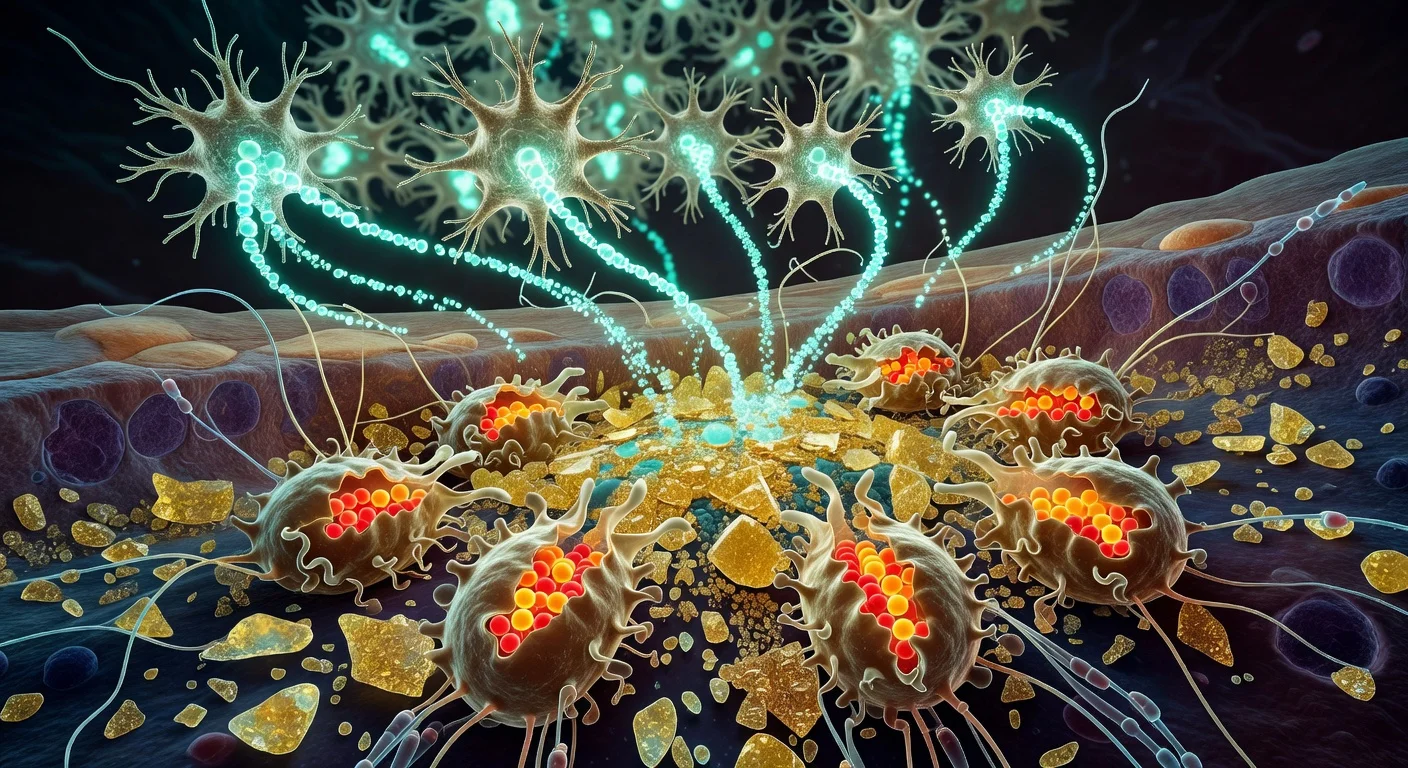
Northwestern大学の研究者らは、先進的なラボ培養人為脊髄オルガノイドモデルを開発し、外傷性損傷の主要特徴—炎症やグリア瘢痕化など—を再現し、実験的な「ダンシングモレキュール」療法がモデル内で瘢痕様組織を減少させ、神経繊維の成長を促進したと述べている。
Northwestern大学の科学者らは、高度に発達した人為脊髄オルガノイドを作成したと報告している。これは誘導多能性幹細胞(iPSCs)から培養した微小組織で、人間に似た組織での外傷性脊髄損傷をモデル化するよう設計されている。オルガノイドは数ミリメートルの大きさで、数ヶ月かけて神経細胞や星状膠細胞などの主要細胞種を含むように開発された。チームは中枢神経系の免疫細胞である微小膠細胞も組み込み、損傷後の炎症反応をより正確に捉えた。 大学と査読済み論文で記述された実験では、オルガノイドは脊髄外傷に関連するいくつかの生物学的特徴を再現した。細胞死、炎症、グリア瘢痕化を含む。異なる損傷形態をモデル化するため、研究者らは2つの損傷パターンを誘導した:裂傷型損傷を模倣するメス切り傷と、重い転倒や車両衝突でよく見られる打撲損傷を模倣する圧迫衝撃。 次に研究者らは、「ダンシングモレキュール」と呼ぶ実験的注射材をテストした。これは2021年に同じNorthwesternグループが最初に報告した超分子ナノファイバー基盤の療法である。液体として投与されゲル状ナノファイバー足場を形成する。この生物活性は、細胞受容体との相互作用を強化する可能性のある急速な分子運動によるものだとグループは述べている。 Northwesternによると、処理された損傷オルガノイドは未処理の損傷オルガノイドに比べて、ニュライト成長(軸索を含む神経細胞突起の成長)の増加、瘢痕様組織と炎症の減少を示した。「オルガノイドの最もエキサイティングな点の一つは、人間組織で新しい療法をテストできることだ」と、研究上級著者で「ダンシングモレキュール」プラットフォームの発明者であるSamuel I. Stuppは述べた。Stuppは、処理後グリア瘢痕が「大幅に薄れてほとんど検知不能になり」、ニュライトが動物で以前に見られた軸索再生に似たパターンで成長したと語った。 Northwesternは2021年に報告されたマウスでの先行前臨床研究も指摘した。重度脊髄損傷後24時間に単回注射が4週間以内の歩行回復と関連したという。大学はこの療法が米国FDAから急性脊髄損傷に対する希少疾病用医薬品指定を受けたと言っている。 オルガノイド損傷研究は2026年2月11日にNature Biomedical Engineeringに掲載された。StuppはNorthwesternの理事会信託教授で再生ナノメディシンセンター所長。論文第一著者はNorthwestern Feinberg医学校の医学研究助教授でセンター員のNozomu Takataである。結果はヒト由来組織での再生戦略評価に役立つ可能性を示唆するが、前臨床段階であり、患者での臨床効果を単独で証明するものではない。