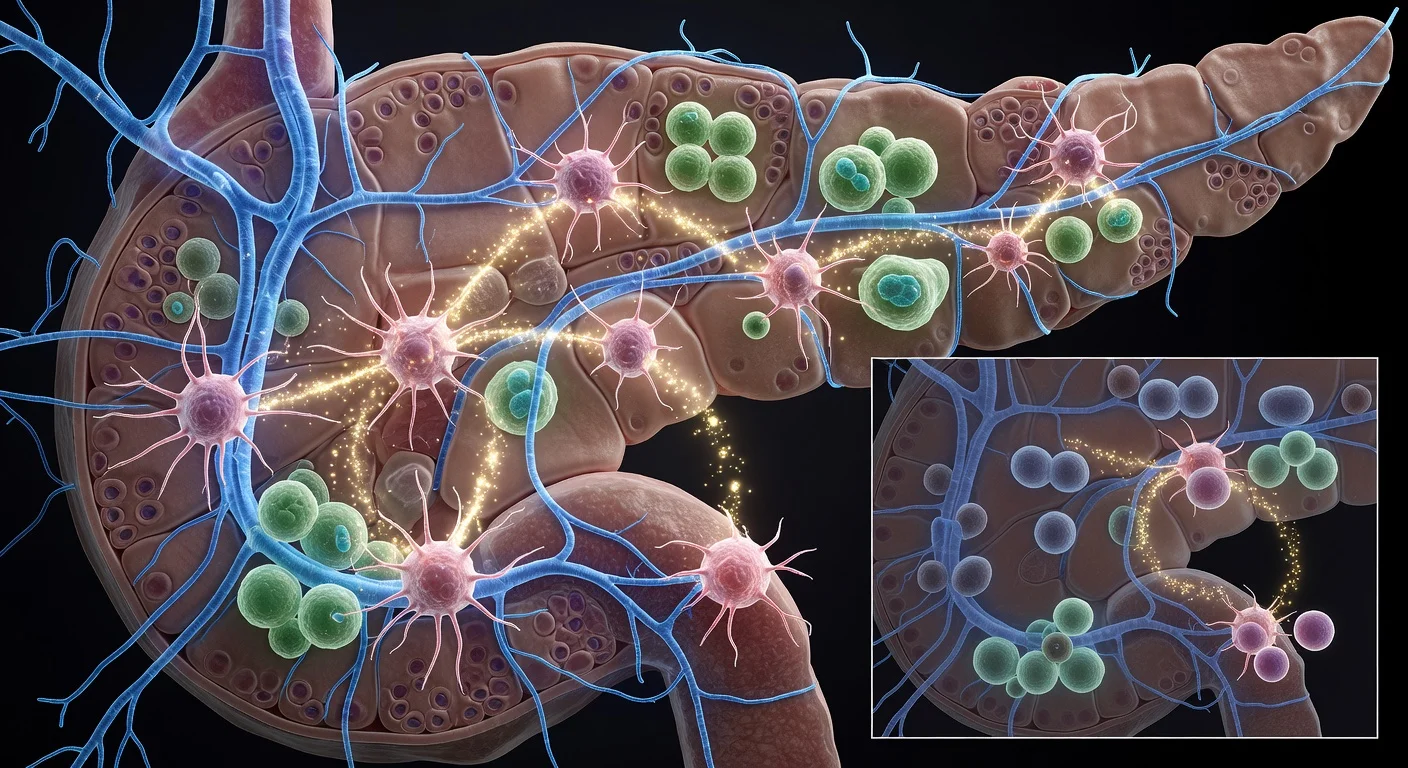
كشف باحثون في البرازيل كيف يستخدم سرطان البنكرياس بروتينًا يُدعى البيريوستين لغزو الأعصاب والانتشار مبكرًا. يفسر هذا الاكتشاف عدوانية المرض ويقترح أهدافًا علاجية جديدة. تشير النتائج، المنشورة في مجلة Molecular and Cellular Endocrinology، إلى قدرة الورم على إعادة تشكيل الأنسجة المحيطة.
يظل سرطان البنكرياس واحدًا من أكثر الأورام الخبيثة فتكًا، حيث تقارب معدل الوفيات معدل التشخيص. على المستوى العالمي، يحصد حوالي 510,000 حياة سنويًا من عدد مماثل تقريبًا من الحالات الجديدة. في البرازيل، يقدر المعهد الوطني للسرطان 11,000 تشخيص جديد و13,000 وفاة كل عام. النوع الأكثر شيوعًا، الغدي الخبيث، ينشأ في الخلايا الغدية ويمثل 90% من الحالات. دراسة بقيادة Carlos Alberto de Carvalho Fraga في مركز البحوث في الأمراض الالتهابية في ساو باولو تكشف أن الأورام لا تنتشر بشكل معزول. بدلاً من ذلك، تعيد برمجة الأنسجة الصحية القريبة باستخدام البيريوستين، الذي تنتجه الخلايا النجمية في البنكرياس. تعيد هذه البروتين تشكيل المصفوفة خارج الخلية، مما يمكن خلايا السرطان من غزو الأعصاب - عملية تُعرف بغزو العصب. «غزو العصب هو علامة على عدوانية السرطان»، يشرح الطبيب الأورامي Pedro Luiz Serrano Uson Junior، أحد المؤلفين. يسمح غزو العصب لخلايا السرطان بالسفر عبر مسارات الأعصاب، مما يسهل النقائل ويسبب ألمًا شديدًا. أكثر من نصف الحالات تظهر ذلك مبكرًا، غالبًا غير مكتشف حتى خزعة ما بعد الجراحة. يثير بيئة الورم أيضًا تفاعلًا نسيجيًا ليفيًا كثيفًا، يشكل حواجز ليفية كثيفة تعيق العلاج الكيميائي والمناعي. «لهذا السبب يظل سرطان البنكرياس صعب العلاج»، يلاحظ Uson. استخدم الباحث الرئيسي Helder Nakaya، أستاذ في جامعة ساو باولو، تحليلًا جينيًا متقدمًا على 24 عينة لرسم هذه العملية. «تمكنا من دمج بيانات من عشرات العينات بدقة فائقة القوة»، يقول Nakaya. ينجو فقط حوالي 10% من المرضى خمس سنوات بعد التشخيص. تشير البحوث إلى البيريوستين كأهداف واعدة. منعها أو الخلايا النجمية قد يمنع الغزو المبكر، متسقًا مع اتجاهات الطب الدقيق. التجارب السريرية لأجسام مضادة البيريوستين في سرطانات أخرى قد تخبر التطبيقات البنكرياسية. «يشير هذا العمل إلى مسارات قد توجه النهج المستقبلية لعلاج سرطان البنكرياس»، يختم Nakaya. يضيف Uson أن مثل هذه العلاجات يمكن أن تمتد إلى سرطان الثدي والأمعاء، حيث يحدث غزو العصب أيضًا.