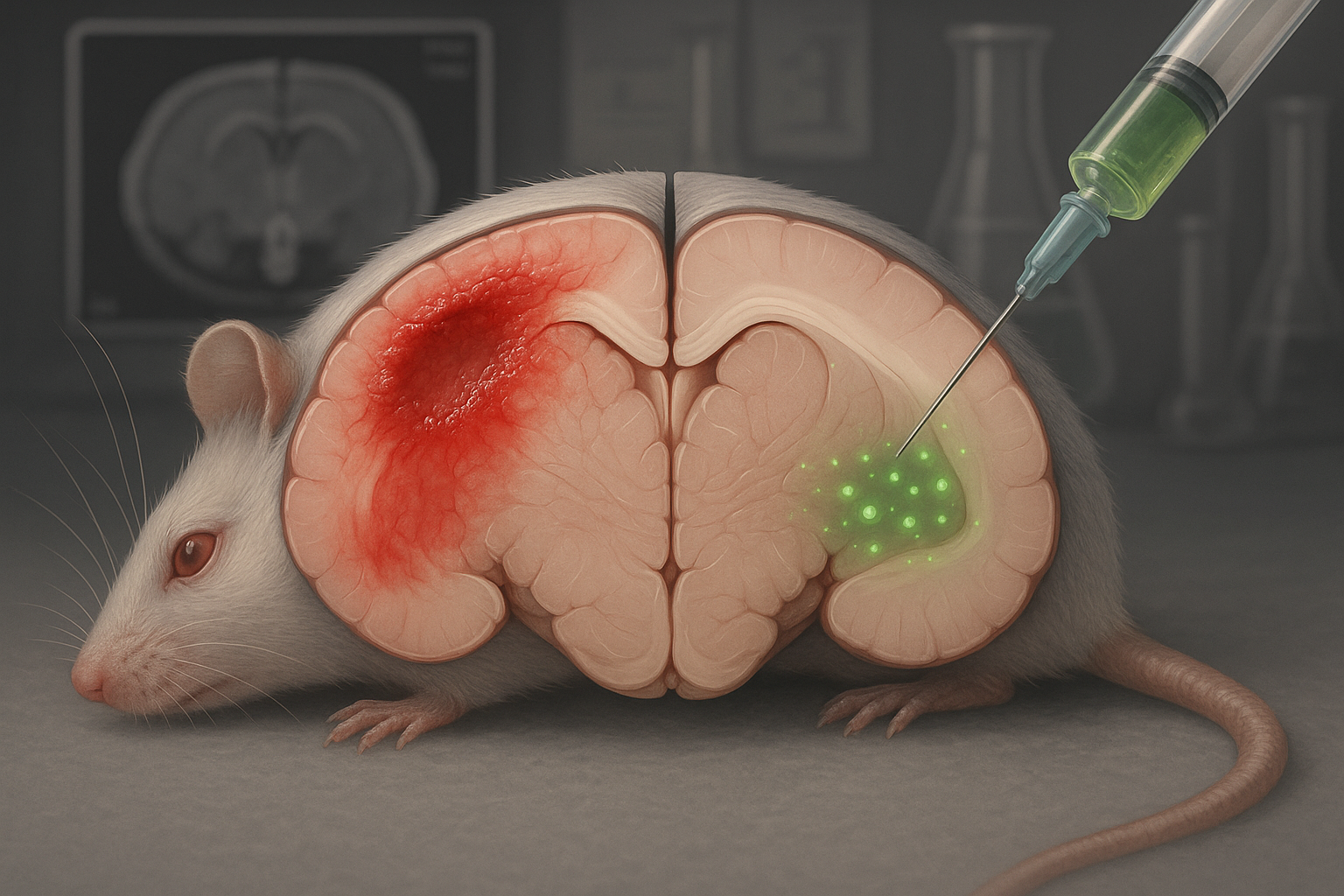
Des chercheurs rapportent qu’un tétrapeptide appelé CAQK, administré par voie intraveineuse après une lésion cérébrale traumatique, s’est accumulé dans les régions cérébrales endommagées et a été associé à une réduction de la taille des lésions et des signaux inflammatoires chez la souris, avec un ciblage similaire observé chez le porc. L’équipe et une startup associée indiquent qu’elles prévoient de demander l’autorisation de la FDA américaine pour lancer des tests humains précoces, bien qu’aucun calendrier n’ait été annoncé.
Une équipe de chercheurs issus de l’université et d’une entreprise startup a rapporté des résultats précliniques pour une thérapie potentielle de lésion cérébrale traumatique (TBI) construite autour d’un peptide extrêmement court, CAQK.
Dans une étude publiée dans EMBO Molecular Medicine en octobre 2025, les auteurs décrivent le CAQK comme un « tétrapeptide » neuroprotecteur (un peptide à quatre acides aminés) qui peut être administré par voie intraveineuse peu de temps après une lésion cérébrale modérée à sévère et qui s’accumule préférentiellement dans le tissu cérébral lésé dans des modèles animaux.
La TBI suit couramment des coups à la tête lors d’événements tels que des accidents de la route, des accidents du travail et des chutes. Les chercheurs citent une estimation d’incidence d’environ 200 cas pour 100 000 personnes par an. Ils notent également que les soins cliniques aigus se concentrent principalement sur la stabilisation des patients — comme le contrôle de la pression intracrânienne et le maintien du flux sanguin cérébral — et qu’il n’existe actuellement aucun médicament approuvé qui arrête directement les dommages initiaux liés à la lésion ou la cascade subséquente qui peut inclure inflammation et mort cellulaire.
Ce nouveau travail s’appuie sur une recherche antérieure publiée en 2016 qui a identifié le CAQK comme un peptide qui « cible » les sites de lésion cérébrale aiguë après administration systémique. Dans cette étude antérieure, le CAQK a été décrit comme se liant à des cibles dans la matrice extracellulaire surexprimées après la lésion et a été étudié comme moyen de délivrer des agents d’imagerie ou des charges thérapeutiques au tissu cérébral endommagé.
Dans l’étude de 2025, les auteurs ont testé le CAQK lui-même comme thérapie. Après une administration intraveineuse peu après la lésion, le peptide s’est accumulé dans les régions cérébrales endommagées chez la souris et le porc. L’équipe rapporte que le CAQK se lie à des composants riches en glycoprotéines et protéoglycanes de la matrice extracellulaire qui augmentent après la lésion.
Dans des expériences sur souris, les animaux traités avec CAQK présentaient des lésions plus petites que les témoins, avec des mesures cohérentes avec une réduction de la mort cellulaire et une expression plus faible de marqueurs inflammatoires dans le tissu lésé. Les chercheurs rapportent également des améliorations dans les tests comportementaux et de mémoire après traitement et indiquent qu’ils n’ont observé aucune toxicité évidente dans les conditions de l’étude.
Le premier auteur de l’étude, Aman P. Mann, a déclaré que l’équipe a observé « moins de mort cellulaire et une expression plus faible de marqueurs inflammatoires » dans la zone lésée et a rapporté de meilleurs résultats aux tests fonctionnels « sans toxicité évidente ». Le coauteur Pablo Scodeller a indiqué que la simplicité et la fabricabilité du peptide — ainsi que des attributs décrits par les chercheurs comme favorables à la pénétration tissulaire et à une faible immunogénéicité — en font un candidat prometteur pour un développement ultérieur.
Selon un rapport de ScienceDaily basé sur des documents du Consejo Superior de Investigaciones Científicas (CSIC), la startup AivoCode — liée aux auteurs de l’étude — prévoit de demander l’autorisation à la Food and Drug Administration américaine pour lancer des essais cliniques de phase I chez l’humain, bien que l’entreprise n’ait pas annoncé de calendrier.
Les résultats restent précliniques, et les auteurs soulignent que des études supplémentaires seraient nécessaires pour établir la sécurité, la posologie et l’efficacité chez l’humain.