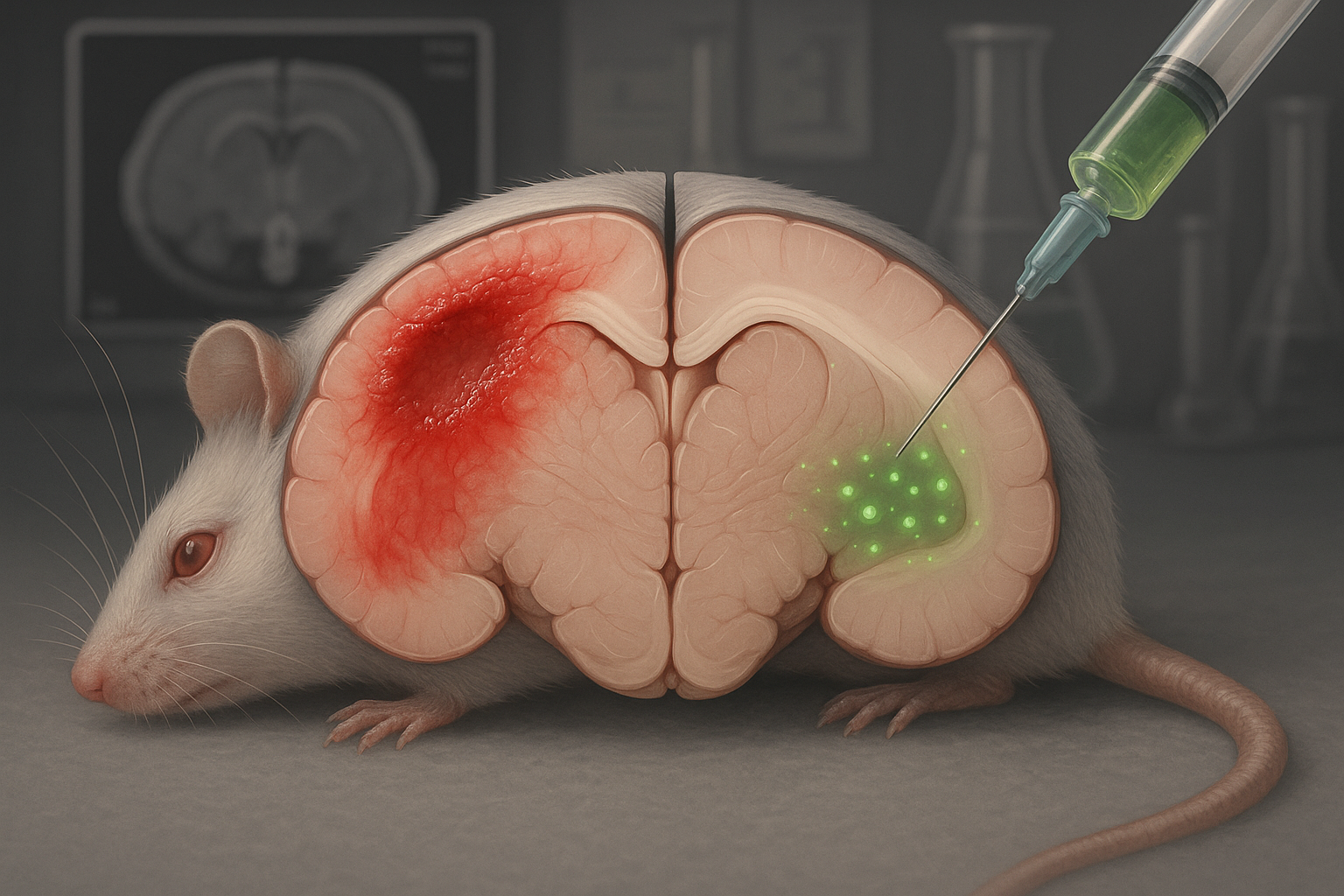
Forskare rapporterar att en tetrapeptid kallad CAQK, given intravenöst efter traumatisk hjärnskada, ackumulerades i skadade hjärnregioner och associerades med minskad lesionsstorlek och inflammatoriska signaler i möss, med liknande riktning sett i grisar. Teamet och ett relaterat startupföretag säger att de planerar att söka FDA-godkännande i USA för att påbörja tidiga humana tester, även om ingen tidslinje har annonserats.
Ett team av forskare från akademin och ett startupföretag har rapporterat prekliniska resultat för en potentiell terapi mot traumatisk hjärnskada (TBI) byggd kring en extremt kort peptid, CAQK.
I en studie publicerad i EMBO Molecular Medicine i oktober 2025 beskriver författarna CAQK som en neuroprotektiv "tetrapeptid" (en fyra-aminosyrors peptid) som kan ges intravenöst strax efter måttlig till svår hjärnskada och som preferentiellt ackumuleras i skadad hjärnvävnad i djurmodeller.
TBI följer vanligtvis slag mot huvudet i händelser som trafikolyckor, arbetsolyckor och fall. Forskare citerar en incidensuppskattning på cirka 200 fall per 100 000 personer per år. De noterar också att akut klinisk vård främst fokuserar på att stabilisera patienter — såsom att kontrollera intrakraniellt tryck och upprätthålla cerebralt blodflöde — och att det för närvarande inte finns några godkända läkemedel som direkt stoppar den initiala skaderelaterade skadan eller den efterföljande kaskaden som kan inkludera inflammation och celldöd.
Det nya arbetet bygger på tidigare forskning publicerad 2016 som identifierade CAQK som en peptid som "homing" till akuta hjärnskadesplatser efter systemisk administrering. I den tidigare studien beskrevs CAQK som bindande till mål i extracellulära matrisen som upregulateds efter skada och undersöktes som ett sätt att leverera bildgivande agens eller terapeutiska payloads till skadad hjärnvävnad.
I 2025-studien testade författarna CAQK självt som terapi. Efter intravenös dosering strax efter skada ackumulerades peptiden i skadade regioner av hjärnan hos både möss och grisar. Teamet rapporterar att CAQK binder glykoprotein- och proteoglykanrika komponenter i extracellulära matrisen som ökar efter skada.
I musexperiment hade djur behandlade med CAQK mindre lesioner än kontroller, tillsammans med mått som är förenliga med minskad celldöd och lägre uttryck av inflammatoriska markörer i skadat vävnad. Forskare rapporterar också förbättringar i beteende- och minnestester efter behandling och anger att de inte observerade någon uppenbar toxicitet under studiens förhållanden.
Studiens förstaförfattare, Aman P. Mann, sade att teamet såg "mindre celldöd och lägre uttryck av inflammatoriska markörer" i det skadade området och rapporterade förbättrade resultat i funktionella tester "utan uppenbar toxicitet". Medförfattaren Pablo Scodeller sade att peptidens enkelhet och tillverkningsbarhet — tillsammans med attribut som forskarna beskriver som gynnsamma för vävnadsgenomträngning och låg immunogenicitet — gör den till en lovande kandidat för vidare utveckling.
Enligt en ScienceDaily-rapport baserad på material från det spanska nationella forskningsrådet (CSIC) planerar startupen AivoCode — kopplad till studiens författare — att söka tillstånd från den amerikanska livsmedels- och läkemedelsmyndigheten för att påbörja fas I-kliniska prövningar på människor, även om företaget inte har annonserat någon tidslinje.
Resultaten förblir prekliniska, och författarna betonar att ytterligare studier skulle behövas för att fastställa säkerhet, dosering och effektivitet hos människor.