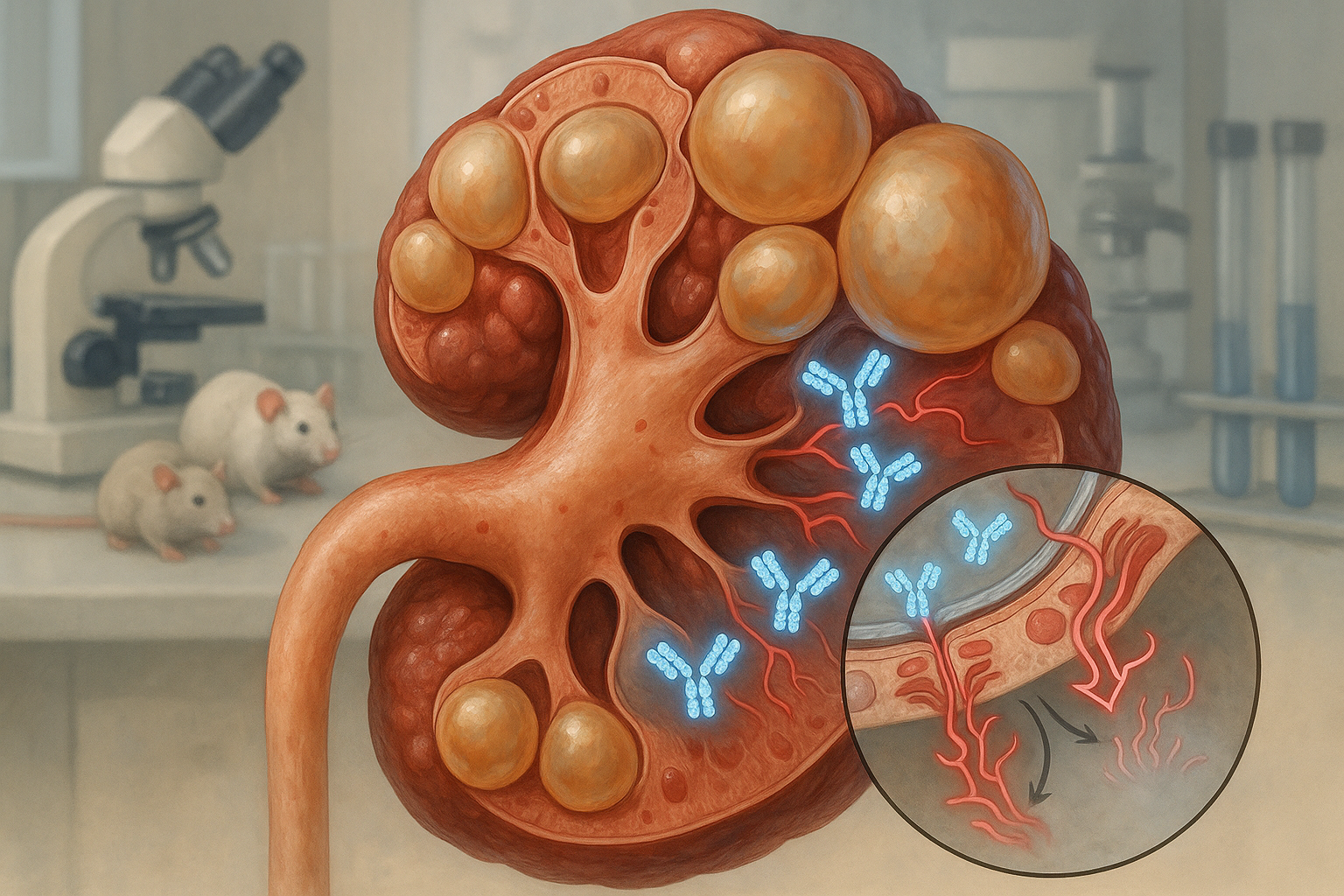
UC Santa Barbaraの研究者らは、二量体IgAモノクローナル抗体が嚢胞内皮上皮を横断し、多発性嚢胞腎症におけるcMETシグナルを抑制できると報告。げっ歯類モデルでは、嚢胞内に蓄積し、経路活性化を減少させ、疾患を遅らせ、健康組織に明らかな害を及ぼさなかったと、研究と大学の発表によると。
多発性嚢胞腎症は、液体充満嚢胞が腎臓に形成される遺伝性疾患で、しばしば組織を損傷し、進行例では透析を必要とする。治療法はない。(niddk.nih.gov)
UC Santa Barbaraの生物学者Thomas Weimbsが率いるチームは、二量体免疫グロブリンA (dIgA) 形式で設計されたモノクローナル抗体が、腎嚢胞の内部に到達し、cMET受容体を介した成長シグナルを阻害することを記述。この仕事は、Cell Reports Medicineに掲載され、第一著者Margaret F. Schimmelが主導し、動物モデルでのプレクリニカルテストを詳述。(news.ucsb.edu)
「嚢胞はただ無限に成長し続けるのです」とWeimbsは述べた。「そして私たちはそれを止めたい。だから、これらの嚢胞に薬を入れ、それらを止めるようにする必要があります。」(news.ucsb.edu)
既存の小分子オプションは嚢胞成長を遅らせるが、副作用を伴う。腫瘍学で非常に成功した従来のIgG抗体は、通常嚢胞上皮を横断せず、PKDでの有用性を制限する。UCSBチームは代わりにIgGをdIgAバックボーンに再フォーマットし、嚢胞内部へのアクセスを改善。(news.ucsb.edu)
その戦略は、嚢胞内皮細胞に豊富なポリマー免疫グロブリン受容体 (pIgR) が、血流から嚢胞腔へのdIgAの積極的トランスサイトーシスが可能であるという以前の知見に基づく。マウスPKDモデルとヒト組織では、dIgAが嚢胞を標的としIgGはそうでなかったため、dIgAベースの治療の根拠を支持。(pmc.ncbi.nlm.nih.gov)
新しい研究では、cMETに対するdIgA抗体がマウスおよびラットモデルで嚢胞内に局在し、cMET活性を減少させ、疾患進行を遅らせ、検出された有害影響なしと著者らは報告。大学の要約はまた、治療後の嚢胞上皮細胞での「劇的なアポトーシス開始」を指摘—しかし健康な腎組織ではなし—。(pmc.ncbi.nlm.nih.gov)
研究はプレクリニカルである。仕事の資金調達にはNational Institutes of Healthと米国国防総省からの助成金が含まれる。論文に記載された共同著者はBryan C. Bourgeois, Alison K. Spindt, Sage A. Patel, Tiffany Chin, Gavin E. Cornick, Yuqi LiuおよびWeimbs。(pmc.ncbi.nlm.nih.gov)
今後について、Weimbsはチームが嚢胞液に見つかる複数の成長因子と受容体に対する抗体を比較—潜在的に組み合わせ—し、最も効果的な戦略を特定することを目指すと述べた。パートナーシップと製造アクセスが必要で、追加候補を生産・テストする。「いくつかの異なる成長因子と受容体のブロックを比較するのは良いアイデアで、おそらく並べて…それが次のステップです」と彼は言った。(news.ucsb.edu)