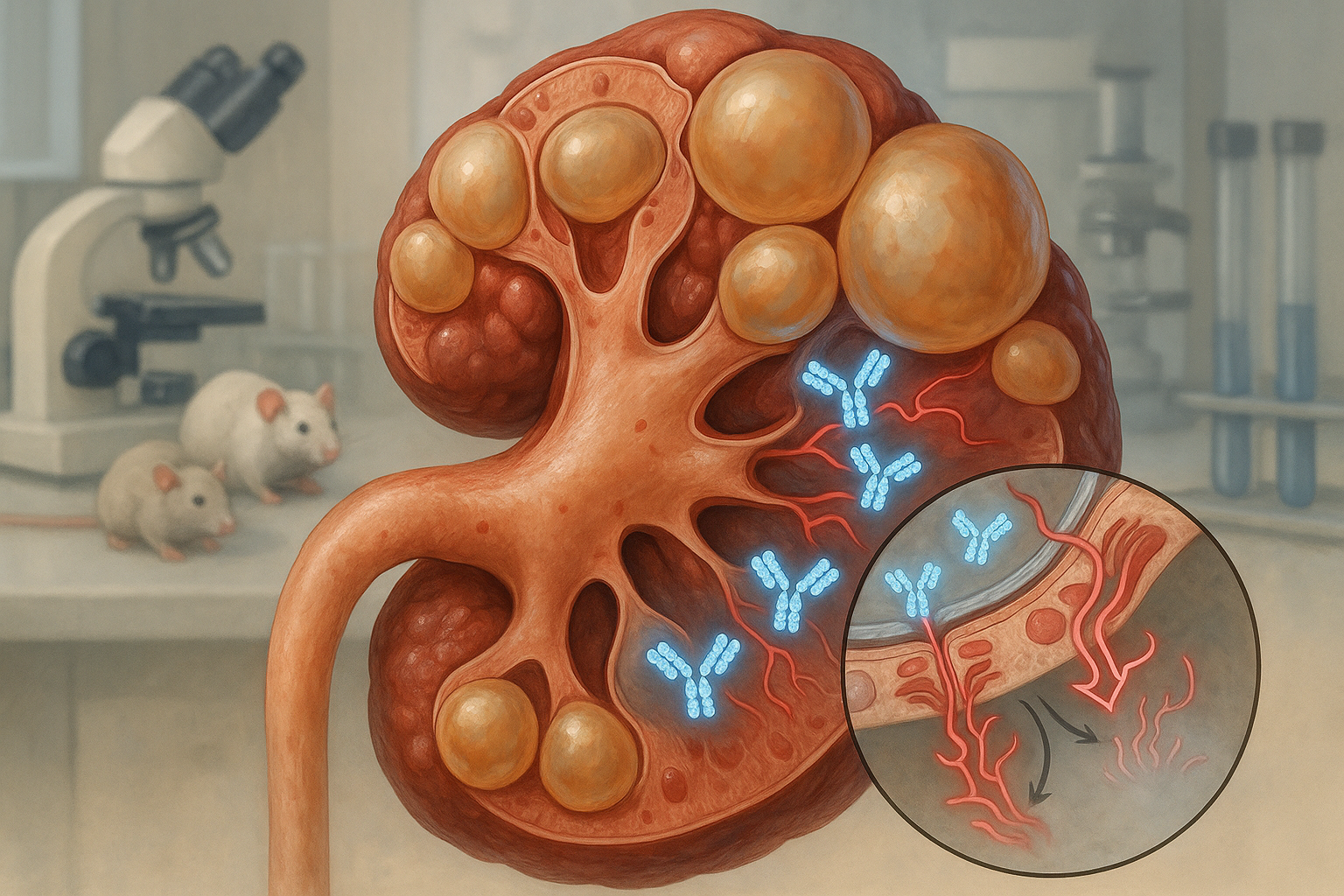
Investigadores de UC Santa Barbara informan sobre un anticuerpo monoclonal IgA dimérico que puede atravesar las epitelios que revisten los quistes y atenuar la señalización de cMET en la enfermedad poliquística renal. En modelos de roedores, se acumuló dentro de los quistes, redujo la actividad de la vía y ralentizó la enfermedad sin daño aparente al tejido sano, según el estudio y el comunicado de la universidad.
La enfermedad poliquística renal es un trastorno genético en el que se forman quistes llenos de líquido en los riñones, a menudo dañando el tejido con el tiempo y, en casos avanzados, llevando a la diálisis. No hay cura. (niddk.nih.gov)
Un equipo de UC Santa Barbara liderado por el biólogo Thomas Weimbs describe un anticuerpo monoclonal diseñado en formato de inmunoglobulina A dimérica (dIgA) para llegar al interior de los quistes renales y bloquear la señalización de crecimiento a través del receptor cMET. El trabajo, publicado en Cell Reports Medicine y liderado por la primera autora Margaret F. Schimmel, detalla pruebas preclínicas en modelos animales. (news.ucsb.edu)
“Los quistes solo siguen creciendo sin fin”, dijo Weimbs. “Y queremos detenerlos. Así que necesitamos introducir un fármaco en estos quistes que los haga parar.” (news.ucsb.edu)
Las opciones existentes de moléculas pequeñas pueden ralentizar el crecimiento de los quistes, pero conllevan efectos secundarios. Los anticuerpos IgG convencionales —altamente exitosos en oncología— típicamente no atraviesan el epitelio del quiste, limitando su utilidad en EIP. El equipo de UCSB en su lugar reformateó un IgG en una estructura dIgA para mejorar el acceso al interior de los quistes. (news.ucsb.edu)
Esa estrategia se basa en hallazgos anteriores de que el receptor de inmunoglobulina polimérica (pIgR), abundante en las células que revisten los quistes, puede transcitosis activamente dIgA desde el torrente sanguíneo hacia los lúmenes de los quistes. En modelos de EIP en ratones y tejidos humanos, dIgA apuntó a los quistes mientras que IgG no lo hizo, apoyando la justificación para terapéuticas basadas en dIgA. (pmc.ncbi.nlm.nih.gov)
En el nuevo estudio, un anticuerpo dIgA contra cMET se localizó dentro de los quistes en modelos de ratones y ratas, redujo la actividad de cMET y ralentizó la progresión de la enfermedad sin efectos adversos detectados, informan los autores. El resumen de la universidad también nota un “inicio dramático de apoptosis” en las células epiteliales de los quistes —pero no en el tejido renal sano— tras el tratamiento. (pmc.ncbi.nlm.nih.gov)
La investigación es preclínica. El financiamiento citado para el trabajo incluye subvenciones del National Institutes of Health y del Departamento de Defensa de EE.UU. Los coautores listados en el artículo son Bryan C. Bourgeois, Alison K. Spindt, Sage A. Patel, Tiffany Chin, Gavin E. Cornick, Yuqi Liu y Weimbs. (pmc.ncbi.nlm.nih.gov)
Mirando hacia el futuro, Weimbs dijo que el equipo busca comparar anticuerpos contra múltiples factores de crecimiento y receptores encontrados en el fluido de los quistes —y potencialmente combinarlos— para identificar las estrategias más efectivas. Se necesitarán asociaciones y acceso a fabricación para producir y probar candidatos adicionales. “Sería una buena idea comparar el bloqueo de varios factores de crecimiento diferentes y varios receptores, quizás uno al lado del otro… Ese sería el siguiente paso”, dijo. (news.ucsb.edu)