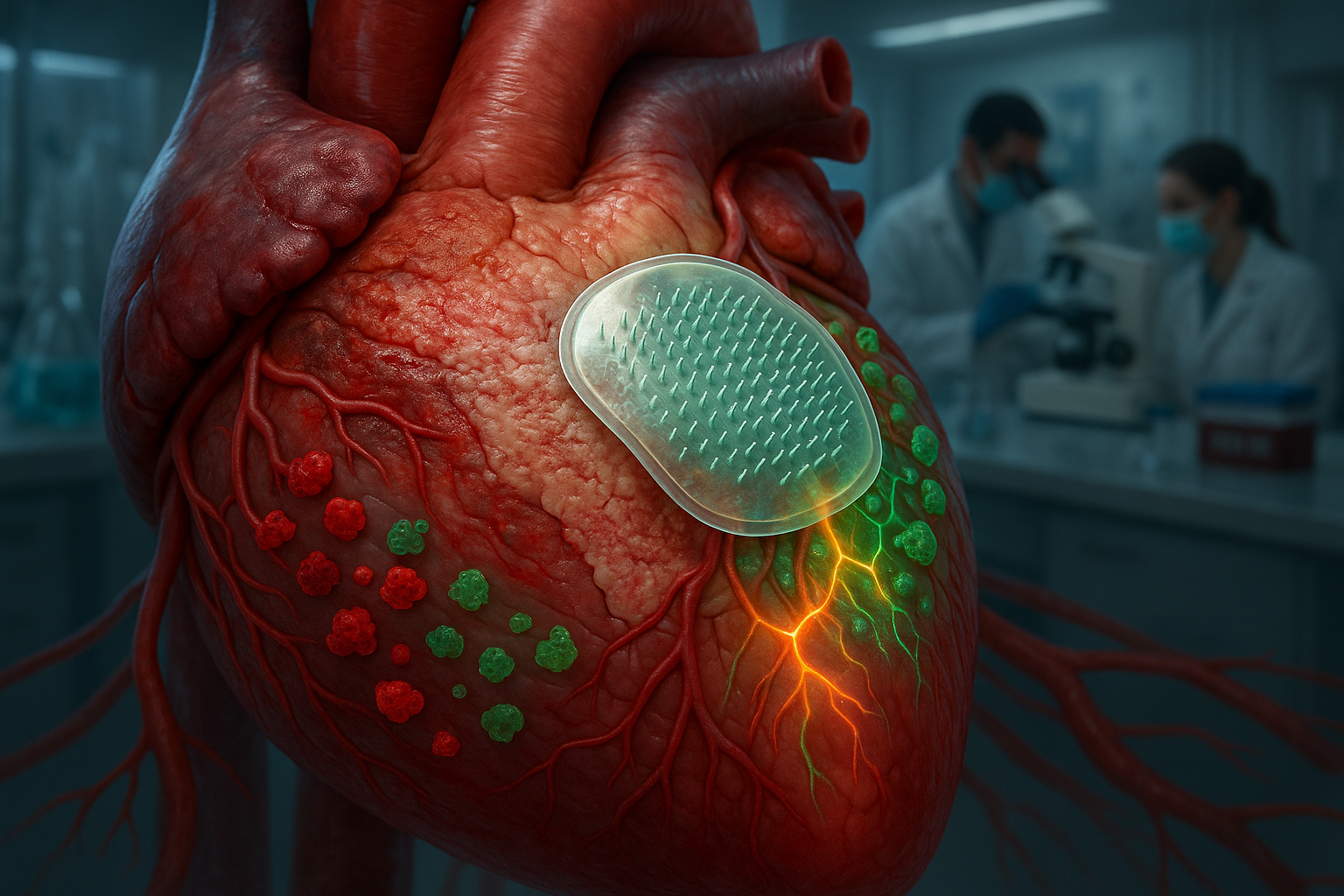
Un equipo de la Universidad Texas A&M ha desarrollado un parche biodegradable de microagujas que administra interleucina-4 directamente al tejido cardíaco dañado después de un infarto. En modelos preclínicos, este enfoque dirigido cambia las células inmunes a un modo de curación y mejora la comunicación entre las células musculares del corazón y las células de los vasos sanguíneos, evitando muchos de los efectos secundarios observados con la administración sistémica de fármacos.
Los infartos privan a las células musculares del corazón de oxígeno y nutrientes, lo que lleva a la muerte celular y la formación de tejido cicatricial. Aunque esta cicatrización ayuda a estabilizar el área dañada, no puede contraerse como el músculo sano, obligando al tejido cardíaco restante a trabajar más y potencialmente contribuyendo a la insuficiencia cardíaca con el tiempo.
Para abordar esto, un equipo liderado por el Dr. Ke Huang en la Universidad Texas A&M ha creado un parche biodegradable de microagujas que administra interleucina-4 (IL-4), una molécula conocida por regular las respuestas inmunes, directamente al tejido cardíaco lesionado. Cada microaguja del parche contiene partículas microscópicas cargadas con IL-4. Cuando se aplica el parche en la superficie del corazón, las microagujas penetran la capa externa y se disuelven, liberando el fármaco en el músculo dañado debajo, según el comunicado de Texas A&M.
Al concentrar IL-4 en el sitio de la lesión, el parche estimula a los macrófagos —células inmunes clave— a cambiar de un estado proinflamatorio a uno reparador. Este cambio ayuda a limitar la formación excesiva de cicatrices y apoya una mejor recuperación funcional en los modelos preclínicos descritos. «Los macrófagos son la clave», dijo Huang en el anuncio de la universidad. «Pueden empeorar la inflamación o ayudar a que el corazón se cure. La IL-4 les ayuda a convertirse en aliados».
Intentos previos de usar IL-4 para reparar el tejido cardíaco se basaron en inyecciones en el torrente sanguíneo, que circulaban la molécula por todo el cuerpo y causaban efectos no deseados en otros órganos. El enfoque localizado con microagujas está diseñado para centrar el tratamiento en el corazón mientras minimiza la exposición sistémica. «La administración sistémica afecta todo el cuerpo», dijo Huang. «Queríamos dirigirlo solo al corazón».
El equipo del estudio también informó cambios notables en el comportamiento de las células musculares cardíacas tratadas, o cardiomiocitos, después de la aplicación del parche. En estudios de laboratorio y animales, los cardiomiocitos se volvieron más receptivos a las señales de los tejidos circundantes, particularmente las células endoteliales que revisten los vasos sanguíneos. Huang dijo que esta comunicación celular mejorada parecía apoyar la recuperación. «Los cardiomiocitos no solo sobrevivían, interactuaban con otras células de maneras que apoyan la recuperación», señaló.
Los investigadores observaron que el parche reducía las señales inflamatorias de las células endoteliales, que de otro modo empeorarían el daño después de un infarto. También detectaron un aumento de actividad en una vía de señalización conocida como la vía NPR1, asociada con la salud de los vasos sanguíneos y la función cardíaca general.
Por ahora, colocar el parche requiere cirugía a pecho abierto en los modelos animales utilizados. Huang y sus colegas dicen que esperan adaptar la tecnología para una administración mínimamente invasiva en el futuro, imaginando una versión que pueda insertarse a través de un tubo pequeño para hacerla más práctica en entornos clínicos.
El trabajo, financiado por los National Institutes of Health y la American Heart Association, se publicó en la revista Cell Biomaterials. El estudio, que probó el parche en modelos de infarto de miocardio en roedores y cerdos, es un esfuerzo de prueba de concepto en etapa temprana y aún no está disponible como tratamiento para pacientes.
Mirando hacia adelante, Huang colabora con Xiaoqing (Jade) Wang, profesora asistente de estadística en el College of Arts and Sciences de Texas A&M, en un modelo de inteligencia artificial para mapear respuestas inmunes y guiar futuras terapias inmunomoduladoras. «Esto es solo el comienzo», dijo Huang. «Hemos demostrado el concepto. Ahora queremos optimizar el diseño y la administración».